南昌大学李志鹏特聘研究员、何伟炜副教授Carbohydrate Polymers发表重要综述
- 2026-05-25 15:34:41

作为自然界中研究最为深入的生物活性多糖之一,β-葡聚糖因其卓越的免疫调节功能,被誉为“免疫黄金”。然而,β-葡聚糖的免疫调节机制究竟是怎样的?面对来源复杂、结构多样的β-葡聚糖,如何通过前沿生物技术实现“精准制造”?南昌大学李志鹏特聘研究员(通讯作者)与何伟炜副教授(第一作者)在Carbohydrate Polymers(中科院一区,TOP期刊)发表了题为“Deciphering immunoregulatory mechanisms and structure-guided biosynthesis of β-glucans”的综述论文,系统性地阐述了β-葡聚糖的免疫调节机制,并创新性地提出了“结构导向的生物合成”策略,为下一代功能性食品原料的开发提供了重要思路。

食源性β-葡聚糖特征

β-葡聚糖广泛存在于谷物(如燕麦、大麦)、真菌(如香菇、灵芝、酵母)、微藻及细菌中,但不同来源β-葡聚糖的结构特征存在显著差异。谷物来源β-葡聚糖多为线性结构,主要由β-(1→3)和β-(1→4)糖苷键连接;真菌来源(如灵芝、酵母)β-葡聚糖往往具有更高的生物活性,其特征在于拥有β-(1→3)主链和β-(1→6)侧链分支,且不仅容易形成更为稳定的三螺旋结构,其独特的分支度也是开启免疫开关的关键钥匙。
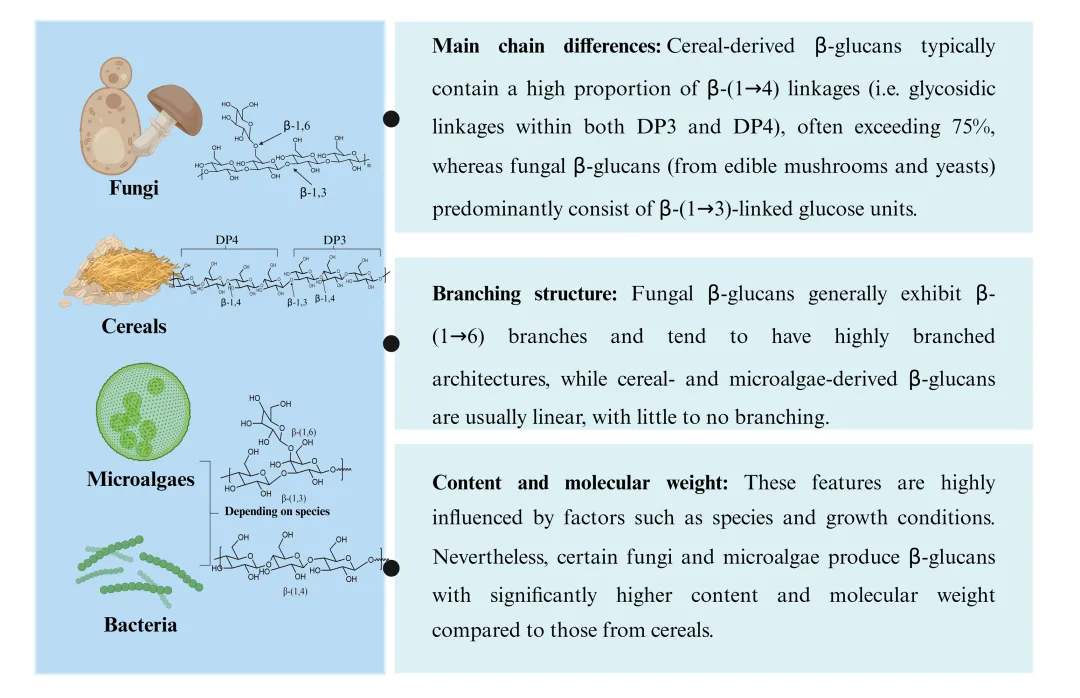
图 不同来源β-葡聚糖的结构特征

β-葡聚糖的肠道吸收和药代动力学

β-葡聚糖虽属于 膳食纤维,但少量可通过被M细胞转运至淋巴系统、被树突状细胞直接捕获,或小分子经上皮细胞微胞饮作用进入等三种途径被肠道吸收。尽管口服生物利用度较低,但其仍通过肠道局部或菌群介导发挥显著免疫调节作用,注射给药可获得更高活性。入血后,β-葡聚糖呈现双相消除模式,主要分布并代谢于肝脏和肾脏。其降解依赖肝脏P450酶、肾脏及血液免疫细胞。最终排泄遵循分子量依赖规律:小分子主要经肾脏由尿液排出,大分子则多经肝脏由胆汁排泄。
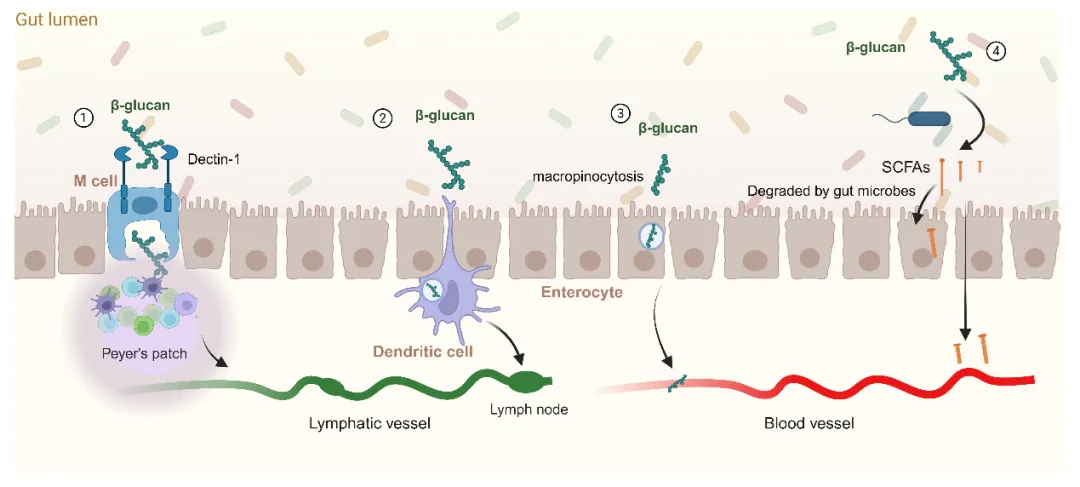
图 β-葡聚糖在肠道内的吸收与利用机制

β-葡聚糖调节宿主免疫的非肠道菌群依赖机制

β-葡聚糖能像一把“钥匙”,直接插入先天免疫细胞表面的“锁孔”——模式识别受体PRRs,如Dectin-1、TLR2/4、CR3等。结合后,能激活NF-κB、MAPK等信号通路,促使巨噬细胞、树突状细胞等“免疫哨兵”进入战斗状态,增强对病原体的吞噬能力。更有趣的是,β-葡聚糖可通过表观遗传重编程和代谢重塑,使先天免疫细胞产生“记忆,当身体再次遭遇病毒或细菌入侵时,这些受过“训练”的细胞能反应得更快、更猛烈。
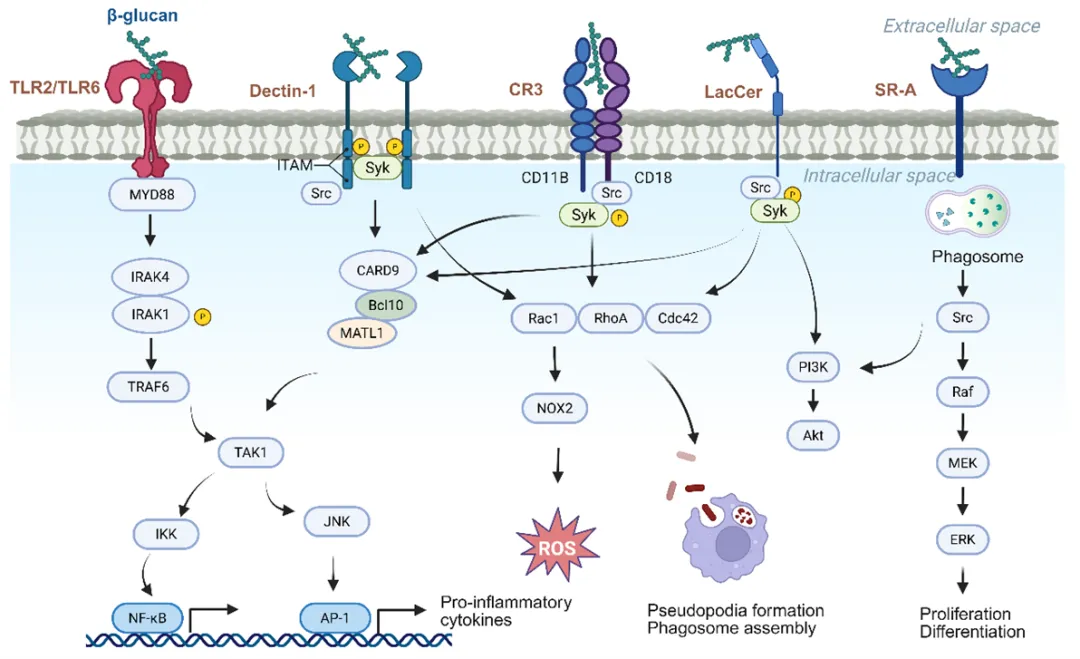
图 β-葡聚糖通过多种模式识别受体触发并调节免疫应答
β-葡聚糖虽不能作为抗原直接激活B细胞或T细胞,但能作为高效佐剂增强适应性免疫。在体液免疫方面,它通过结合B细胞表面的Dectin-1受体,促进B细胞分化为浆细胞及生发中心B细胞扩增,从而增强抗体分泌及亲和力成熟。在细胞免疫方面,它主要通过诱导DC细胞成熟及表达共刺激分子,间接激活T细胞。此外,β-葡聚糖能重塑肿瘤微环境,逆转DC免疫抑制状态,并能协同增强PD-1/PD-L1抑制剂的抗肿瘤疗效。
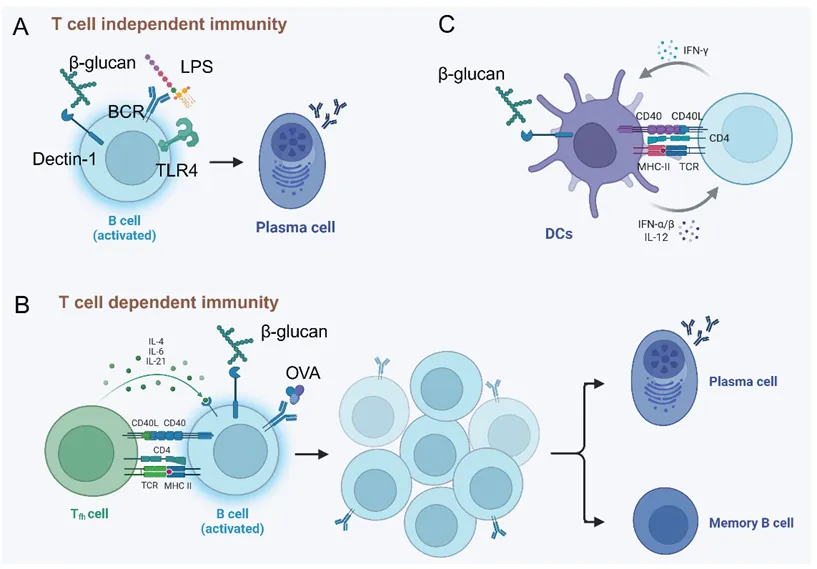
图 β-葡聚糖对适应性免疫的调节作用

β-葡聚糖调节宿主免疫的肠道菌群依赖机制

口服的β-葡聚糖大部分无法被直接吸收,而是作为优质的“益生元”进入结肠。通过菌群发酵,β-葡聚糖能促进双歧杆菌、拟杆菌等有益菌的增殖。其代谢产物短链脂肪酸不仅能修复肠道屏障,防止内毒素入血,还能调节全身的炎症反应,改善肥胖、胰岛素抵抗等代谢疾病。
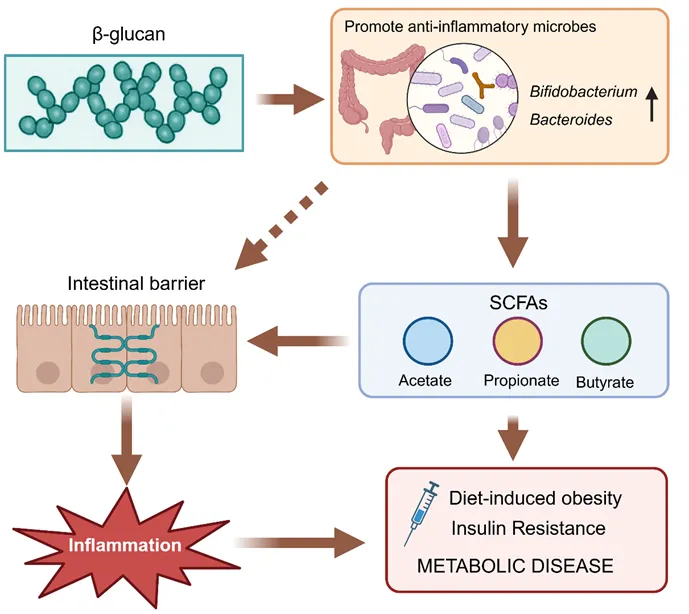
图 β-葡聚糖通过调节肠道菌群及其代谢产物,增强肠道屏障并缓解慢性炎症,从而改善代谢性疾病

β-葡聚糖免疫调节活性的构效关系

β-葡聚糖的一级结构决定其与受体的亲和力:具有β-(1→6)分支的β-(1→3)主链结构对Dectin-1的亲和力最强,显著优于线性β-(1→3)或单一β-(1→6)结构,且特定的分支比例(如1:3或1:4)能诱导更强的免疫刺激;二级结构中,稳定的三螺旋构象比单螺旋构象更易被Dectin-1识别,因而表现出更高的免疫及抗癌活性。分子量对活性的影响尚无定论,不同来源的β-葡聚糖表现各异,需结合给药途径具体分析。因此,针对特定结构(如三螺旋、特定分支)的合成生物学设计将是提升β-葡聚糖疗效的关键方向。
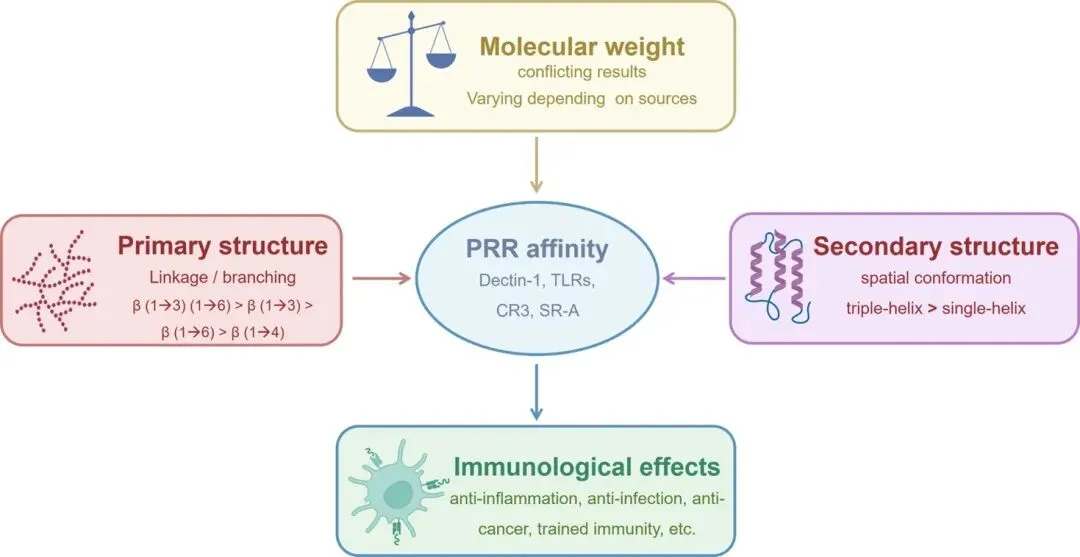
图 β-葡聚糖结构特征与其免疫效应之间的关系

β-葡聚糖制备现状以及未来生物合成技术趋势

尽管真菌来源的β-葡聚糖活性优异,但传统的提取方法面临着自然资源有限、提取工艺复杂、批次间质量不稳定的瓶颈。部分珍稀药用真菌(如冬虫夏草)的培养条件更是极为苛刻。如何打破这一僵局?团队提出了前瞻性的解决方案——“结构导向的生物合成”。文章深入探讨了利用合成生物学和基因工程技术(如CRISPR/Cas9基因编辑、多基因共过表达等)进行底盘细胞改造的策略。精准设计方法:通过基因工程改造微生物底盘细胞(如酵母),定向引入β-(1→6)侧链合成酶基因,让微生物直接生产出具有特定分支度、特定分子量的高活性β-葡聚糖。底盘优化方法:通过调控关键基因(如GLS、UGP)的表达,结合发酵条件的优化(碳氮源调节),实现β-葡聚糖的高效、低成本、规模化生产。
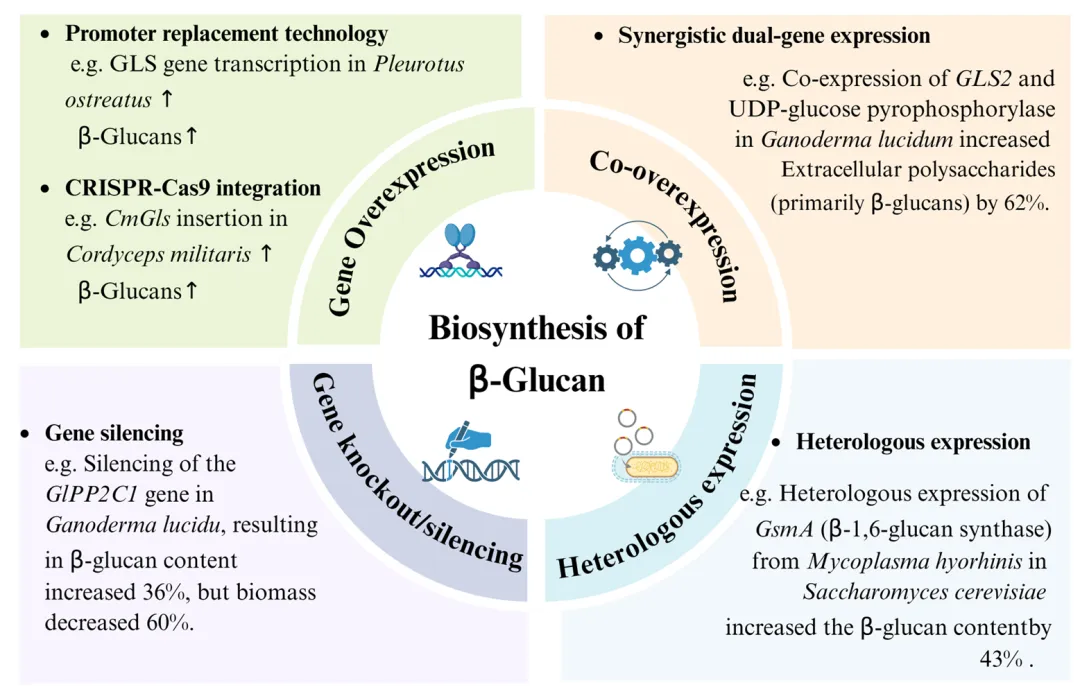
图 基因工程技术在生物合成β-葡聚糖中的应用
综上,文章系统阐述了β-葡聚糖在分子层面的直接免疫识别机制,以及通过调节肠道菌群介导的间接免疫调节通路。在此基础上,文章剖析了传统制备技术的局限性,并提出了利用合成生物学策略构建下一代高效生物合成体系的未来蓝图。
(请点击标题查看)
分子对接与分子动力学黄酮类化合物
食品感官科学与分析农产品贮藏与加工
肉与肉制品蛋与蛋制品水产品
奶及奶制品豆及豆制品果蔬及果蔬制品
大米及米制品
炎症性肠病糖尿病肝病神经疾病
(请点击标题查看)
(请点击学者姓名查看)


在线投稿平台链接:https://www.wjx.top/jq/85151447.aspx
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅仅是出于学术交流和传播信息的需要,并不意味着代表本平台观点或证实其内容的真实性;转载文章版权归原作者所有,作者如果不希望被转载或有侵权行为,请联系本平台删除。由于编译水平有限,推文或简历有不妥之处,深感抱歉,请联系本平台修改或者删除。
