TransMed | 南昌大学江西医学院第一附属医院刘芬教授团队—脓毒症诱导的PICS:免疫代谢机制、新兴生物标志物与精准化管理
- 2026-04-19 07:49:09
近日,南昌大学江西医学院第一附属医院重症医学科刘芬教授团队在TransMed发表了题为“Sepsis-induced PICS: immunometabolic mechanisms, emerging biomarkers, and precision management”的文章。

英文题目:Sepsis-induced PICS: immunometabolic mechanisms, emerging biomarkers, and precision management
中文题目:脓毒症诱导的PICS:免疫代谢机制、新兴生物标志物与精准化管理
原文链接:https://www.sciencedirect.com/science/article/pii/S3117397726000097
DOI:10.1016/j.tmed.2026.100009
第一作者:黄美玲,杨馨怡,李春帆
通讯作者:温学欢,刘芬,白松杰
主要单位:南昌大学江西医学院第一附属医院
摘要
脓毒症是由感染引发的危及生命的器官功能障碍。许多幸存患者会进展为“持续性炎症、免疫抑制和分解代谢综合征(PICS)”,这是一种极度消耗机体的病理状态。尽管临床上对其日益重视,但PICS复杂的病理生理机制仍未完全阐明。本文通过系统梳理现有研究基础并结合单细胞测序领域的前沿进展,全面构建了PICS的病理机制框架。我们首先回顾了PICS诊断标准的演变历程及其局限性;随后,深入剖析了介导PICS“核心三联征”的关键分子与细胞机制。然后,本文总结了PICS动物模型的发展现状及其在机制研究中的应用。最后,我们评估了用于PICS诊断的新兴生物标志物,并探讨了靶向免疫调节与代谢支持的个体化治疗策略。本文旨在通过整合系统性病理机制框架,推动新型诊断工具与靶向干预措施的研发,从而最终改善脓毒症幸存患者的远期预后。
研究亮点:
脓毒症晚期表现出严重的免疫抑制与分解代谢增加。
单细胞组学揭示脓毒症中过度炎症与免疫抑制并存的双重特征。
现行PICS诊断标准亟需整合影像学及免疫学等多模态指标。
1.引言
脓毒症是由感染引发的危及生命的临床综合征,以进行性器官功能障碍为核心。全球每年发病约1.66亿例,死亡超2140万例,医疗负担沉重。脓毒症的病理生理核心在于免疫失调:早期过度炎症引发急性器官衰竭与死亡;随病程进展,机体陷入严重且持久的免疫抑制,极易发生继发感染。现代重症监护技术虽显著降低了早期死亡率,但患者远期死亡率仍高达50%-70%。因此,逆转晚期脓毒症的持续免疫抑制状态,已成为改善预后的当务之急。
晚期脓毒症幸存者常表现出ICU住院时间延长、C反应蛋白(CRP)持续升高、淋巴细胞减少及伴有显著体重下降的严重分解代谢等共同特征。为概括这一慢性危重症表型,Gentile等于2012年提出了“持续性炎症、免疫抑制和分解代谢综合征”(PICS)的概念,其典型临床特征为重度淋巴细胞减少及单核细胞HLA-DR表达下降。作为脓毒症严重的远期遗留问题,PICS提出十余年来,其分子机制研究进展依然缓慢,高质量临床证据匮乏,使得该综合征的诊疗仍面临巨大挑战。
近十年来,高通量测序与多组学技术为探究疾病机制提供了强大工具。单细胞测序技术更以前所未有的解析度精准识别了关键致病细胞亚群。本综述将前沿多组学技术与分子致病机制深度融合:临床层面,梳理PICS诊断标准的演变;机制层面,结合单细胞测序成果,剖析PICS核心三联征的内在病理途径。此外,本文还评估了现有动物模型,并探讨了新兴生物标志物及潜在干预策略。本综述旨在搭建基础研究与临床转化之间的桥梁,为构建PICS的病理机制框架与精准化管理提供参考。
2. PICS定义的演变轨迹
1992年,脓毒症被首次定义为由感染引发的全身炎症反应综合征。随着研究深入,学者们发现机体在促炎的同时,也会启动由IL-4、IL-10等细胞因子介导的抗炎反应。当抗炎反应占主导时,即表现为代偿性抗炎反应综合征,患者陷入免疫抑制,单核细胞HLA-DR表达下降,极易发生继发感染。2003年后,学界逐渐认识到脓毒症并非单纯的炎症反应,而是伴随复杂的急性器官功能障碍。这一观念转变最终促成了2016年Sepsis-3.0的发布,将脓毒症重新定义为“宿主对感染的反应失调引起的危及生命的器官功能障碍”。
随着现代重症复苏与器官支持技术的进步,多数脓毒症患者能挺过急性感染期,但其中很大一部分却陷入了“既未急性死亡,也未完全康复”的慢性危重症(CCI)状态。这类患者常伴有严重的肌肉消耗、代谢紊乱、认知障碍及机会性感染易感性增加。目前CCI尚无统一标准,临床多指气管切开、长期机械通气或ICU住院>14天的患者;而持续性危重症(PerCI)则特指ICU住院>10天的群体。荟萃分析显示,约28%的脓毒症患者会进展为PerCI或CCI,其远期预后极差,院内及1年死亡率分别高达27%和45%。
为精准识别这类病程迁延的外科ICU患者,Gentile等于2012年首次提出了PICS的概念。其初始诊断框架包括:持续性炎症(ICU住院>10天且CRP >150 μg/dL);免疫抑制(总淋巴细胞 <0.8×10⁹/L);分解代谢(住院期间体重下降>10%,或BMI、白蛋白等指标显著降低)。从概念上看,CCI代表一种广泛的慢性未恢复状态,而PICS则是CCI中一种特定的病理生理内型,它精准描绘了这部分高危人群“炎症迁延、免疫瘫痪与代谢消耗”的核心特征。
PICS标准提出后,其临床适用性在验证中不断演变。Hesselink等研究指出,早期单纯依赖CRP和淋巴细胞等实验室指标诊断PICS的敏感性(44%)和阳性预测值(36%)极低,无法准确预测复发性感染等临床结局,提示诊断框架必须以临床结局为导向。为适应异质性更广的ICU人群,Mira等将标准调整为ICU住院>14天且CRP >50 μg/dL。2022年,Nakamura等基于441例ICU患者数据开发了机器学习诊断模型,将其评估节点锁定在入ICU第14天,并进一步将CRP阈值降至>20 μg/dL,这一调整更准确地反映了PICS特有的“低级别迁延性炎症”表型。
综上所述,PICS是脓毒症幸存者中具有重要临床意义的亚群。然而,现有诊断体系仍面临诸多局限:CRP、淋巴细胞及白蛋白等常规标志物缺乏特异性且易受临床干预干扰;连续体重监测在常规操作中难以落实;更为关键的是,不同临床场景(如多发伤、心脏术后、ECMO支持)下PICS的病理机制差异巨大,亟需建立基于特定场景的诊断框架。未来研究应优先致力于开发大数据驱动的动态预测模型,并挖掘新型生物标志物,以实现PICS的精准识别、风险分层与个体化治疗。
3. PICS的病理生理机制
3.1. 持续性炎症
持续性炎症是PICS患者的核心临床特征,其严重程度与死亡率密切相关。在脓毒症中,先天免疫系统的模式识别受体(PRRs)通过识别病原相关分子模式(PAMPs)和损伤相关分子模式(DAMPs),激活NF-κB、cGAS-STING等下游信号通路,引发级联炎症反应。在脓毒症后期,尽管抗生素治疗使PAMPs水平显著下降,但DAMPs的持续存在是驱动PICS慢性炎症的关键。例如:释放到胞外的氧化型HMGB1、胞外冷诱导RNA结合蛋白(eCIRP)、胞外ATP及线粒体DNA(mtDNA)等,持续通过TLR4、NLRP3炎症小体或cGAS-STING通路激活免疫细胞。这种PAMPs和DAMPs的持续刺激最终导致免疫细胞陷入“免疫瘫痪”并诱发免疫耐受。尽管靶向抑制DAMPs在动物模型中显示出减轻炎症的潜力,但其在PICS患者中的确切作用仍需大规模队列研究验证。
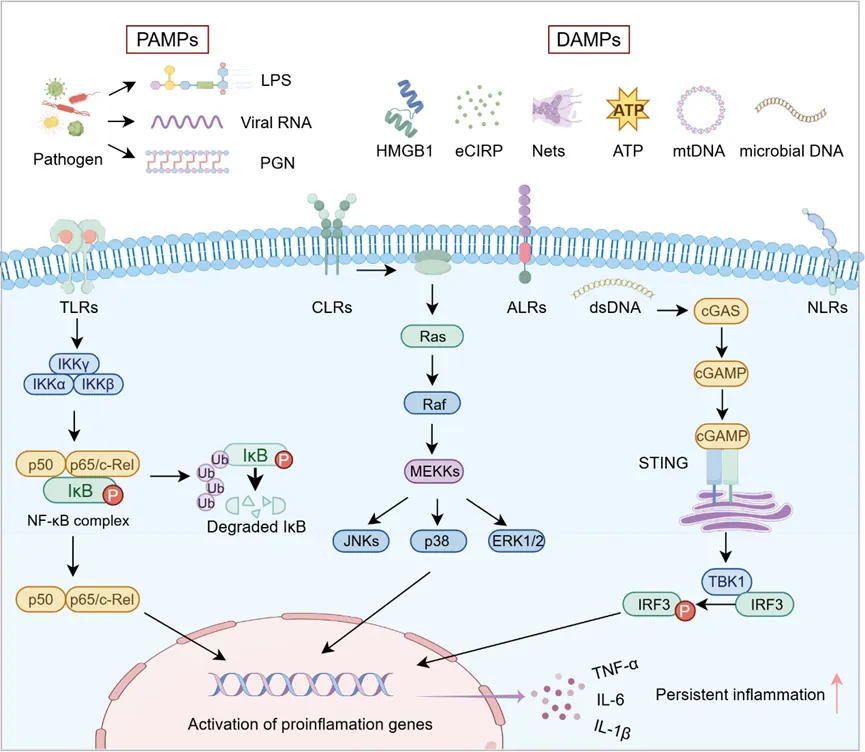
代表图1. PICS中持续性炎症的机制模式图
3.2. 免疫抑制
3.2.1. 单核细胞
单细胞RNA测序(scRNA-seq)揭示,脓毒症中的单核细胞呈现高度异质性,远超传统的CD14/CD16分类。研究发现,脓毒症患者外周血中出现了一种以HLA-DR低表达、S100A高表达(如MS1亚群)为特征的功能障碍单核细胞。这类细胞的抗原呈递能力严重受损,代谢从氧化磷酸化转向糖酵解并迅速走向代谢耗竭。更重要的是,它们能强效抑制T细胞增殖并诱导调节性T细胞(Tregs)的分化。这种“高促炎与重度免疫抑制”并存的单核细胞表型,其丰度与脓毒症严重程度高度相关。
3.2.2. 中性粒细胞
中性粒细胞在脓毒症中是一把“双刃剑”。急性期强烈的炎症刺激会触发骨髓的“紧急粒细胞生成”,释放大量未成熟的中性粒细胞入血。scRNA-seq及功能学研究表明,这些未成熟/功能失调的中性粒细胞不仅吞噬杀菌能力低下,还会通过PD-L1等直接接触途径,强效抑制T细胞的激活与增殖,并促进Tregs的生成。这表明在脓毒症中,未成熟中性粒细胞是介导全身免疫抑制的关键因素。
3.2.3. 树突状细胞 (DCs)
作为连接固有与适应性免疫的桥梁,DCs在脓毒症中遭遇了严重的数量枯竭与功能瘫痪。无论在急性期还是PICS阶段,患者的髓系DCs和浆细胞样DCs数量均显著下降,且表面HLA-DR表达广泛下调,导致抗原呈递能力严重受损。近期单细胞图谱研究进一步识别出一种“无能/耐受型”DC表型(表达高水平PD-L1的mregDCs)。这类处于“功能耗竭”的DCs不仅无法启动有效的抗感染免疫,反而通过分泌大量IL-10等抑制性因子,介导免疫抑制状态。
3.2.4. T细胞
适应性免疫衰竭是晚期脓毒症免疫抑制的重要特征。在PICS阶段,患者脾脏及外周血中的CD4+和CD8+ T细胞发生大规模凋亡(耗竭),而具有免疫抑制作用的Tregs显著扩增。同时,残存T细胞表面的免疫检查点分子(如PD-1、CTLA-4、BTLA)表达上调,导致其增殖、活化及抗病毒能力长期受损。这种广泛的T细胞功能障碍由多种因素共同驱动,包括表观遗传修饰(如miR-31下调)以及持续存在的DAMPs(如HMGB1、eCIRP)的外部干预。
3.2.5. B细胞
B细胞不仅负责抗体产生,更是调控脓毒症从“细胞因子风暴”向“免疫抑制”转变的核心枢纽。脓毒症会导致严重的B细胞减少(尤其是记忆B细胞),且存活B细胞处于易凋亡的过度活化状态。对于调节性B细胞(Bregs),其在不同病理阶段作用复杂:成年患者中Bregs的缺失与极高死亡率相关;而在某些特定微环境中,Bregs又会分泌过量IL-10抑制Th1反应。其机制涉及胞外ATP/腺苷代谢通路的异常,以及β-淀粉样蛋白-CD74轴对B细胞转录程序的抑制。
3.2.6. 髓源性抑制细胞 (MDSCs)
MDSCs并非固定的细胞系,而是在重症感染等病理状态下由髓系细胞转化而来的一种“强效免疫抑制功能态”。在脓毒症中,尤其是粒系MDSCs(G-MDSCs)会大量扩增。值得注意的是,虽然MDSCs在早期即开始积聚,但其免疫抑制功能的全面获得往往发生在中后期(约第14天),这与PICS的发生时间窗高度契合。在DAMPs(如S100A9、HMGB1)、缺氧微环境(HIF-1α)及非编码RNAs的共同驱动下,MDSCs通过上调PD-L1和精氨酸酶等途径,介导PICS免疫抑制。
3.2.7. 脓毒症中高炎症与免疫抑制共存
传统观念认为脓毒症是“先高炎症、后免疫抑制”的双相过程。然而,单细胞层面的证据颠覆了这一认知:高炎症与免疫抑制是同时存在、相互交织的。PAMPs和DAMPs在驱动剧烈炎症的同时,触发骨髓释放大量未成熟、功能失调的髓系细胞(如HLA-DR低表达单核细胞、未成熟中性粒细胞及MDSCs)。这些细胞在重度炎症的驱动下获得了强大的免疫抑制特性,它们通过下调抗原呈递、上调免疫检查点和分泌抑制性介质,导致效应T/B细胞的广泛耗竭,最终使机体陷入高炎症与免疫瘫痪并存的恶性循环。
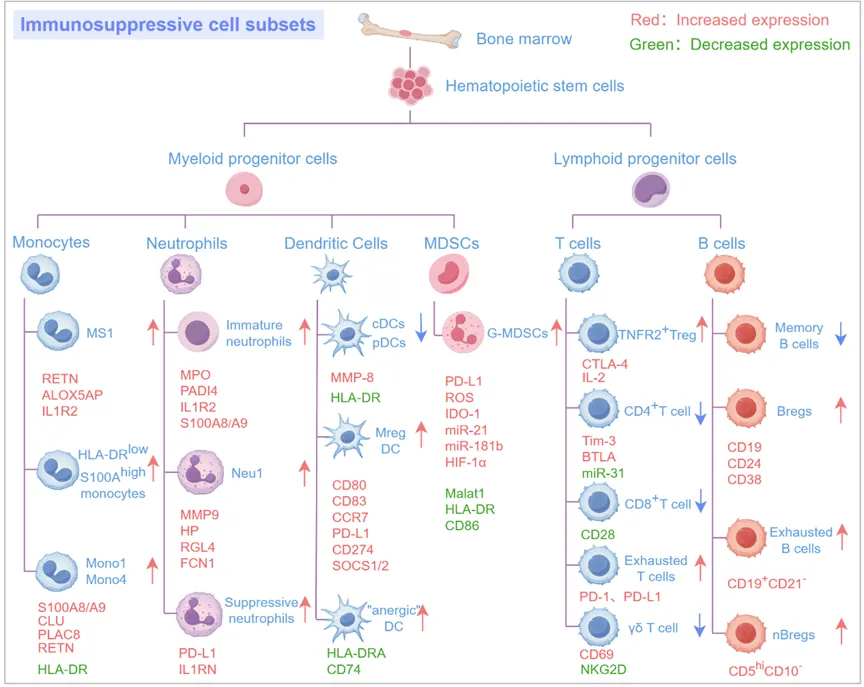
代表图2. PICS中免疫抑制的细胞全景图
3.3. 分解代谢
PICS患者长期的住院状态与持续性炎症会引发严重的分解代谢与营养耗竭,导致显著的肌肉萎缩和ICU获得性衰弱,极大地阻碍了患者生活能力的恢复。临床上,该状态表现为白蛋白、胰岛素样生长因子结合蛋白3下降,而胰高血糖素样肽-1及尿3-甲基组氨酸升高。转录组学揭示,脓毒症患者肌肉组织中存在核糖体生物合成受损及泛素-蛋白酶体系统的过度激活,并伴随线粒体功能障碍、氧化应激加剧与细胞死亡通路的激活。
持续性炎症是驱动脓毒症肌萎缩的核心因素。研究发现,晚期脓毒症肌肉组织中存在大量中性粒细胞浸润,其持续释放的NETs加剧了局部炎症。此外,高表达的S100A8/A9通过结合RAGE受体,激活Drp1蛋白磷酸化,引发线粒体过度分裂、ATP产能骤降,直接导致肌细胞萎缩。靶向抑制S100A8/A9或Drp1有望成为缓解肌萎缩的有效策略。
作为脓毒症的重要特征,肠道微生态失调同样扮演着关键角色。肠屏障受损导致大量PAMPs、DAMPs及有害代谢物“泄漏”入血,加剧全身炎症。粪菌移植实验证实,将PICS小鼠的粪便菌群移植给脓毒症小鼠会显著加重受体的肌萎缩。测序结果显示,PICS模型中条件致病菌大量富集,而参与色氨酸代谢的有益菌显著减少。补充色氨酸代谢物(如吲哚-3-乳酸)能有效修复肠屏障并缓解肌萎缩,凸显了“肠-肌轴”在分解代谢中的调控枢纽作用。
在分子通路层面,多种机制共同促成了肌肉蛋白的丢失:(1) 肌肉组织中Gasdermin D的活化促使成熟IL-18释放,通过AMPK/FOXO3a轴上调肌肉特异性E3泛素连接酶(Atrogin-1和MuRF1),加速蛋白降解;(2) 肌肉驻留的2型固有淋巴细胞(ILC2s)因PD-1高表达而陷入免疫耗竭,丧失了分泌组织修复因子IL-13的能力,导致慢肌纤维损伤;(3) 转录因子ZBED6的异常升高可抑制DOCK3基因转录,进而阻断PI3K/AKT合成通路,导致肌肉蛋白合成减少。目前针对脓毒症肌萎缩的临床研究仍极度匮乏,亟待探索新的治疗策略。
总体而言,PICS的病理机制绝非单一过程的线性叠加,而是一个由多重病理状态相互交织、不断强化的恶性循环。其核心由“持续性炎症、免疫抑制与分解代谢”三联征构成。其中,持续性炎症往往是始动因素,驱动着晚期的免疫抑制与严重分解代谢;而免疫缺陷又反过来导致感染难以清除、炎症迁延不愈;同时,严重的肌萎缩阻碍了患者的远期康复。这种高度复杂的交互网络提示,未来针对PICS的临床干预必须摒弃单一靶点思维,转向更为系统、整合的多维协同治疗策略。
4. PICS的动物模型
盲肠结扎穿孔(CLP)模型是研究脓毒症的基石。通过调整结扎长度,该模型可精准调控疾病严重程度(如50%结扎对应中度,75%对应重度),并在小鼠中诱发显著的多器官功能障碍。在CLP模型的基础上,研究者们为深入探索PICS的病理机制,不断改良并开发了多种PICS动物模型。
2017年,Pugh等人首次系统构建了PICS小鼠模型。他们采用33%盲肠结扎加单次穿刺构建中度脓毒症,且全程不使用抗生素或镇痛药以排除药物干扰。该模型在术后第8天精准再现了PICS的三大核心特征:(1) 持续性炎症(多器官中性粒细胞增多);(2) 免疫抑制(T细胞亚群锐减,未成熟巨噬细胞扩增,且对二次铜绿假单胞菌感染的清除能力和存活率严重下降);(3) 高分解代谢(持续消瘦及大腿肌质量减少)。为模拟PICS患者因二次感染导致的病情急剧恶化,Chen等人在CLP联合抗生素治疗的基础上,于第11天腹腔注射LPS,构建了“二次打击”模型(定义为“PIICS”)。相比单一PICS模型,PIICS小鼠展现出更严重的体重下降、低白蛋白血症及肌萎缩基因的高表达。该模型最突出的优势是呈现出CLP后和LPS注射后的“双相死亡高峰”,极大地还原了临床患者因二次感染致死的病程轨迹。
重症患者常伴随内源性糖皮质激素的持续升高。Wang等人通过在CLP后连续注射地塞米松来模拟这一状态。至第14天,小鼠不仅表现出典型PICS特征,还伴有严重的肠屏障破坏及肠道菌群失调。将该模型小鼠的粪便移植给单纯CLP小鼠后,受体也出现了PICS样症状,这为“肠道微生态失调是驱动PICS的关键机制”提供了直接的体内证据。为进一步模拟复杂的ICU环境,Stortz等对CLP小鼠施加每日慢性束缚应激(DCS)。研究发现,老年小鼠在DCS联合CLP的双重打击下,死亡率远超年轻小鼠,且体重持续无法恢复。至第14天,老年小鼠展现出促炎因子升高、功能性MDSCs扩增及持续消瘦等典型的PICS特征,凸显了年龄和环境应激在PICS病程中的推波助澜作用。
上述模型各有优劣:无抗生素模型排除了药物干扰,重复性极佳;抗生素治疗模型更贴近临床现实,但药物种类和剂量的异质性导致缺乏标准化;而叠加慢性应激或二次打击的模型则最高保真地还原了ICU的复杂生态。尽管现有动物模型已能重现PICS的典型特征,但由于动物年龄、感染严重程度及干预策略的巨大差异,目前仍缺乏完全标准化的PICS公认模型,且大型动物模型领域尚属空白。在未来,开发具有广泛普适性、标准化且经过严格验证的PICS动物模型,仍是该领域实现临床转化的首要任务。
5. PICS的生物标志物
PICS是一个包含炎症、免疫和代谢的复杂临床综合征。PICS的准确诊断仍然是重症医学面临的重大挑战。如前所述,目前的诊断标准存在一定的局限性。虽然在临床实践中很容易获得CRP、淋巴细胞计数和白蛋白等指标,但这些传统实验室标志物的敏感性和特异性不足,可能导致PICS的漏诊或延迟识别。
关于持续性炎症,由坏死细胞释放入血的DAMPs(如HMGB1、eCIRP、S100蛋白)持续激活固有免疫,是反映慢性炎症的潜力指标。此外,量化血浆中的微生物游离DNA有助于评估感染类型与抗生素疗效。未来需重点开展针对疾病中晚期的大规模前瞻性队列研究,以确立这些指标的诊断价值。
针对免疫抑制,常规指标中,中性粒细胞/淋巴细胞比值的持续升高是预后不良的强预测因子。而在细胞与分子层面,scRNA-seq等技术揭示了更精细的标志物:在固有免疫方面,单核细胞和DC表面HLA-DR表达的显著下调是“免疫瘫痪”的标志;同时,外周血中出现大量具有免疫抑制特性的未成熟中性粒细胞。在适应性免疫方面, T细胞表面免疫检查点分子(PD-1、CTLA-4、TIM-3)的高表达标志着“T细胞耗竭”;同时伴有Tregs和Bregs比例的失衡。血浆中抗炎细胞因子(IL-10、TGF-β、IL-4、IL-35)及腺苷浓度的显著升高,都是免疫抑制的潜在指标。
对于分解代谢,除了肌酐身高指数外,尿素/肌酐比值是另一个重要的指标;该比值升高反映了肌肉蛋白质分解的加速。3-甲基组氨酸是肌肉降解的特异性产物,其尿液水平升高表明肌肉发生显著流失。此外,生长分化因子-15(GDF-15)也是一个关键的生物标志物。作为一种应激反应激素,其最初的升高旨在保护机体并限制过度损伤。然而,GDF-15的持续高表达会加剧肌肉萎缩、体重下降和营养不良,使其成为评估分解代谢的一个重要预后指标。
值得注意的是,目前的诊断体系过度依赖血液化验,缺乏影像学等多维数据。Huang等人通过腹部CT测量L3椎体骨骼肌横截面积变化(ΔSMI)来量化肌肉萎缩,证实肌肉流失越快,脓毒症患者死亡风险越高。这凸显了将超声和CT等影像学纳入诊断框架的必要性。
上述标志物的临床转化仍面临一定障碍:流式细胞术与单细胞测序等技术门槛及成本过高;PICS的动态轨迹要求进行纵向连续监测而非单一基线测量;且缺乏普遍验证的标准化截断值。未来需优先开发高性价比且具标准阈值的生物标志物组合,并借助人工智能整合多模态临床与影像数据,以构建动态的PICS预测模型。
6. PICS的治疗策略
鉴于PICS在炎症、免疫抑制和分解代谢方面存在显著异质性,“一刀切”的治疗并不适用。相反,必须采取个体化、基于生物标志物指导的精准施治。
控制持续性炎症的首要任务是严格的感染源管理,包括管路护理与新发感染预防。监测上,由于常规检测PAMPs/DAMPs存在难度,动态追踪细胞因子谱具有潜在价值。治疗方面,尽管单一细胞因子单抗效果不佳,但对重度炎症患者,免疫球蛋白、多细胞因子阻断或细胞因子吸附仍是可供选择的策略。此外,新兴纳米载体有望克服传统干预缺乏组织特异性的瓶颈。
逆转免疫抑制是PICS治疗的核心。任何干预必须基于患者实时的免疫状态(如监测HLA-DR和PD-1),严禁在活跃炎症期使用免疫刺激剂以防病情恶化。GM-CSF或IFN-γ可恢复单核细胞抗原递呈并上调HLA-DR;IL-7可促进T淋巴细胞增殖,胸腺法新能促进其成熟;而免疫检查点抑制剂有望逆转T细胞耗竭。需要注意的是,现有免疫疗法数据多源自急性脓毒症或肿瘤队列,直接外推至PICS具有继发炎症的风险。T细胞工程和过继细胞疗法等前沿技术的适用性仍需进一步探索。
应对分解代谢的重点是早期充足的肠内营养与肠道菌群保护。特定术后患者可采用富含精氨酸、Omega-3、谷氨酰胺等的免疫增强饮食。此外,调控细胞免疫代谢成为前沿策略,例如通过双靶向糖酵解与STING通路的纳米颗粒重编程巨噬细胞,以增强免疫治疗。在系统层面,氧雄龙或IGF-1等合成代谢药物可减轻重度烧伤等患者的肌肉消耗。面对PICS特有的“合成代谢抵抗”,早期个体化的物理康复锻炼对于激活肌肉合成信号极为关键。
总体而言,将抑制炎症、挽救免疫和逆转分解代谢进行协同整合,是PICS的潜在治疗途径。由于现有策略多从烧伤或肿瘤领域外推而来,未来仍需在PICS的专病临床队列中验证其确切疗效。
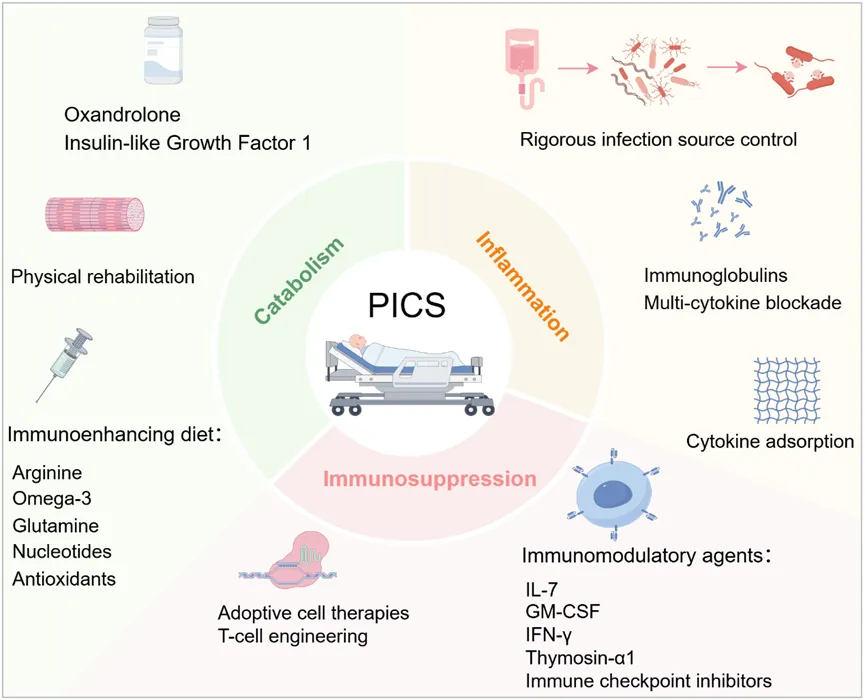
代表图3. PICS的治疗策略
7. 当前的局限性与转化挑战
尽管在揭示脓毒症诱发PICS的机制上取得一定进展,但其临床转化仍面临三大局限:首先,PICS患者群体异质性极强,在感染病因、器官损伤程度及免疫代谢表型上差异巨大。其次,缺乏标准化的多模态诊断标准。现有体系过度依赖CRP、白蛋白等传统化验指标,缺乏与影像学数据的交叉验证,无法全面反映PICS的复杂全貌,阻碍了早期识别及跨研究的横向对比。最后,现有机制研究过度依赖小鼠CLP等动物模型。这些模型虽具可重复性,但无法真实重现经历长期、复杂ICU干预患者的病理生理学轨迹。展望未来,应对这些挑战需建立多中心前瞻性队列以明确PICS的长期预后影响;构建整合细胞因子谱、免疫代谢表型与影像数据的多模态诊断框架;并开发高度还原ICU临床现实的实验模型。
8. 结论
PICS是导致脓毒症幸存者远期预后不良的关键因素,但在其诊疗体系中仍存在显著的循证空白。过去基于经验和传统标志物的诊断模式敏感度不足。为推进诊断,需探索多维度的评估体系:通过PAMPs/DAMPs评估炎症;结合HLA-DR、未成熟中性粒细胞、免疫检查点及细胞因子谱评估免疫功能;通过尿素/肌酐比值、GDF-15、尿3-甲基组氨酸并辅以超声/CT影像评估分解代谢。
在治疗层面,未来的管理模式将向生物标志物指导的多模态策略演进:以感染源控制和细胞因子清除为基础,辅以动态监测指导的精准免疫调节,并通过强化肠内营养、维持微生态、合成代谢药物及早期康复对抗分解代谢。由于诸多机制认知源于临床前观察,上述靶点亟须前瞻性干预临床试验的严格验证。未来,将人工智能与多组学技术深度融合以构建动态的PICS风险预测模型,将是改善脓毒症患者长期预后的新方向。
作者简介

黄美玲(共同一作)
南昌大学江西医学院2025级临床医学博士生。
主要研究方向:脓毒症晚期免疫抑制与肌肉萎缩的调控机制。近年来在Journal of Intensive Care、《中华急诊医学杂志》等期刊上发表多篇学术论文。

杨馨怡(共同一作)
医学博士,毕业于南昌大学,现就职于南昌大学江西医学院第一附属医院(在站博士后)。
主要研究方向:脓毒症肺损伤的分子机制;近年来在Journal of Inflammation Research、Free Radical Biology and Medicine、Functional & Integrative Genomics等期刊上发表多篇学术论文;主持院级课题1项,参与国家自然科学基金面上项目2项、江西省自然科学基金2项。

李春帆(共同一作)
南昌大学江西医学院2022级临床医学博士生。
主要研究方向:血液系统危重症疾病与重症感染。近年来,在American Journal of Therapeutics、International Journal of General Medicine等期刊上发表多篇学术论文。

温学欢(通讯作者)
医学硕士,毕业于浙江大学医学院,现就职于温州医科大学附属苍南医院。
主要研究方向:多组学生物信息分析及AI辅助临床决策。近年来在Molecular Medicine、Journal of Intensive Care、Journal of Biological Chemistry等期刊上发表多篇学术论文,致力于推动人工智能与临床医学的深度交叉融合。

刘芬(通讯作者)
医学博士,江西省重大公共卫生医学中心感染ICU主任,南昌大学江西医学院第一附属医院重症医学科副主任,南昌大学教授、博士生导师;兼任江西省医学会重症医学分会主任委员。
主要研究方向:脓毒症诱发多器官功能障碍的病理生理机制与干预靶点研究。近年来在Inflammation Research、Journal of Inflammation Research、Life Sciences、International Immunopharmacology、Shock、Experimental Lung Research等期刊上发表多篇学术论文。主持国家自然科学基金5项。

白松杰(通讯作者)
医学博士,毕业于浙江大学医学院,现就职于南昌大学江西医学院第一附属医院。
主要研究方向:脓毒症的基础与临床转化研究;近年来在Cell Reports、Journal of Hazardous Materials、Journal of Intensive Care等期刊上发表学术论文十余篇;主持国家自然科学基金1项、江西省自然科学基金1项、厅局级课题2项;担任《中华创伤杂志》青年学术委员。
引用格式:
Huang M, Yang X, Li C, Chen H, Pan Y, Chen L, et al. Sepsis-induced PICS: immunometabolic mechanisms, emerging biomarkers, and precision management. TransMed. 2026:100009. doi: https://doi.org/10.1016/j.tmed.2026.100009.
文章链接:
https://www.sciencedirect.com/science/article/pii/S3117397726000097

期刊信息
TransMed (ISSN: 3117-3977) 是由KeAi出版社(科学出版社与Elsevier战略合作平台)联合数百位华人医学科学家共同创办的本土转化医学学术期刊。期刊以Science Translational Medicine、Nature Biomedical Engineering、eBioMedicine等国际顶尖医学期刊为标杆,致力于打造连接基础研究—临床应用—产业转化的高端学术交流平台,助力全球医药领域创新成果快速传播与落地,为科研工作者提供极具影响力的学术展示窗口。TransMed计划在创刊2–3年内跻身中科院Top 1区期刊,预计影响因子IF 15+,助力高质量医学研究成果实现快速国际传播与临床转化。
