南昌大学程细高AHM | PPOD@CeCDs响应型平台精准拦截ROS炎症级联,助力椎间盘退变治疗
- 2026-04-23 16:46:01
 关注我,更新不错过
关注我,更新不错过
椎间盘退变(IVDD)是下腰痛的主要病理基础,活性氧(ROS)过度积累引发的氧化应激-炎症级联反应是其核心致病机制。现有干预手段难以实现退变微环境靶向滞留与持续ROS清除。南昌大学医学院第二附属医院程细高研究团队构建PPOD@CeCDs响应型平台,通过动态共价水凝胶实现CeCDs稳定释放,精准拦截ROS炎症级联,为IVDD治疗提供新策略。相关成果以"A Pathological Microenvironment–Responsive Catalytic Carbon Nanodots Release Platform Intercepting the ROS–Inflammation Cascade to Alleviate Intervertebral Disc Degeneration"为题发表在Advanced Healthcare Materials上。

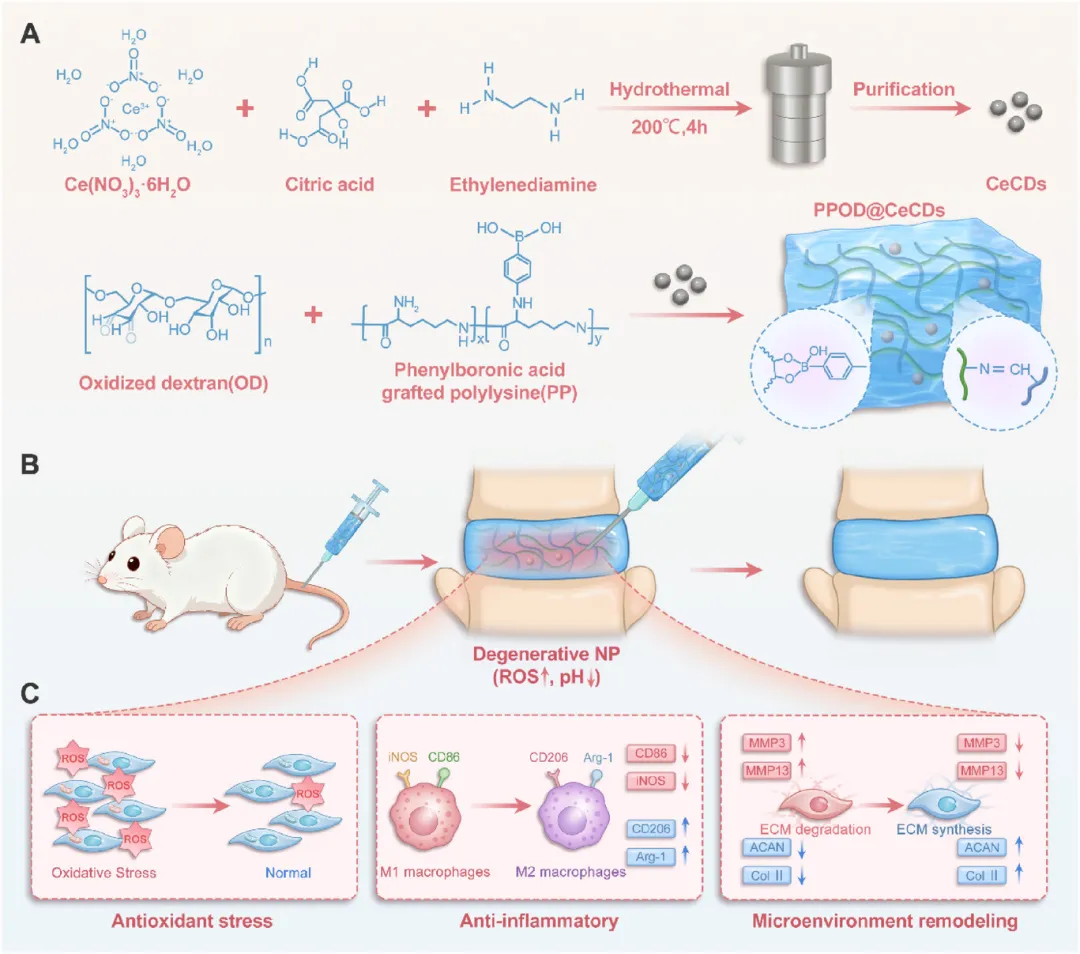
CeCDs与PPOD@CeCDs表征 水热法合成的CeCDs为类球形,分散性良好,平均粒径2.75±0.13 nm,HRTEM可见0.21 nm晶格条纹,对应石墨碳(002)晶面;Raman光谱ID/IG=1.15,兼具部分石墨化结构与表面缺陷;Zeta电位为+22.7±2.2 mV,胶体稳定性优良。
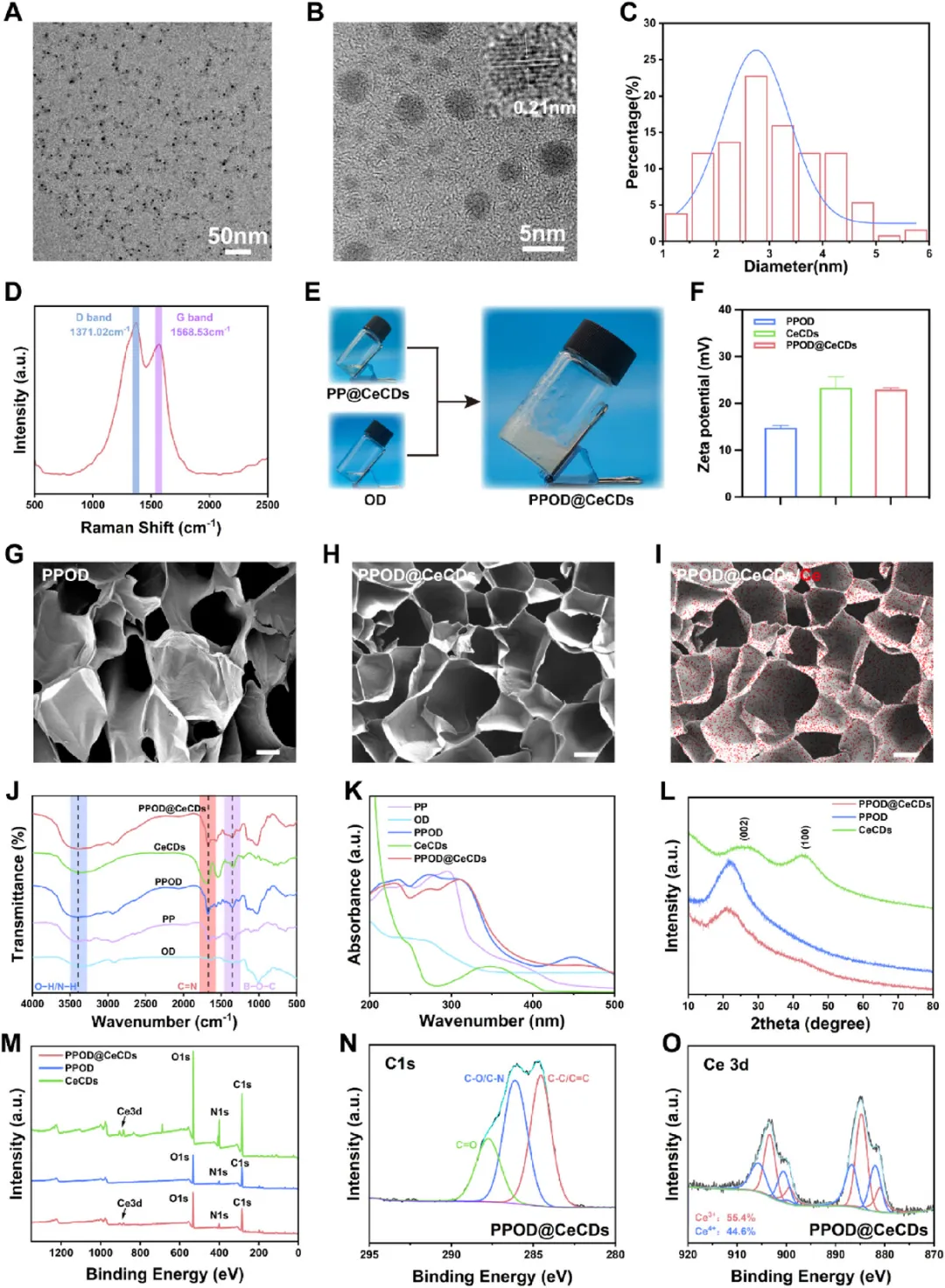
PPOD@CeCDs通过PP与OD的苯硼酸酯键和席夫碱键动态交联形成,SEM显示其具有均匀多孔三维网络,CeCDs均匀分散其中;FT-IR、XRD及XPS证实两种动态共价键共存,Ce以Ce³⁺(55.4%)和Ce⁴⁺(44.6%)混合价态稳定存在。
PPOD@CeCDs水凝胶性能 该水凝胶具有优良自修复性和可注射性,挤压后可快速原位成型;流变学测试显示,其储能模量(G′)始终高于损耗模量(G″),负载CeCDs后网络更强,且保留剪切变稀特性和抗疲劳性。
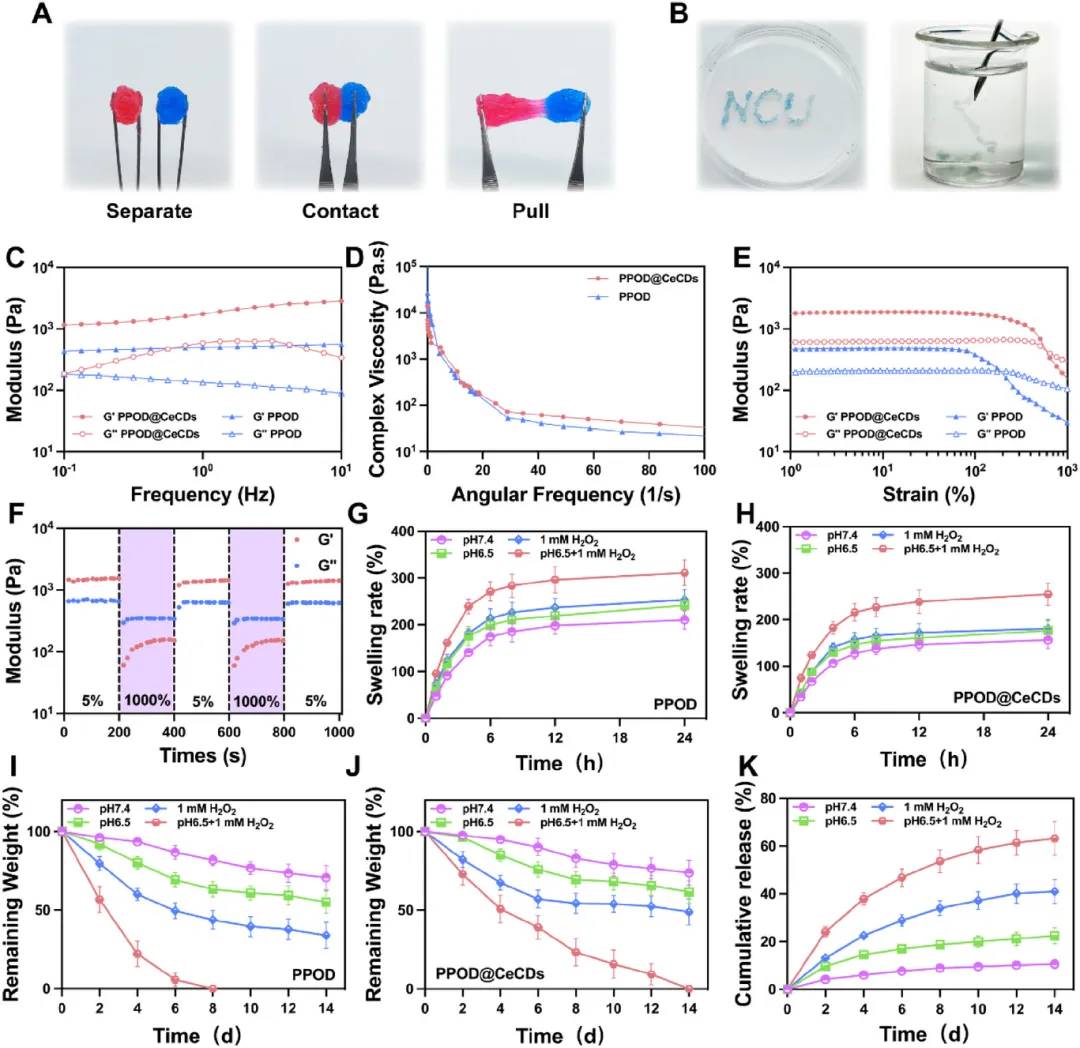
在模拟退变椎间盘环境(pH 6.5+1 mM H₂O₂)中,4h肿胀率达182.44±13.54%,8h达254.89±24.10%;7天内可实现近完全降解,CeCDs累计释放率达61.16±5.78%,而生理环境(pH 7.4)下释放量极低,实现微环境响应型控释。
生物相容性与酶促活性 CeCDs在≤100 μg/mL浓度下对NP细胞无细胞毒性,100 μg/mL时对100 μM H₂O₂诱导的细胞损伤保护效果最佳。PPOD@CeCDs与NP细胞、RAW264.7巨噬细胞共培养48h,细胞存活率维持在高水平,生物相容性优良。
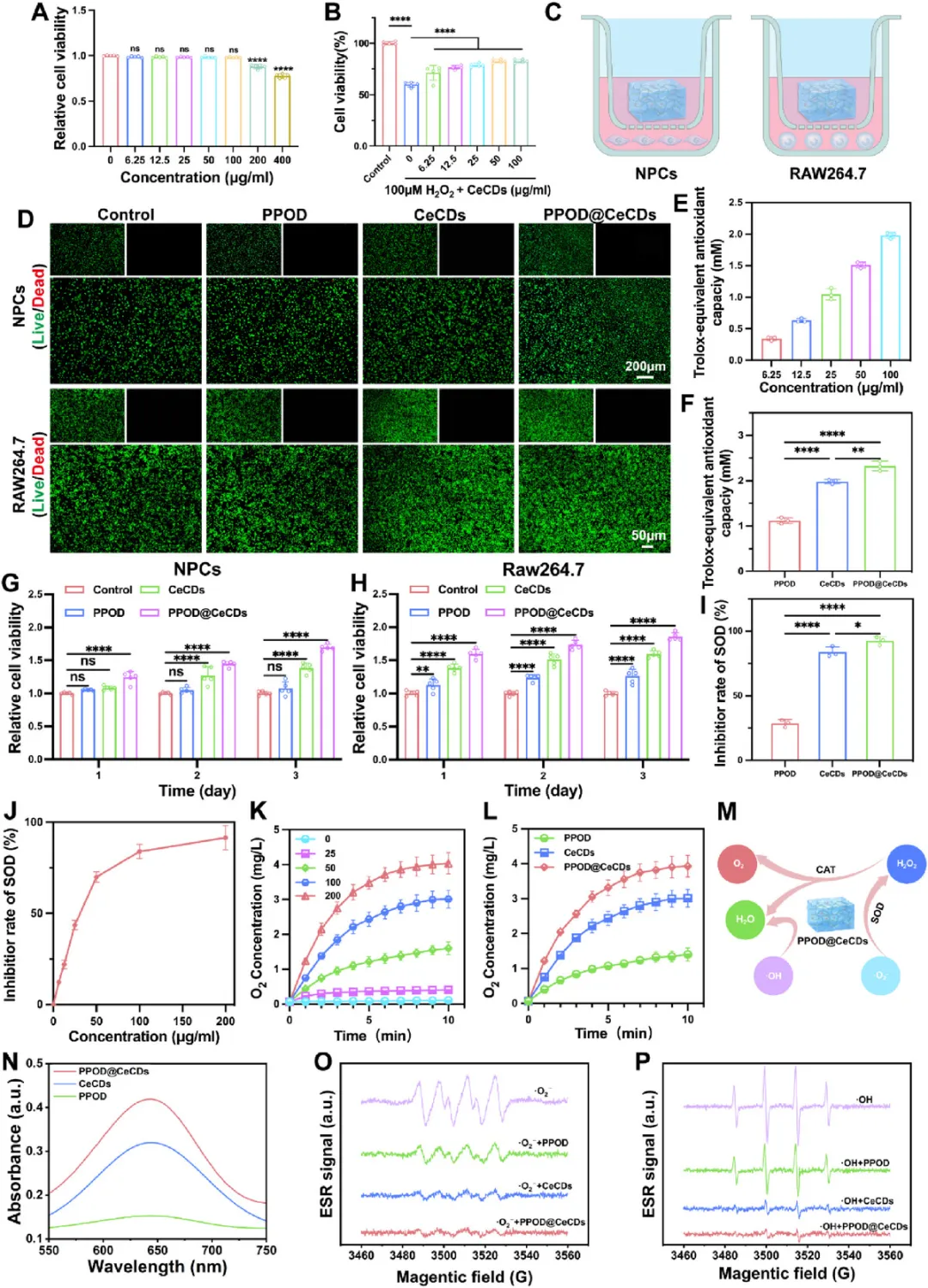
酶促活性测试显示,PPOD@CeCDs的总抗氧化能力、SOD样、CAT样、POD样活性均显著优于PPOD和CeCDs单独使用,可高效清除O₂•⁻和•OH。
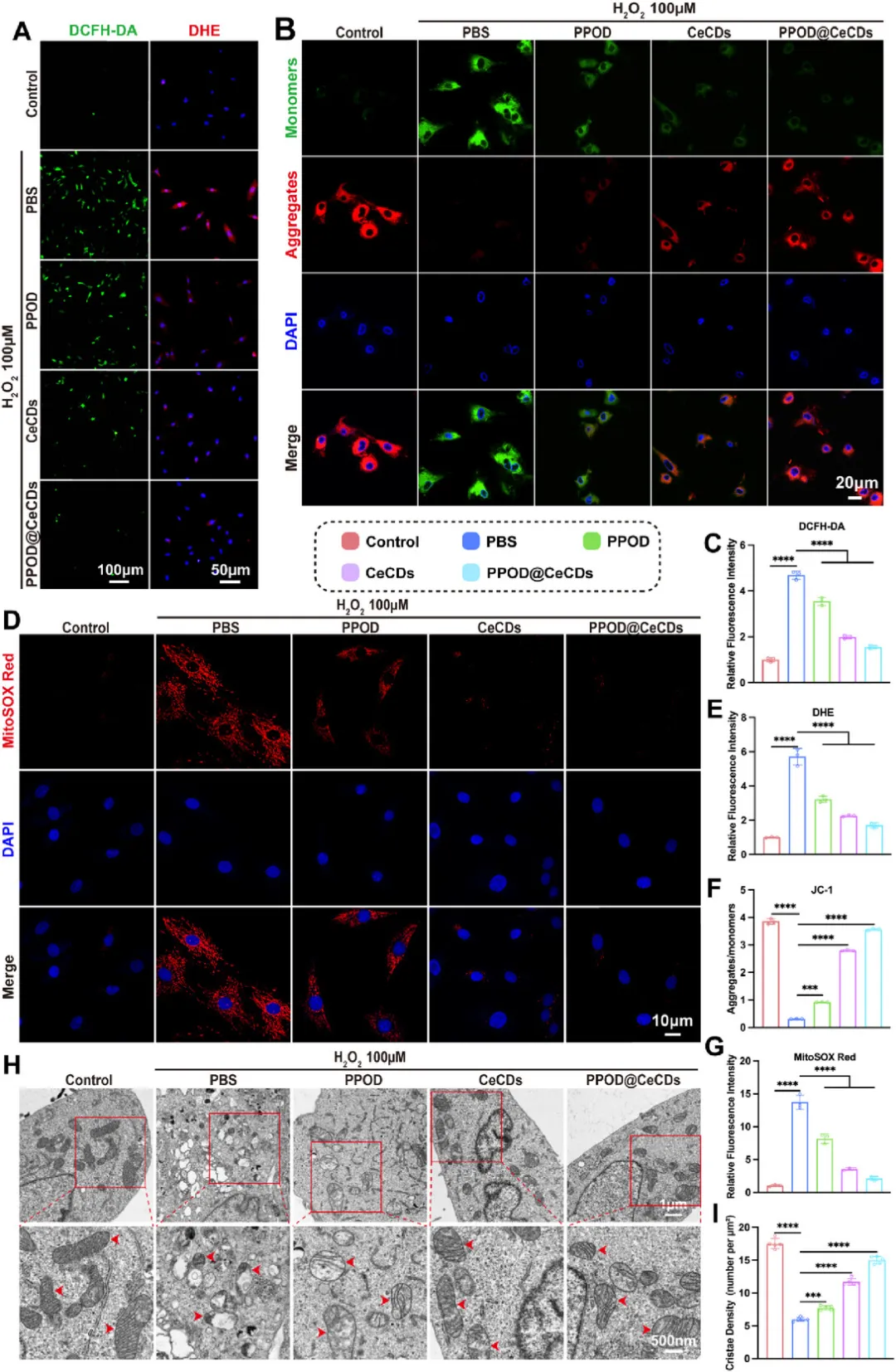
线粒体保护与ROS清除 100 μM H₂O₂诱导NP细胞ROS大量积累,PPOD@CeCDs可显著降低细胞总ROS和超氧阴离子水平;JC-1染色显示其可有效维持线粒体膜电位,抑制线粒体ROS爆发;TEM观察证实,其能最大程度保护线粒体结构完整,恢复嵴密度,切断线粒体损伤-ROS放大的正反馈循环。
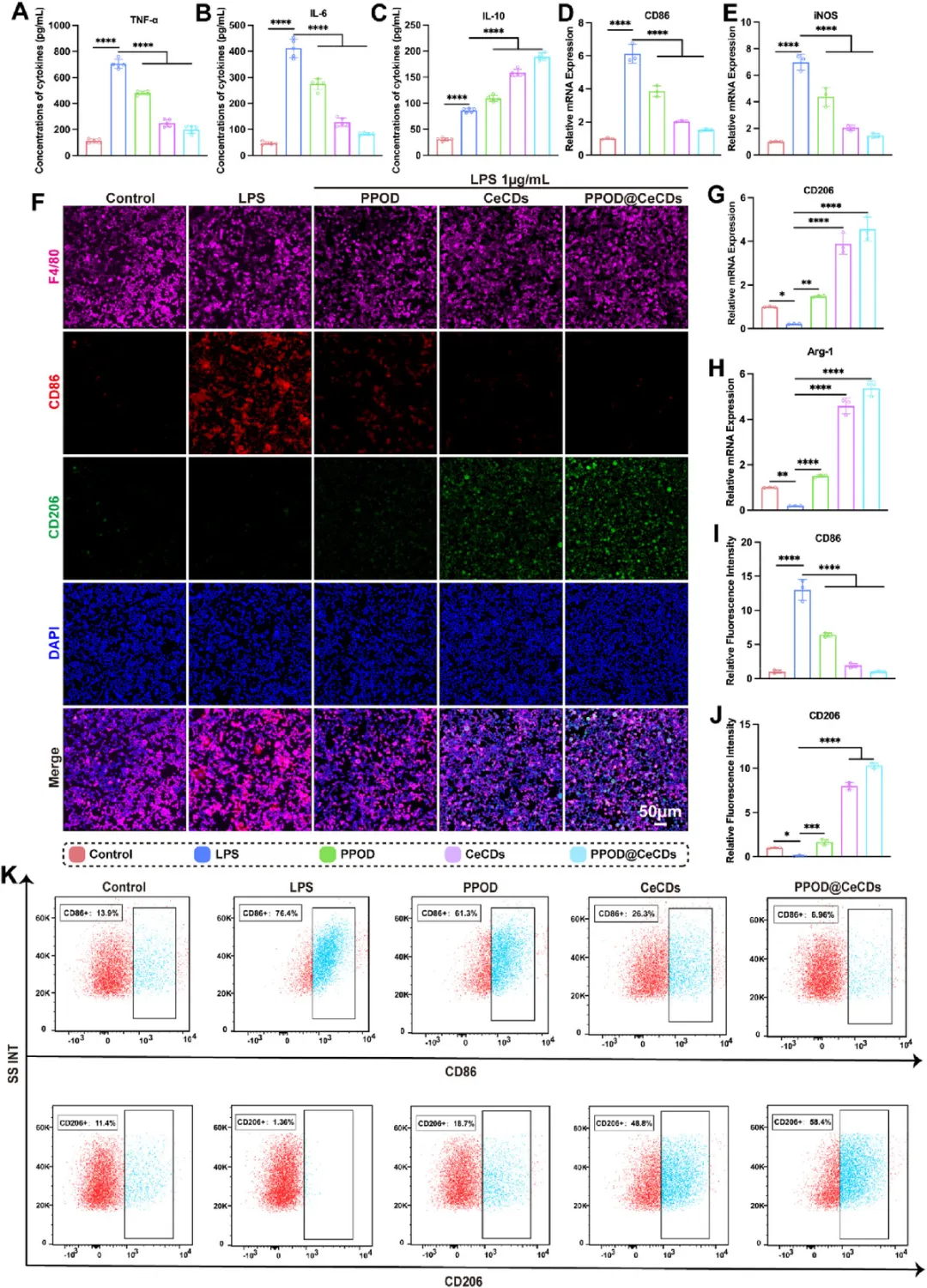
巨噬细胞极化调控 LPS(1 μg/mL)诱导RAW264.7巨噬细胞M1极化,PPOD@CeCDs可显著降低TNF-α、IL-6水平,升高IL-10水平;下调M1标志物CD86、iNOS,上调M2标志物CD206、Arg-1;流式细胞术显示,其可将CD86⁺细胞比例降至6.96%,CD206⁺细胞比例升至58.4%,高效诱导巨噬细胞向M2修复型极化。
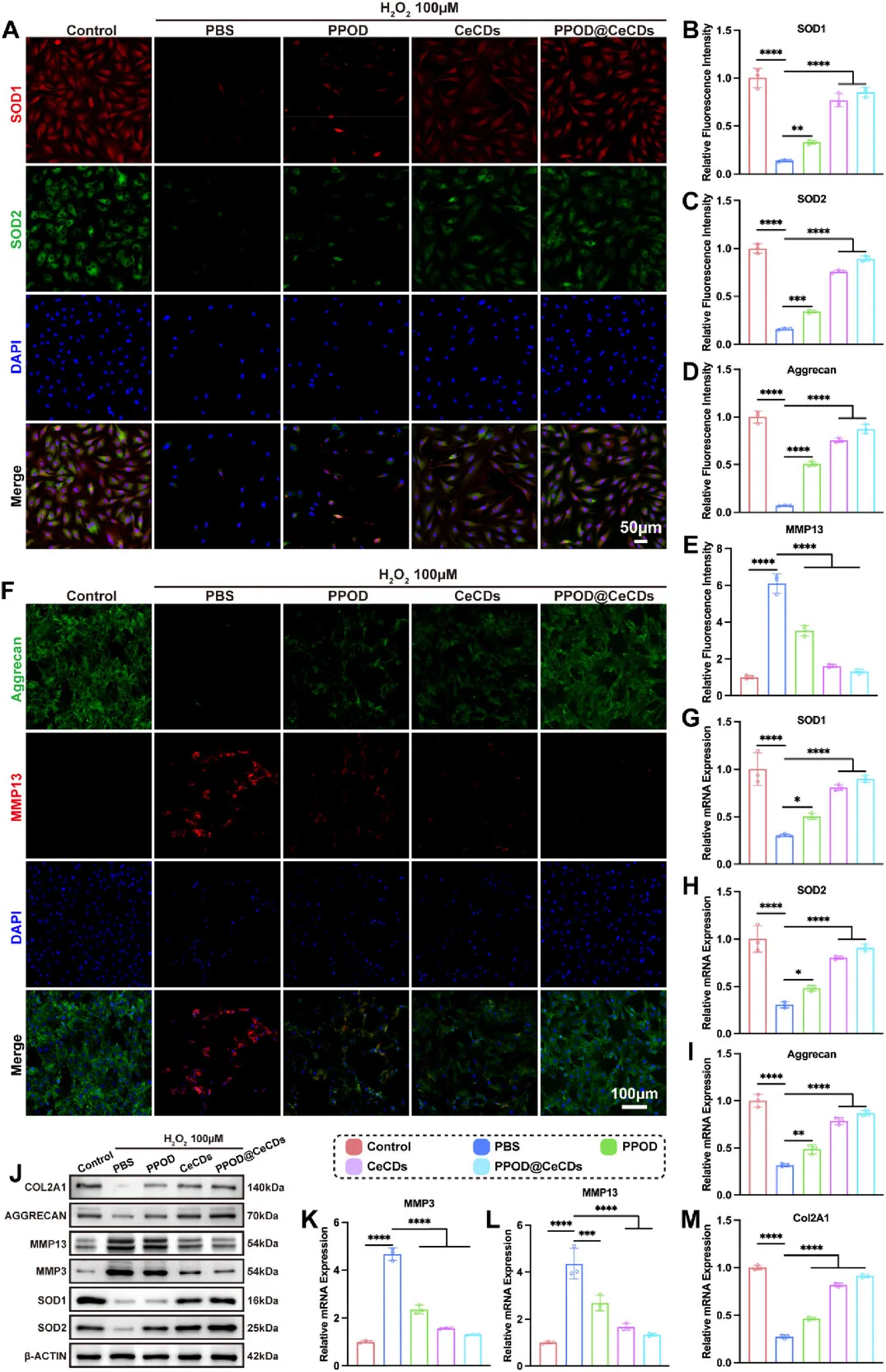
NP细胞微环境稳态重塑 H₂O₂诱导下,NP细胞SOD1、SOD2表达显著下调,Aggrecan、Col2a1表达降低,MMP3、MMP13表达升高;PPOD@CeCDs可完全恢复SOD1、SOD2表达,显著提升Aggrecan、Col2a1水平,抑制MMP3、MMP13过度表达,有效逆转基质代谢失衡,恢复细胞稳态。
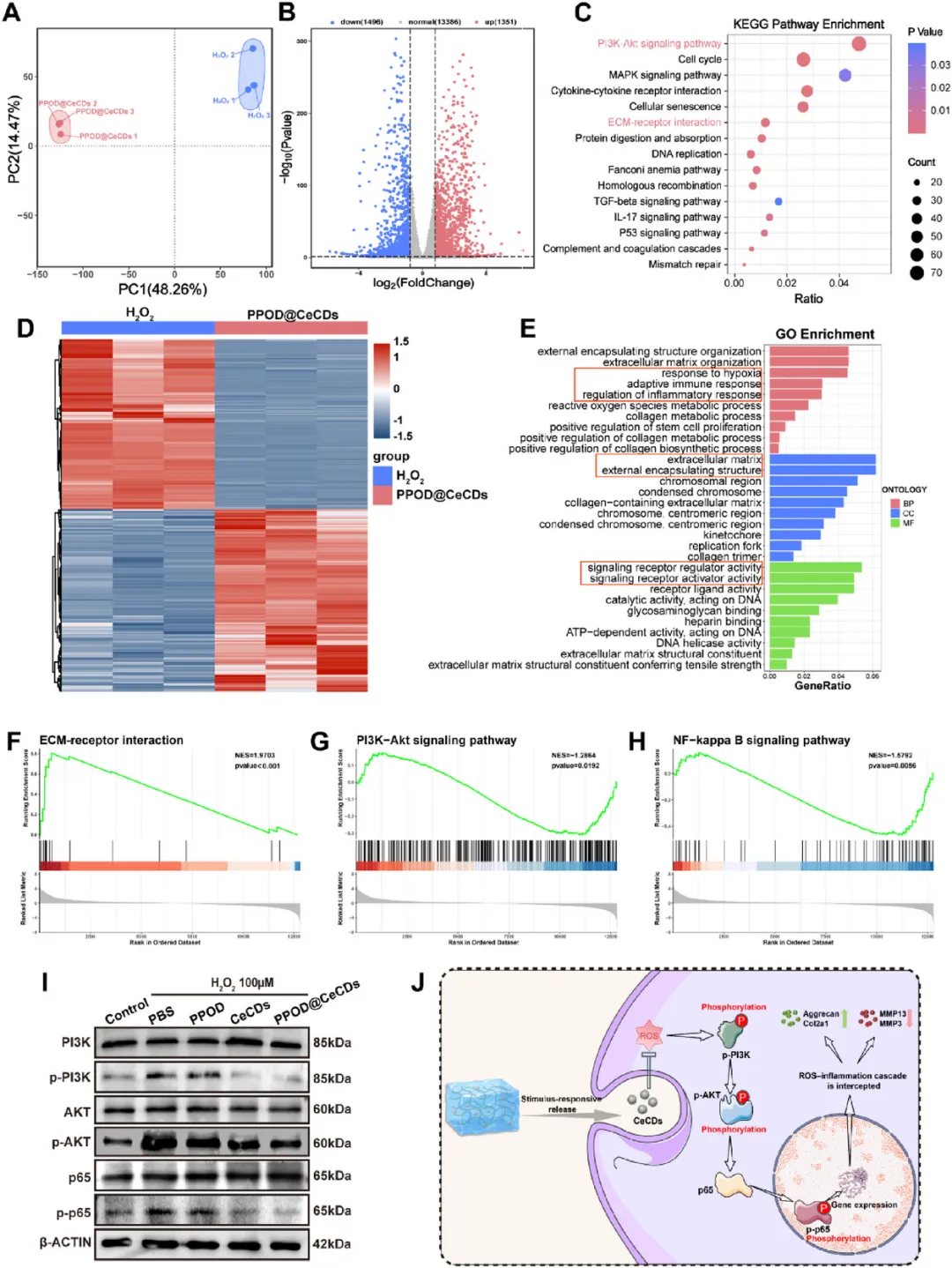
转录组分析与机制验证 PCA和差异表达分析显示,PPOD@CeCDs可驱动退变NP细胞系统性转录重编程,共鉴定出2847个差异基因;KEGG和GSEA分析表明其主要调控PI3K-Akt、NF-κB等信号通路;Western blot证实,其可显著抑制PI3K、AKT、p65的异常磷酸化,阻断ROS介导的炎症信号传导。
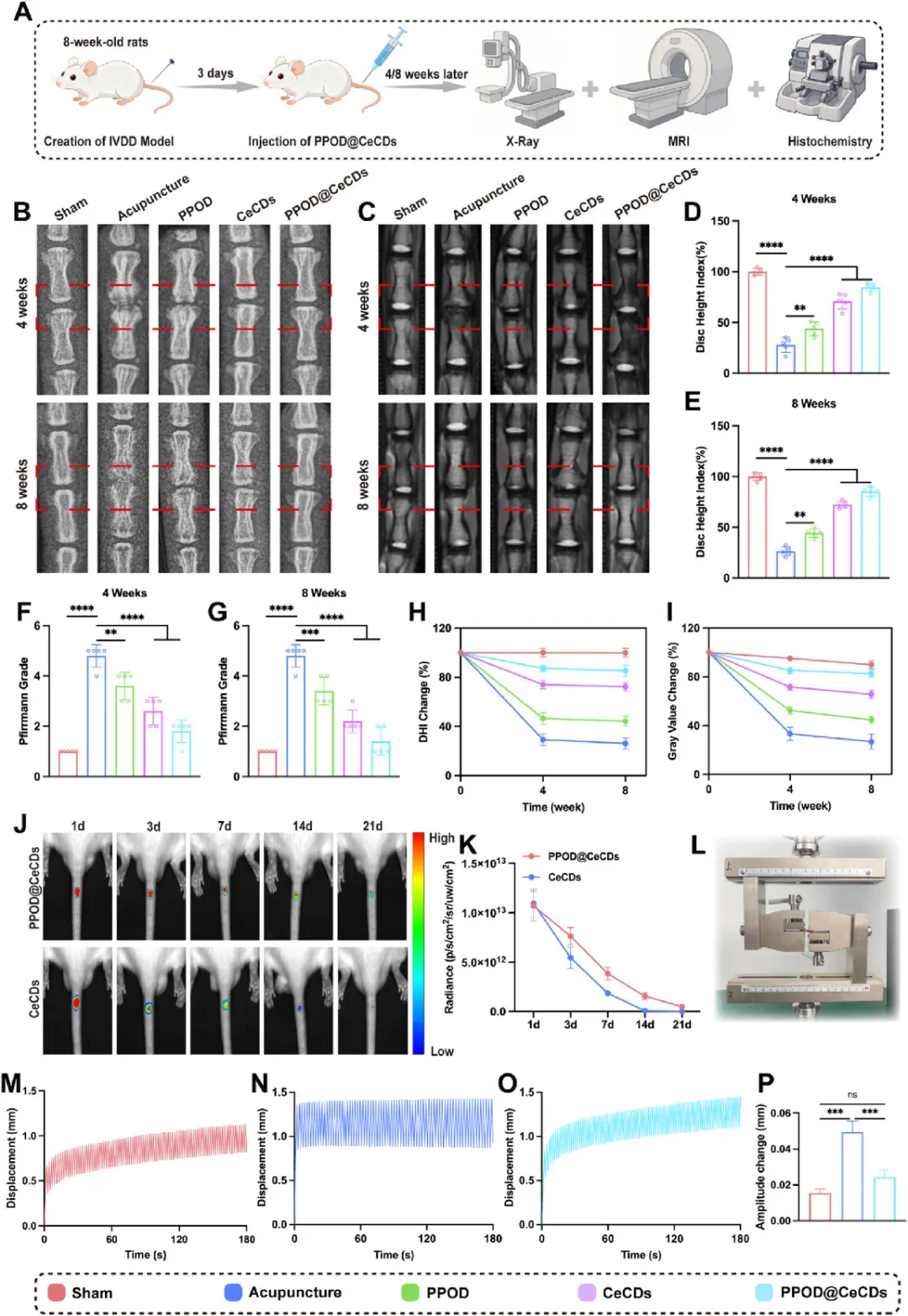
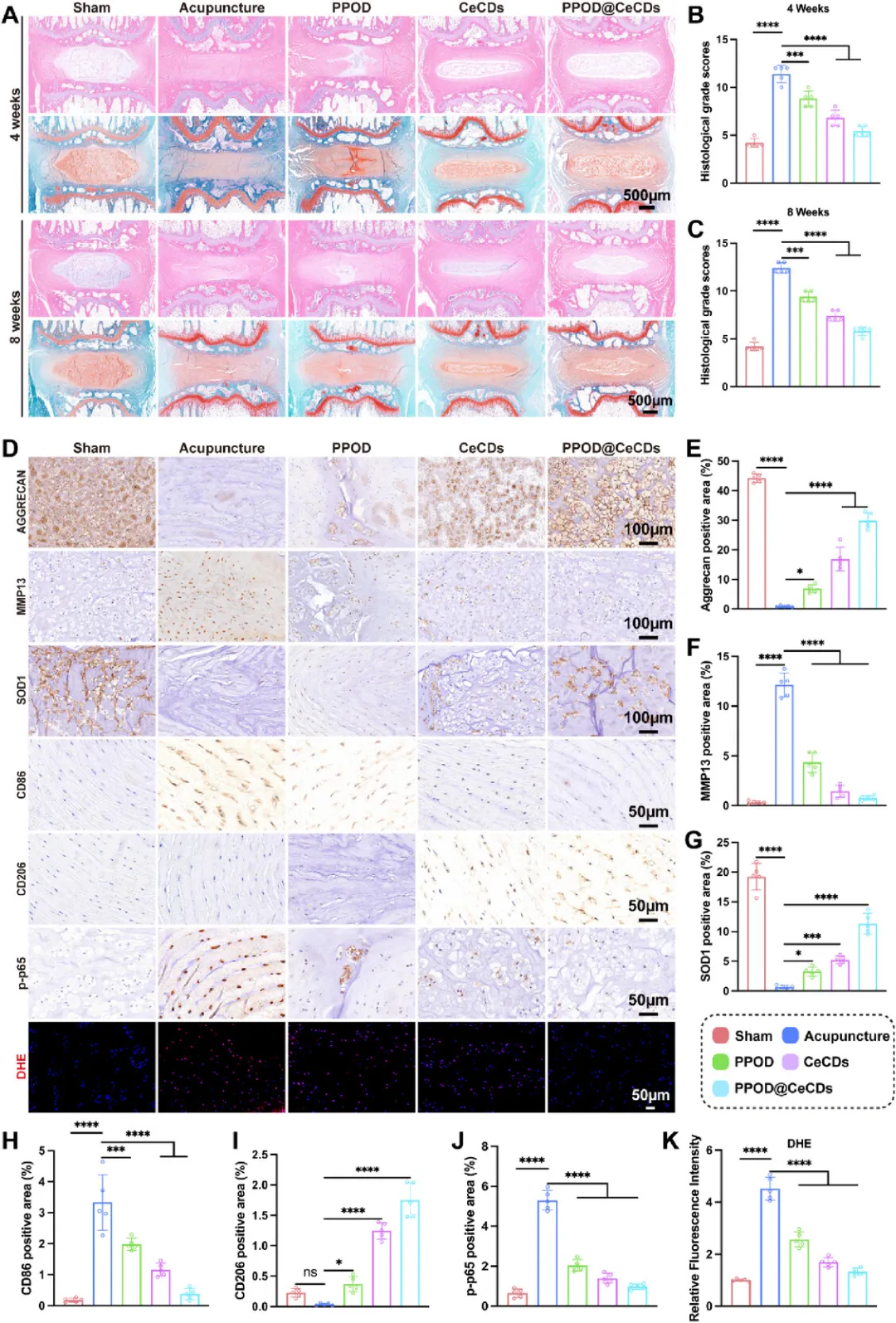
体内治疗效果 大鼠尾椎穿刺IVDD模型中,PPOD@CeCDs处理后4周和8周,椎间盘高度指数(DHI%)接近假手术组,T2-MRI信号显著高于其他治疗组;体内荧光成像显示,其在椎间盘内可稳定保留21天,而游离CeCDs 14天即基本清除;生物力学测试表明,其可有效恢复椎间盘剪切强度和抗疲劳性能,接近正常水平。
体内组织学验证 组织染色显示,PPOD@CeCDs可显著保留NP结构和蛋白聚糖含量,改善AF排列紊乱;免疫组化证实,其可提升Aggrecan、SOD1表达,降低MMP13、CD86、p-p65水平,增加CD206阳性区域,显著降低椎间盘内ROS水平;主要脏器无病理损伤,血清生化指标正常,生物安全性良好。
总 结
PPOD@CeCDs通过动态共价水凝胶实现CeCDs稳定滞留与退变微环境响应型释放,精准拦截ROS炎症级联,调控巨噬细胞极化,恢复NP细胞稳态,为椎间盘退变提供了安全有效的新型治疗策略。
相关文献
Xiang Luo, Jiajun Xie, Fengxu Yan, Zhidong Peng, Chongzhi Pan, Yiming Hu, Jian Zhang, Changxiong Cai, Jinghong Yuan, Yang Li, Xinxin Miao, Dingwen He, Xigao Cheng. A Pathological Microenvironment–Responsive Catalytic Carbon Nanodots Release Platform Intercepting the ROS–Inflammation Cascade to Alleviate Intervertebral Disc Degeneration. Advanced Healthcare Materials (2026): e71151.
https://doi.org/10.1002/adhm.71151
通讯作者简介
程细高
博士,主任医师,教授,博士生导师。现任南昌大学第二附属医院党委委员、南昌大学第二附属医院骨科主任、南昌大学医院院长、江西省骨科研究所所长、南昌大学第二附属医院骨科博/硕士学位点负责人、南昌大学第二附属医院骨科教研室主任。
主持国家自然科学基金5项,省级重大科研项目15项,累计科研资助经费近1482.08万。主持的四项成果达“国际先进、国内领先”水平,其中一项2018年度江西省科技进步二等奖,2020年度江西省医学科技一等奖,两项江西省科技进步三等奖。
上海交大马昕&复旦陈立/王旭&华东理工李玉林AFM | ASM@SCD微球通过“润滑-护软骨-抗铁死亡”协同干预治疗创伤后踝关节炎
NanoBioLab微信公众号欢迎各课题组投稿,投稿信箱:nanobiolab@126.com
 点关注不迷路,转发分享多条路
点关注不迷路,转发分享多条路
