CNS快讯 | 警惕,无辣不欢!南昌大学贾惊宇等团队合作发现辣椒素饮食诱发肠道炎症及潜在机理
- 2026-06-10 01:36:31

特发性矮小(ISS)仍是儿科面临的主要挑战,原因不明且对生长激素治疗反应不一致。2025年12月30日,南昌大学贾惊宇、程细高、刘希娟共同通讯在nature communications(IF=15.7)在线发表题为“Capsaicin diet drives gut inflammation and exosomalmiR-17-3pelevation in idiopathicshort stature”的研究论文。

本研究发现ISS患儿的血浆外泌体中hsa-miR-17-3p表达升高,该microRNA可破坏生长信号传导并抑制软骨细胞增殖。miR-17-3p的高表达会抑制ZNF148/SOS1信号通路,从而将ISS的分子功能异常与饮食暴露关联起来。
为了研究环境诱因,研究开发了一个富含辣椒素的饮食大鼠模型,重现了ISS,显示Gh/Igf-1水平正常,但血浆miR-17-3p升高。该饮食诱发轻度肠道炎症,增加肠道和血浆外泌体中的miR-17-3p。ISS儿童的粪便样本中miR-17-3p和炎症标志物也表现出类似升高,显示辣味饮食与ISS发病机制有关。最后,设计用于沉默miR-17-3p的工程外泌体结合局部生长激素疗法,恢复了生长板功能。这些发现揭示了ISS背后的由饮食驱动的外泌体轴,并为高辣椒素区域儿童提出了新的治疗策略。
矮小症定义为儿童身高低于同性别、同年龄、同种族儿童平均身高的 2 个标准差或第3 百分位以下。该病症可能对患儿的身心健康产生显著影响。重组人生长激素(rhGH)为矮小症患儿带来了治疗希望,尤其适用于生长激素缺乏症患者。然而,在排除全身性疾病、营养缺乏、精神障碍、染色体异常和生长激素缺乏症后,大多数病例最终被归类为特发性矮小症(ISS),其病因仍不明确。与生长激素缺乏相关的矮小症患儿不同,ISS患儿的生长激素水平正常。在临床治疗中,ISS患儿对rhGH治疗不敏感的情况并不少见。因此,与治疗生长激素缺乏性矮小症相比,ISS的rhGH治疗需要更高剂量,且疗效存在较大差异。rhGH治疗的有效性和安全性仍是颇具争议的话题。2016年美国儿科内分泌学会指南强调,rhGH治疗并非适用于所有ISS患者,特别是那些矮小程度较轻或无明显生理或社会心理负担的患者。鉴于这些挑战,深入了解ISS的分子机制对于开发更有效、更具靶向性的治疗方法至关重要。
近年来,研究人员通过全基因组测序鉴定出了特定的ISS易感基因,然而,这些基因的突变率仅为1%-5%,尽管有助于进一步的ISS分型,但极大地限制了其在临床治疗中的潜在应用。此外,尽管下丘脑-生长激素-胰岛素样生长因子(hypothalamic-GH-IGF)轴是调控儿童线性生长的关键通路,但大多数ISS患者在该通路中并未表现出明显异常。生长板作为下丘脑-生长激素-胰岛素样生长因子轴的终末调节器官,通过软骨内成骨负责骨骼的纵向生长,决定最终成年身高,是身高发育的“引擎”。分析ISS患儿生长板的分子病理变化有助于阐明其发病机制。然而,从ISS患儿获取生长板样本面临的伦理挑战,为病因研究和新疗法开发带来了巨大障碍。众所周知,组织和器官分泌的多种激素和生长因子通过血液输送至生长板,通过细胞间信号传导过程与其相互作用,调控生长发育。既往研究表明,ISS患者循环中生长激素、糖皮质激素和甲状腺激素的分泌无异常。但血液循环中除了激素和生长因子外,还含有大量外泌体(exosome)。作为天然纳米颗粒,外泌体可跨越生物屏障且不引发免疫原性反应,在药物递送方面具有巨大潜力。尽管外泌体有望推动对ISS的理解和治疗,但它们在ISS发病机制中的具体作用仍不明确,值得进一步研究。
本研究表明,ISS患儿的血浆来源外泌体可显著抑制软骨细胞增殖和骨形成,这一效应与hsa-miR-17-3p过表达相关。然而,ISS患者血浆外泌体中hsa-miR-17-3p升高的来源仍不清楚。研究者回顾了流行病学数据,发现ISS在辣椒素高消费的中国地区患病率更高。这些大规模观察结果表明,习惯性高辣椒素摄入与ISS发病机制之间可能存在关联,具有重要的公共卫生意义。动物实验中使用的辣椒素饮食模型,旨在反映这些高发地区的流行病学特征——高辣椒素饮食是当地日常生活的常见组成部分。
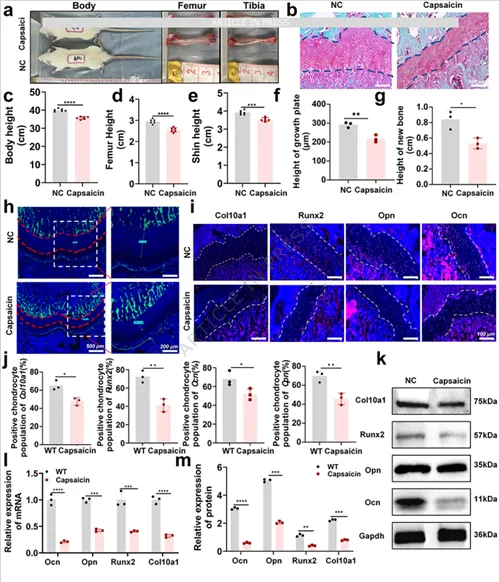
辣椒素饮食诱导的矮小表型。图自:Nature Communications
在后续实验中,研究设计了模拟这些高发地区辣椒消费水平的高辣椒素饮食,该饮食在SD大鼠(Sprague-Dawleyrats)中诱发了轻度肠道炎症。这种炎症激活了核因子-κB(NF-κB)信号通路,而该通路被确定为血浆外泌体hsa-miR-17-3p水平升高的主要驱动因素。本研究首次直接将饮食辣椒素、肠道炎症与ISS发病机制相关联,为ISS病因学提供了新的见解。此外构建了具有生长板靶向能力的工程化外泌体,用于递送小干扰RNA(siRNA),有效抵消了hsa-miR-17-3p过表达的抑制作用,同时允许精准的局部生长激素给药。这种方法显著提高了矮小症的治疗效果,代表了一种有前景的创新治疗策略。本研究结果不仅加深了对ISS分子机制的理解,还提出了一种突破性的靶向治疗途径,有望彻底改变当前的治疗方法。最后,研究结果强调,有必要进一步关注高辣椒素饮食对儿童纵向生长的影响,尤其是在ISS高危人群和接受生长激素治疗的矮小症儿童中。
来源:iNature
原文链接:
https://doi.org/10.1038/s41467-025-67883-2
往期基因编辑·CNS快讯相关推文
上海交通大学曹亚南团队通过单细胞扰动,解码2型糖尿病中核糖体应激监控新机制和靶点
从“致病”到“御病”:研究利用人群天然遗传韧性,揭示预防血癌的全新干预范式
威斯腾生物基因编辑·前沿热点服务项目
基因编辑|铁死亡|肿瘤代谢|肿瘤免疫|细胞自噬
外泌体|细胞焦亡|类器官|单细胞测序|单细胞代谢
病理空间组|脑科学|circRNA|lncRNA|相分离
线粒体|干细胞|组蛋白|肠道菌群|免疫调控
转录调控|内质网|高内涵筛药
更多科研请咨询:400-675-6758
凡来电咨询者皆可免费领取一张基因编辑敲除细胞2000元代金券

威斯腾生物成立于2007年,是一家聚焦基因功能研究与肿瘤早期诊断产品开发领域的生物高科技公司;是国家高新技术企业、科技型企业、中关村生物医药研发检测共享平台,18年专注模式动物构建、多病毒包装改造、多组学研究、基因编辑研究、基因调控、基因靶点发现验证等高质量基因功能研究CRO平台。
威斯腾生物放眼于全球生命科学基因功能研究前沿技术创新转化应用开发,立足于全国生命科学基因功能研究高品质技术服务,以肿瘤早诊、快诊以及传染病快速诊断为创新转化方向;以CRISPR/Cas9-13a基因编辑、类器官研究、外泌体研究、空间病理组学、基因及蛋白互作、CtDNA超微量捕获为核心特色技术。
威斯腾生物研发团队由华人科学家Jiang Guo教授领衔,2位海外院士、5位千人专家、2位长江学者、2位全国科技领军人才共同组建,北美研发中心设在美国·纽约州,中国研发中心分别位于北京大兴、重庆高新区和上海浦东区,在全国22个省市建立了直属运营中心。
威斯腾生物以赋能“生命科学基因功能研究”为己任,加快肿瘤早诊创新产品开发进程,推动生命科学基因功能研究行业发展,为人类健康保驾护航。
威斯腾生物·生命科学部·服务项目
细胞生物学 | 分子生物学
多组学研究 | 表观遗传学研究
机制/通路研究 | 基因功能研究
动物建模 | CRISPR/Cas9基因编辑
更多科研请咨询:400-675-6758
凡来电咨询者皆可免费领取一份高纯度质粒提取试剂盒,包邮到家!
诚聘编辑(兼职/在线办公)
脑科学研究 | 基因编辑 | 类器官 | 基因调控
肿瘤微环境 | miRNA研究 | 流式应用
脂代谢组 | 蛋白组学 | 蛋白质互作
免疫 | 干细胞
……
【详情咨询】
QQ:3636762840
电话:400-675-6758

版权声明:除原创内容及特别说明之外,推送稿件部分文字及图片均来自网络及主流媒体。如认为有侵权内容,请联系我们删除。
End
