【GUT MICROBES】南昌大学聂少平教授团队发现AKK细胞外囊泡通过“肠菌-色氨酸代谢-神经炎症”轴改善结肠炎相关认知障碍的作用与机制
炎症性肠道疾病(IBD),尤其是溃疡性结肠炎(UC),其疾病的临床表现已超出胃肠道范围。现有大量临床数据表明,UC患者是认知功能障碍和痴呆加速进展的高风险人群。肠道炎症与神经功能衰退之间的双向关联,被普遍归因于肠-脑轴的失调:肠道菌群紊乱(生态失调)可破坏肠道屏障,引发全身性炎症,并最终导致神经炎症。恢复微生物稳态是潜在治疗策略。其中,细菌胞外囊泡(bEVs)作为一种由细菌分泌的纳米级脂质双层结构,作为宿主-微生物通讯的关键媒介,能穿越血脑屏障,调节神经免疫反应。被认为是介导宿主-微生物对话的关键信使。与活菌相比,bEVs具有稳定性高、可穿越生物屏障、靶向递送且无增殖风险等独特优势。IBD相关的认知功能障碍涉及血脑屏障破坏、胶质细胞活化和色氨酸代谢紊乱等多个环节,而这些都可能被EVs所携带的活性物质调节。尽管阿克曼氏菌(A. muciniphila)及其胞外囊泡(AmEVs)在改善结肠炎方面显示出潜力,但其能否以及如何缓解结肠炎伴随的认知缺陷,此前尚未被探索。后续是否可以将AmEVs作为一种多靶点治疗工具,能否有效连接肠道微生态与神经免疫稳态,为IBD及其神经并发症提供新策略?针对以上科学问题,2026年1月6日,国家食品科学与资源重点实验室南昌大学聂少平教授团队在《GUT MICROBES》杂志(IF = 11.0)在线发表了题为“Akkermansia muciniphila-derived extracellular vesicles alleviate colitisrelated cognitive impairment via tryptophan metabolic reprogramming of the gut‒brain axis”的研究论文。
本研究针对阿克曼氏菌(A. muciniphila)产生的胞外囊泡(AmEVs)进行深入研究,确认其通过肠-脑轴的色氨酸代谢重编程减轻结肠炎相关的认知障碍。研究采用了多层次、系统性的实验流程,从体内动物模型(行为、病理、屏障、菌群、代谢)到体外细胞机制验证,结合了组学技术和分子生物学方法,全面阐述了AmEVs通过调节“肠道菌群-屏障-色氨酸代谢-神经炎症”轴来改善结肠炎相关认知障碍的作用与机制。本研究首次系统地证明,口服Akkermansia muciniphila来源的胞外囊泡(AmEVs)是一种能够同时靶向肠道和大脑的多功能纳米疗法。它通过修复屏障、抑制炎症、重塑菌群,并核心地通过双向重编程色氨酸代谢,最终修复突触功能,从而协同改善结肠炎及其相关的认知损伤,为治疗炎症性肠病相关的神经精神共病提供了全新的策略和理论依据。本研究遵循“临床问题 → 模型验证 → 机制深挖 → 细胞验证”的经典研究范式,系统地阐明了阿克曼菌胞外囊泡(AmEVs)如何通过“肠-脑轴”改善结肠炎相关认知障碍。一、 核心实验材料制备
AmEVs的分离与鉴定:
形态:透射电子显微镜(TEM)观察其典型的碟形囊泡形态。
粒径与浓度:纳米颗粒追踪分析(NTA)显示主要粒径集中在123.8 nm。
蛋白定量:使用BCA法测定蛋白浓度,分装后于-80°C保存。
来源:从Akkermansia muciniphila菌株(保藏于南昌大学食品科学与资源国家重点实验室)的厌氧培养上清液中提取。
分离方法:采用超速离心法。培养液经离心去除细菌后,上清依次通过1.2、0.45、0.22 μm滤膜过滤,最后在150,000×g、4°C条件下超速离心2小时获得沉淀,用PBS重悬。
表征:
二、 动物模型与干预
动物与分组:使用6周龄雄性C57BL/6J小鼠,随机分为三组:
实验周期:共21天,包括1周适应期。从第15天开始用DSS造模,行为学测试在第20-21天进行,第22天处死取材。
三、 行为学与认知功能评估
Y迷宫测试:评估小鼠的空间工作记忆。记录小鼠5分钟内进入各臂的次数和时间,计算自发交替率。
新物体识别测试:评估小鼠的短时识别记忆。记录小鼠探索新、旧物体的时间,计算辨别指数。设定总探索时间≥5秒为有效数据标准。
四、 样本采集与组织病理学分析
样本采集:小鼠处死后,收集血液(制备血浆)、结肠、盲肠内容物、脾脏和海马体等组织。
结肠病理学:
五、 分子与细胞生物学分析
免疫荧光/免疫组化:
肠道与血脑屏障:检测结肠和海马组织中紧密连接蛋白(Occludin, ZO-1)的表达。
神经炎症与结构:检测海马中小胶质细胞(Iba1)、星形胶质细胞(GFAP)、神经元(Map2)以及5-HT1A受体的表达与分布。
EVs体内分布:尾静脉注射PKH26标记的AmEVs,6小时后取脑、结肠、肝、脾制作冰冻切片,观察荧光分布。
基因与蛋白表达:
qRT-PCR:提取结肠和海马组织RNA,检测炎症因子(Il6, Tnfa, Il1β)、屏障蛋白(Occludin)、色氨酸代谢相关酶(Tph2)、5-HT1A受体(Htr1a)及神经营养因子(Bdnf)的mRNA水平。
ELISA/液相芯片:检测结肠、海马和血浆中的5-HT、IDO-1水平,以及结肠和海马组织中的炎症因子(如IL-1β, IL-4, IL-6, TNF-α, IFN-γ)浓度。
Western Blot:检测海马组织中突触标志物(PSD95, SYP)及紧密连接蛋白的表达。
微生物组与代谢组学:
16S rRNA测序:提取粪便微生物DNA,对16S rRNA基因V4区进行扩增子测序(Illumina NovaSeq平台),分析肠道菌群组成、多样性与差异物种。
短链脂肪酸分析:使用气相色谱法测定盲肠内容物中乙酸、丙酸、丁酸等SCFAs的含量。
非靶向代谢组学:对血浆样本进行UPLC-MS/MS分析,鉴定差异代谢物并进行KEGG通路富集分析。
蛋白质组学:
六、 体外细胞实验验证
细胞模型:使用小鼠海马神经元细胞系HT-22。
细胞分化与处理:将HT-22细胞在分化培养基中培养诱导分化后,分为:
功能检测:
5-HT产生:通过ELISA检测细胞培养上清中的5-HT水平。
机制验证:使用TLR2抑制剂(C29, 25 μM)或色氨酸羟化酶抑制剂(PCPA, 25 μM)进行共处理,探究AmEVs/Amuc_1100的作用通路。
细胞摄取:将PKH26标记的AmEVs与HT-22细胞共孵育6小时,通过荧光显微镜观察细胞对EVs的摄取。
七、 数据分析与统计
使用QIIME2进行微生物组数据分析,MetaboAnalyst 6.0进行代谢组学分析,Spectronaut进行蛋白质组学分析。
行为学轨迹使用ImageJ和R studio分析。
数据以均值±标准误表示,采用单因素方差分析(ANOVA)或Kruskal-Wallis检验进行组间比较,*p < 0.05, p < 0.01,p < 0.001,***p < 0.0001。
1. AmEV通过降低炎症反应和促进结肠粘膜修复改善DSS诱导的结肠炎嗜粘蛋白阿克曼氏菌(A. muciniphila)来源的细菌细胞外囊泡(AmEVs)的制备:通过超速离心获得AmEVs,电镜显示其呈盘状、具完整膜结构,粒径约123.8 nm,主要来源于细菌细胞质。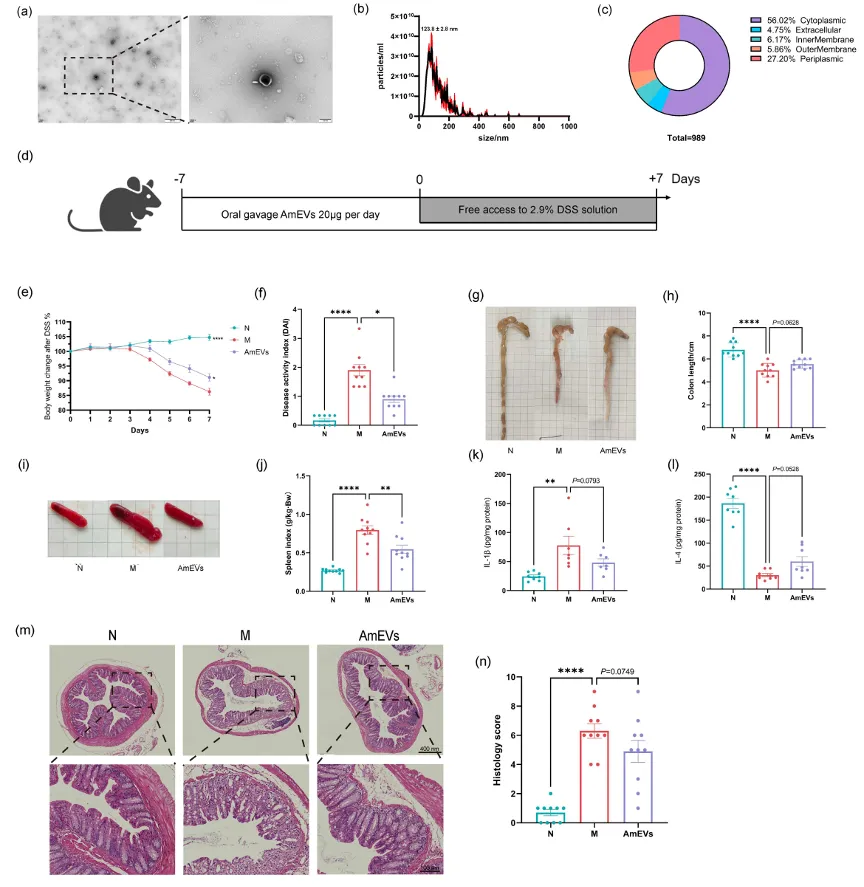 图1. AmEVs的制备及在缓解DSS诱导的结肠炎的作用在结肠炎模型中,使用AmEVs干预模型可以显著缓解疾病症状,包括改善模型体重维持、降低疾病活动指数(DAI)、减轻脾脏肿大,并在一定程度上改善结肠缩短和组织病理损伤,提示其可以促进粘膜修复。此外,AmEVs组还表现为促炎因子IL-1β水平下降、抗炎因子IL-4水平上升。总体表明,AmEVs通过增强抗炎作用和增强粘膜屏障功能有效改善结肠炎进展。
图1. AmEVs的制备及在缓解DSS诱导的结肠炎的作用在结肠炎模型中,使用AmEVs干预模型可以显著缓解疾病症状,包括改善模型体重维持、降低疾病活动指数(DAI)、减轻脾脏肿大,并在一定程度上改善结肠缩短和组织病理损伤,提示其可以促进粘膜修复。此外,AmEVs组还表现为促炎因子IL-1β水平下降、抗炎因子IL-4水平上升。总体表明,AmEVs通过增强抗炎作用和增强粘膜屏障功能有效改善结肠炎进展。2. AmEVs改善DSS诱导的认知功能障碍与神经炎症
DSS诱导的结肠炎模型小鼠出现显著的空间和识别记忆障碍:Y迷宫自发交替率从对照组的68.02%降至57.93%,新物体识别辨别指数由64.15%降至48.49%。AmEVs治疗有效逆转了这些认知缺陷,使Y迷宫表现恢复至70.32%,新物体辨别指数回升至65.9%。机制研究表明,模型小鼠海马区促炎细胞因子IL-6、TNF-α、IFN-γ和IL-1β显著升高,而AmEVs处理组小鼠组的海马区相应蛋白水平恢复至或低于对照组。尽管部分炎症基因表达未完全归零,这些结果均可以表明AmEVs能通过协同减轻神经炎症和恢复细胞因子稳态,改善了结肠炎相关的认知功能障碍,凸显其在肠-脑轴调控中的治疗潜力。3. AmEVs可以重塑肠道菌群结构并恢复短链脂肪酸(SCFAs)代谢
小鼠粪便的16S rRNA测序显示,DSS诱导的结肠炎模型组有较低的微生物多样性与丰度,而AmEVs处理组小鼠肠道微生物多样性则恢复其至接近正常水平,该组群落结构得到重塑。门水平上,拟杆菌门(Bacteroidetes)恢复,变形菌门(Proteobacteria)减少;属水平上,致病菌(如Bacteroides、Mucispirillum)减少(均与IL-6等脑部促炎因子正相关),益生菌(如Bifidobacterium,Allobaculum等)增加(与IL-6等呈负相关)。
图3. AmEVs对结肠炎小鼠肠道微生物群和SCFA的重塑
此外,AmEVs能有效恢复关键短链脂肪酸(SCFA)水平,尤其是具有肠-脑调节功能的乙酸、异丁酸和异戊酸,丙酸、丁酸等。
这些结果表明,AmEVs可通过多层次调控—抑制致病菌、富集有益菌及重建SCFA代谢—来纠正肠道生态失衡,从而可能介导其对神经炎症和认知障碍的改善作用。
4. .AmEVs修复肠-脑屏障、抑制胶质细胞活化、促进突触修复
DSS诱导的结肠炎通过破坏肠道屏障(如闭合蛋白表达下降)和引发菌群失调,导致细菌内毒素入血,诱发全身炎症、血脑屏障(BBB)损伤及神经炎症。
图4. AmEV通过屏障强化、神经胶质内稳态和突触/神经元修复恢复肠道-脑轴内稳态
AmEVs处理组能有效逆转这一肠-脑轴病理级联:结肠和海马中Occludin、ZO-1等紧密连接蛋白等关键蛋白得到恢复表达,这修复肠道与BBB完整性;同时Iba-1(小胶质细胞)与GFAP(星形胶质细胞)的3D重构结果显示,AmEVs可以抑制其细胞活化形态,恢复静息态;此外,AmEVs组的海马组织突触蛋白SYP、PSD95表达恢复,神经元骨架蛋白MAP2+神经元修复,神经营养因子BDNF mRNA表达上调。
这些结果均表明,AmEVs通过协同强化屏障功能、抑制神经胶质过度激活、修复突触与神经元结构,全面重建肠-脑轴稳态。
5.AmEVs调控色氨酸代谢、恢复5-羟色胺(5-HT)平衡并靶向海马神经元
小鼠血浆非靶向代谢组学显示,AmEVs可显著改变血浆代谢谱,主要在色氨酸代谢与胆汁酸合成通路得到显著富集。结肠与血浆中5-HT在结肠炎模型组中过度升高,AmEVs处理后恢复至正常水平;海马中5-HT在结肠炎模型中降低,AmEVs处理后显著回升结肠炎模型组中的结肠组织和血浆中(5-HT)异常升高,而海马组织中的5-HT水平下降;
图5. AmEV双向调节肠道和大脑中的色氨酸代谢并修复神经损伤
AmEVs处理组能有效逆转这一双向失调,恢复海马5-HT及其合成关键酶Tph2的表达,并抑制竞争性Trp代谢酶Ido-1的上调,二者呈显著负相关。
DIA蛋白组学显示AmEVs携带色氨酸代谢相关蛋白;PKH26示踪显示AmEVs在6h内富集于海马,并被HT-22神经元细胞直接摄取。体外HT-22神经元细胞实验表明,AmEVs携带的关键蛋白,Amuc_1100蛋白可逆转LPS诱导的5-HT下降,且该效应部分依赖TLR2(toll样信号受体)通路(TLR2抑制剂C29引起的通路影响较低,另外一个色氨酸羟化酶通路抑制剂的抑制效果较好),这也可能提示AmEVs中的关键蛋白Amuc_1100蛋白可能参与更多的信号通路影响。图6. AmEV双向调节肠道和大脑中的色氨酸代谢并修复神经损伤整体实验表明AmEVs通过递送功能蛋白(如Amuc_1100)进入海马神经元,重塑局部5-HT代谢,恢复5-HT1A受体表达,进而启动BDNF-PSD95突触重塑级联反应。
该研究系统阐明了嗜粘蛋白阿克曼氏菌来源的细菌细胞外囊泡(AmEVs)通过调控肠-脑轴,同时缓解结肠炎及其相关认知障碍的机制。(1)双重治疗效果:AmEVs能显著减轻DSS诱导的小鼠结肠炎症状(如体重下降、疾病活动指数升高),并有效逆转结肠炎引发的认知缺陷(空间和识别记忆缺陷)。(2)肠-脑屏障修复:AmEVs通过上调肠道和血脑屏障(BBB)的关键紧密连接蛋白(如Occludin, ZO-1)表达,修复受损的物理屏障,阻止炎症因子和细菌毒素入脑。(3)神经炎症抑制与神经修复:AmEVs通过抑制海马区小胶质细胞和星形胶质细胞的过度活化,降低促炎细胞因子表达水平,促进突触蛋白(SYP, PSD95)、神经元骨架蛋白(Map2)及神经营养因子(BDNF)的表达,修复神经元和突触功能。(4)色氨酸代谢重编程:这是核心机制。AmEVs对色氨酸代谢进行双向精准调控——在肠道抑制过量的5-HT产生,在海马则恢复5-HT水平及其受体(5-HT1A)表达。研究鉴定出AmEVs中的关键蛋白Amuc_1100,它能直接被神经元摄取,并通过TLR2信号通路促进5-HT合成。(5)肠道菌群与代谢物重塑:AmEVs干预可纠正菌群失调(如富集双歧杆菌、抑制致病菌),并恢复短链脂肪酸(SCFAs)等有益代谢物的水平,为整体抗炎和神经保护效应提供支持。(1)功能成分的贡献度未量化:尽管发现了Amuc_1100的关键作用,但AmEVs中其他蛋白质、核酸或脂质成分对整体疗效的具体贡献尚未明确。TLR2抑制剂仅能部分阻断AmEVs效应,提示存在其他并行机制。(2)因果关系证据链可加强:菌群变化与神经保护之间的因果关系尚未完全确立。例如,通过粪菌移植实验验证“AmEVs修饰后的菌群”是否足以产生神经保护作用,将更具说服力。文中多数机制关联基于相关性分析(如特定菌属与炎性因子的相关),需更多功能获得/丧失实验来证实。(3)神经通路未被探索:研究未考察迷走神经等直接神经通路是否参与了AmEVs的肠脑信号传导。切断迷走神经可能有助于区分神经与体液通路各自的贡献。(4)模型与性别局限性:研究仅使用了雄性小鼠模型,而IBD和认知障碍均存在性别差异,结果的外推需谨慎。(5)临床转化距离:所有实验均在临床前小鼠模型中进行,AmEVs在人体内的安全性、有效性、最佳剂量及递送方案均有待未来研究(1)概念创新:首次将AmEVs定义为一种能够同时治疗肠道炎症和认知共病的多功能纳米治疗剂,为“肠-脑轴”干预提供了新范式。(2)机制深化:超越了传统的抗炎解释,首次系统阐明了AmEVs通过“色氨酸代谢重编程”这一精确的分子开关来协调肠脑通讯。特别是发现了5-HT在肠与脑中截然相反的双向调节模式,并明确了其下游的BDNF-突触可塑性通路。(3)技术视角创新:揭示了益生菌衍生的EVs具有天然脑靶向递送能力,能直接将功能性细菌蛋白(如Amuc_1100)运送到海马神经元,这为开发基于细菌EVs的脑部疾病靶向给药系统提供了概念验证。(4)转化价值:AmEVs作为“后生元”,相比活菌具有更好的安全性、稳定性和可控性,临床转化潜力更大。Driving innovation for better life!