Gut Microbes | 南昌大学聂少平/谢俊华团队揭示Akk菌来源胞外囊泡缓解肠炎相关认知障碍新机制
- 2026-05-21 06:33:09
细菌胞外囊泡(bEVs)是一类由细菌分泌的纳米级膜性囊泡,在机体健康与疾病中发挥重要调控作用。其中,来自益生菌的EVs正逐渐成为极具潜力的“后生元”治疗手段 。
近日,南昌大学食品科学与资源挖掘全国重点实验室聂少平/谢俊华团队在国际期刊 Gut Microbes发表了题为“Akkermansia muciniphila-derived extracellular vesicles alleviate colitis-related cognitive impairment via tryptophan metabolic reprogramming of the gut-brain axis”最新研究论文,硕士生陈鑫洋(现为赫尔辛基大学在读博士生)为该论文第一作者,通过炎症细胞和动物模型,揭示了嗜黏蛋白阿克曼氏菌衍生的胞外囊泡(AmEVs)缓解溃疡性结肠炎及其相关的认知功能损伤的作用及其分子机制。

在分子机制层面,AmEVs展现了精准的“跨器官”调节能力,其首要任务是全方位重塑中枢神经系统的稳态环境。研究证明,AmEVs能显著上调肠道及血脑屏障中的紧密连接蛋白,有效封堵炎症因子由外周向中枢渗透的路径 。同时,AmEVs展现出强大的免疫调节力,能够逆转由结肠炎触发的海马体小胶质细胞和星形胶质细胞的异常活化,诱导其由促炎表型回归静息态 。这种环境的改善为神经修复创造了前提,通过上调神经营养因子BDNF的表达,进一步带动了突触相关蛋白PSD95与SYP的水平恢复,从物理屏障到免疫环境全面守护神经元 。
在稳定的中枢环境下,AmEVs对色氨酸代谢平衡的系统性重构成为修复认知的核心 。在肠炎状态下,色氨酸代谢往往发生“厚此薄彼”的紊乱:肠道内5-HT过度合成加剧炎症,而在脑中因限速酶Tph2表达下调导致5-HT极度匮乏,且活化的小胶质细胞会诱导Ido-1水平升高,强行将色氨酸拉向Kyn通路,挤压了5-HT的合成空间 。AmEVs通过纠正这种偏离实现了“拨乱反正”:一方面抑制肠道内过量的5-HT产生,另一方面恢复结肠炎所导致海马内的5-HT浓度降低。
作者通过诱导分化后的HT-22血清素能神经模型进行验证,发现AmEVs和关键蛋白Amuc_1100能够上调5-HT的产生,这可能是通过TLR2受体激活所实现的。值得注意的是,尽管TLR2抑制能部分阻断该效应,但并未完全消除AmEVs的治疗作用,提示其可能还依赖其他囊泡成分或并行信号通路共同维持海马内5-HT能神经元投射纤维的5-HT产生水平及5-HT1A受体表达。此外,AmEVs还提升了双歧杆菌等益生菌丰度,并促进了具有神经保护潜力的乙酸等短链脂肪酸(SCFAs)恢复,从底层巩固了肠脑轴稳态。
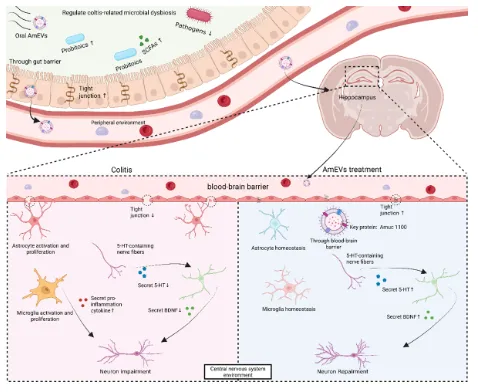
图1. 口服 AmEVs 经由肠-脑轴治疗结肠炎及其相关认知障碍的机制假说
综上所述,AmEVs可能是一种多功能治疗剂,能够通过时空调控肠脑轴同时缓解结肠炎及其认知障碍。其双向疗效由三种协同机制介导:外周强化肠道屏障完整性、中枢向海马神经元输送细菌来源代谢酶,以及全身性抑制神经炎症级联反应。该研究不仅揭示了AmEVs作为天然纳米药物在肠-脑轴通讯中的关键价值,同时也重新定义了益生菌来源的EVs作为具有固有脑靶向特异性的天然纳米治疗剂,为对抗IBD相关神经精神共病提供了新策略。
参考文献:
Akkermansia muciniphila-derived extracellular vesicles alleviate colitis-related cognitive impairment via tryptophan metabolic reprogramming of the gut-brain axis. Gut Microbes. 2026 Jan 18(1): 2611546. https://doi.org/10.1080/19490976.2025.2611546


