Nature子刊|南昌大学一附院乳酸化介导 H3K18la 修饰驱动 CXCL1 转录,揭示胰腺癌中性粒细胞浸润与免疫逃逸全新机制
- 2026-05-21 06:31:24

胰腺癌素有“癌王”之称,免疫治疗长期无效,核心困境在于极度免疫抑制的肿瘤微环境。中性粒细胞大量浸润、CD8+杀伤性T细胞匮乏,是胰腺癌进展快、易耐药、预后差的关键原因。
南昌大学第一附属医院张呈生教授团队发表于Nature Communications的重磅研究,运用大数据分析、质谱流式、CUT&Tag、分子对接、动物模型等核心技术,首次揭示一条全新代谢-表观-免疫调控轴:肿瘤糖酵解产生乳酸,经PCAF催化组蛋白H3K18乳酸化(H3K18la),直接转录激活CXCL1,招募大量促癌中性粒细胞,最终诱发免疫逃逸。
该研究不仅破解胰腺癌免疫抑制底层逻辑,更证实PCAF抑制剂联合抗PD-1可强效激活抗肿瘤免疫,为冷肿瘤胰腺癌带来颠覆性联合治疗策略!
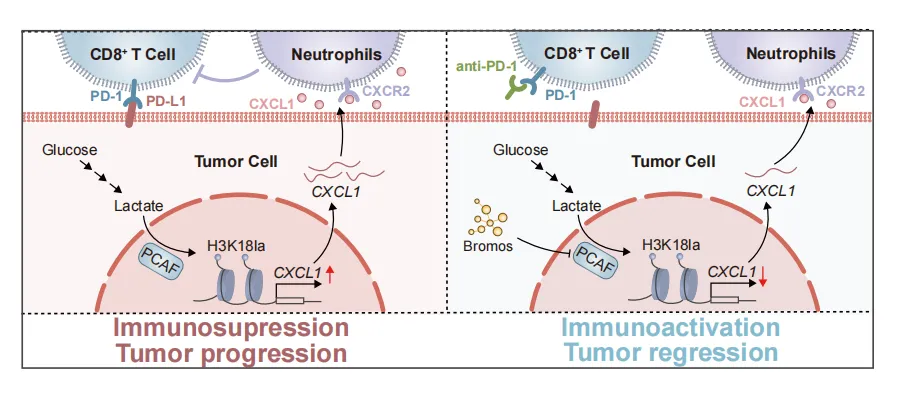
标题:Histone lactylation increases CXCL1 expression for neutrophil infiltration and immune escape in pancreatic cancer.
译名:组蛋白乳酸化通过上调 CXCL1 表达促进胰腺癌中性粒细胞浸润与免疫逃逸
期刊:Nature communications
影响因子:IF=15.7
发表时间:2026.2.9
通讯作者: Chengsheng Zhang
集思从集思专业从事大数据分析、质谱流式、CUT&Tag、分子对接、动物模型,生信分析和课题设计服务,需要的老师长按下面二维码联系。

研究思路
团队先通过TCGA、CPTAC泛癌数据锁定高糖酵解-高中性粒细胞-差预后的关联; 再利用糖酵解抑制剂、LDH敲低、中性粒细胞敲除等手段,证实糖酵解通过中性粒细胞介导免疫抑制; 随后经RNA-seq、CUT&Tag、ChIP-qPCR定位CXCL1为关键趋化因子,明确H3K18la直接激活其转录; 通过分子对接、体外乳酸化实验、抑制剂筛选鉴定PCAF为H3K18la核心乳酸转移酶; 最终在皮下与原位胰腺癌模型中,验证PCAF抑制剂+抗PD-1的协同治疗效果,完整搭建乳酸-PCAF-H3K18la-CXCL1-中性粒细胞调控网络。
文章主要内容
1:高糖酵解招募中性粒细胞,加速胰腺癌进展
生物信息学与动物实验证实:
胰腺癌糖酵解活性越高,中性粒细胞浸润越多、CD8+T细胞越少,患者生存期越短
抑制糖酵解(2DG、LDH敲低)可显著减少中性粒细胞、增加CD8+T细胞,抑制肿瘤生长
清除中性粒细胞可逆转糖酵解介导的免疫抑制,恢复CD8+T细胞杀伤功能直接证明糖酵解-中性粒细胞轴是胰腺癌免疫逃逸核心推手。
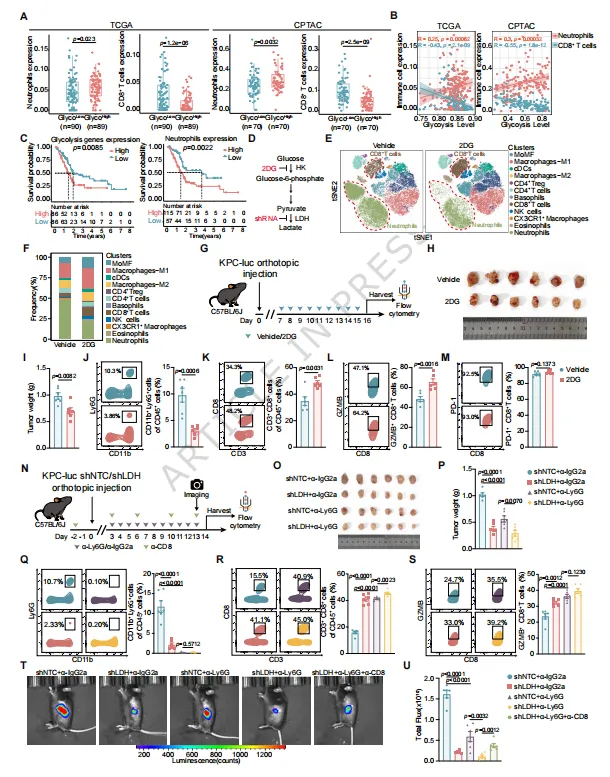
图 1 糖酵解招募中性粒细胞,促进胰腺癌进展
2:CXCL1是糖酵解招募中性粒细胞的关键趋化因子
RNA-seq筛选与功能实验显示:
CXCL1是糖酵解调控最显著的趋化因子,在胰腺癌中高表达且预示不良预后
抑制糖酵解可显著降低CXCL1的mRNA与蛋白水平
回补CXCL1能恢复中性粒细胞浸润,抵消糖酵解抑制的抑癌效果
CXCL1通过CXCR1/2介导中性粒细胞趋化,是肿瘤的“中性粒细胞磁铁”。
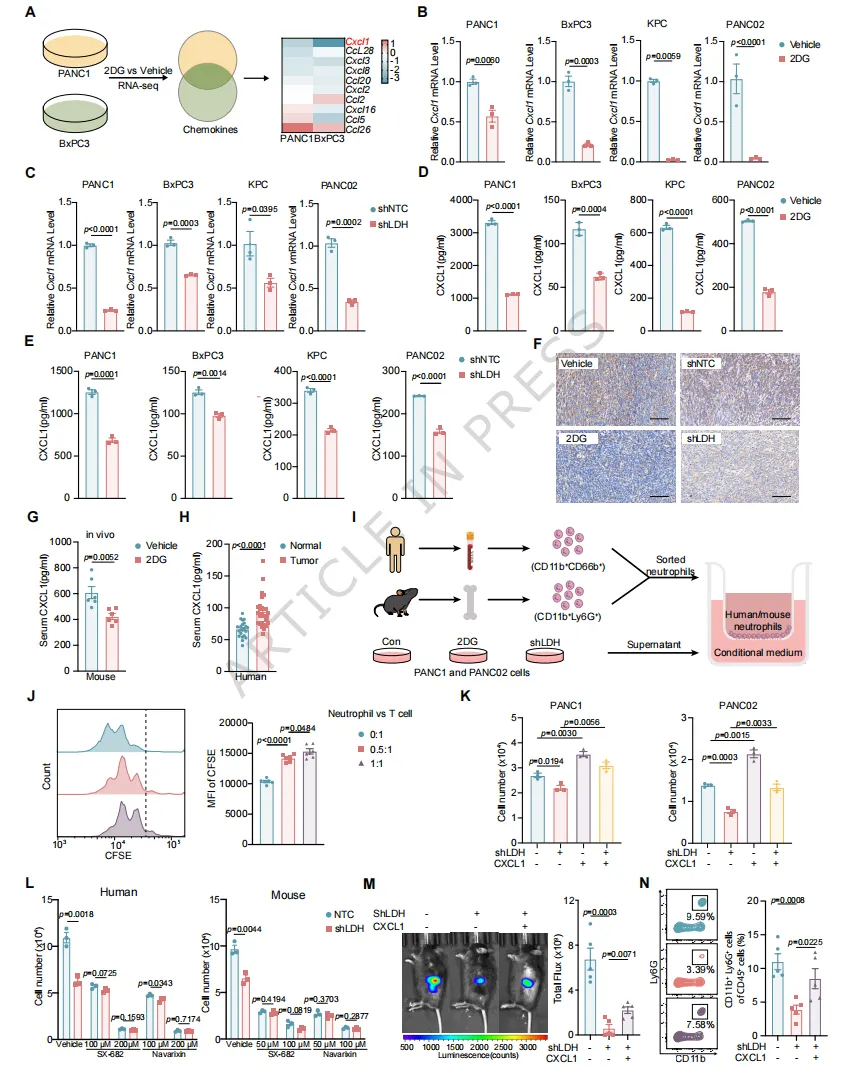
图 2 糖酵解通过上调 CXCL1 表达增强中性粒细胞浸润
3:乳酸诱导H3K18la,直接转录激活CXCL1
机制核心发现:
糖酵解产物乳酸是组蛋白乳酸化的直接供体,显著提升H3K18la水平
H3K18la直接结合CXCL1启动子,强力驱动其转录
2DG、LDH敲低降低H3K18la与CXCL1,补充乳酸可完全恢复
临床样本中H3K18la与CXCL1表达显著正相关首次建立乳酸→H3K18la→CXCL1的表观转录调控通路。
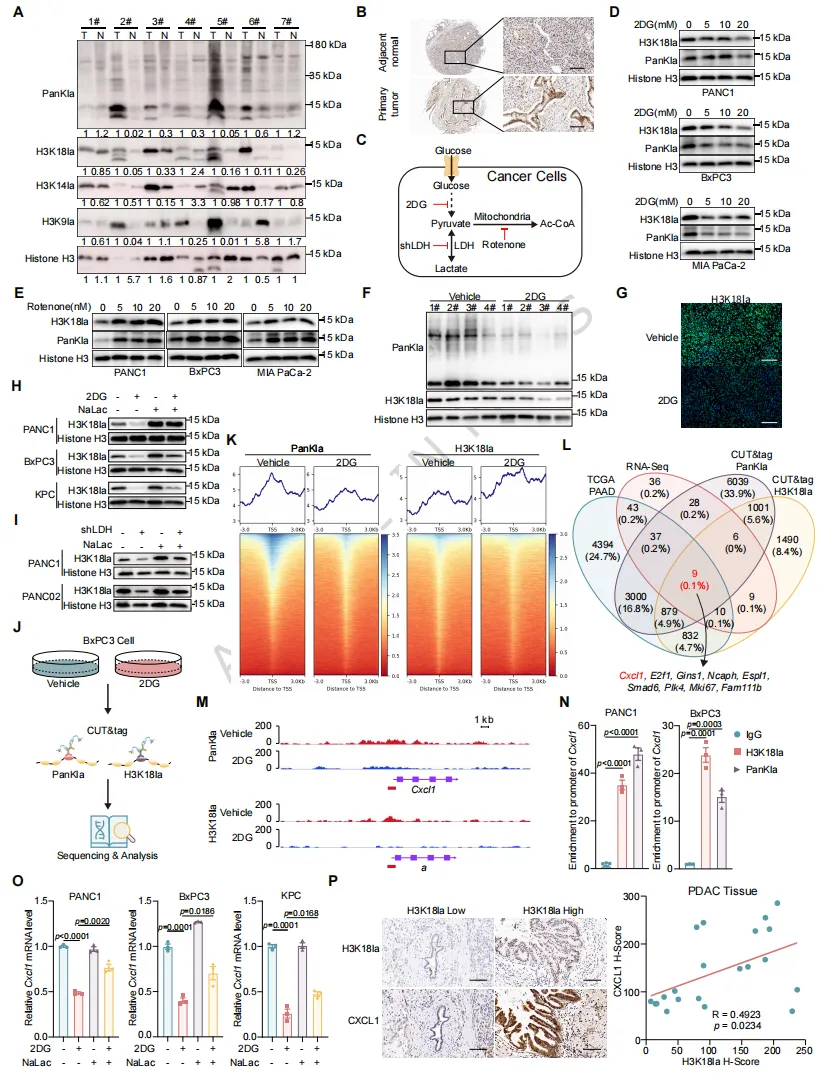
图 3 糖酵解来源的乳酸增强 H3K18la 修饰并促进 CXCL1 表达
4:PCAF是催化H3K18la的关键乳酸转移酶
突破性靶点发现:
筛选证实PCAF抑制剂(Bromosporine)可显著降低H3K18la水平
分子对接显示PCAF可结合乳酰-CoA,体外实验直接证实PCAF催化H3K18乳酸化
敲低或抑制PCAF,同步降低H3K18la、CXCL1与中性粒细胞浸润
临床样本中PCAF与H3K18la表达正相关明确PCAF为胰腺癌H3K18la的核心“书写酶”,成为全新可药用靶点。
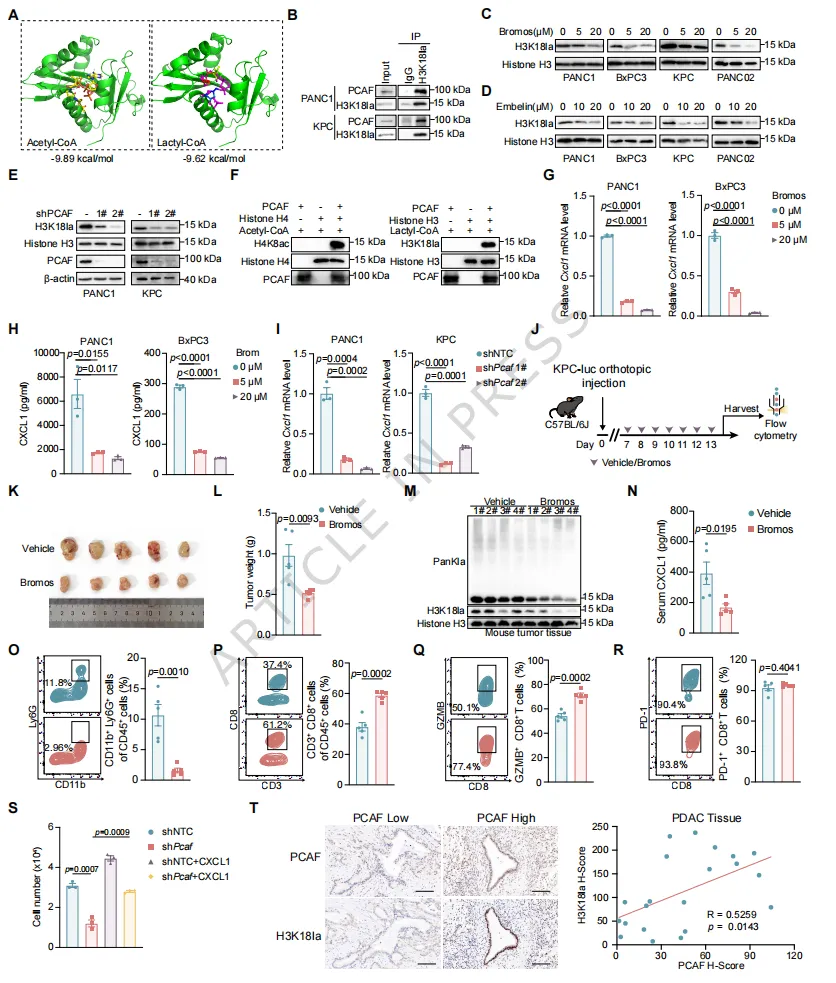
图 4 PCAF 作为胰腺癌中 H3K18 的组蛋白乳酸转移酶
5:PCAF抑制剂联合抗PD-1,协同攻克胰腺癌
最具转化价值的结果:
单独抗PD-1对胰腺癌几乎无效
PCAF抑制剂+抗PD-1联合治疗:
1.显著缩小肿瘤体积,延长小鼠生存期
2.减少肿瘤中性粒细胞浸润,增加CD8+T细胞与GZMB+杀伤性T细胞
3.降低PD-1+耗竭T细胞比例,逆转免疫抑制
4.下调H3K18la与CXCL1水平,阻断免疫逃逸通路成功将胰腺癌“冷肿瘤”转化为“热肿瘤”,实现免疫治疗增效。
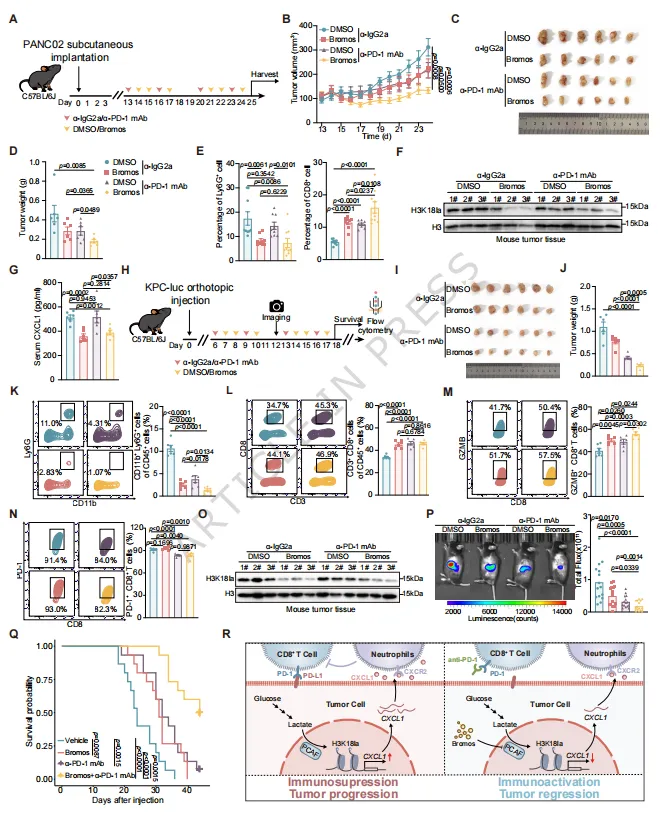
图 5 PCAF 抑制剂与抗 PD-1 单抗联合治疗胰腺癌
文章总结
本研究首次在胰腺癌中完整阐明乳酸-PCAF-H3K18la-CXCL1全新代谢-表观-免疫轴:肿瘤通过高糖酵解产生乳酸,PCAF催化H3K18la转录激活CXCL1,招募中性粒细胞构建免疫抑制微环境,最终介导免疫逃逸。该成果三大核心价值:
揭示胰腺癌免疫逃逸全新表观机制,填补代谢与免疫交叉领域空白 鉴定PCAF、H3K18la、CXCL1为胰腺癌预后标志物与治疗靶点 开创PCAF抑制剂+免疫检查点抑制剂联合方案,为胰腺癌免疫治疗提供全新方向
集思从集思专业从事大数据分析、质谱流式、CUT&Tag、分子对接、动物模型,生信分析和课题设计服务,需要的老师长按下面二维码联系。

往期推荐 ·
IF15.4顶刊!巴豆酰化修饰组学揭秘癫痫发病新机制:重庆医科大学肖飞团队发现STXBP1巴豆酰化修饰失衡致抑制性突触传递受损加重癫痫易感性
IF=33.9重庆医科大学:KDM5B驱动代谢-表观级联通路,通过乳酸化修饰 hnRNPA1调控AR-V7剪接,破解前列腺癌恩杂鲁胺耐药难题
《PNAS》(IF=14.1)重磅发布!田恒力团队合作揭示m⁶A修饰通过SOCS3调控小胶质细胞“刹车”神经炎症,为创伤性脑损伤治疗提供新靶点
注:本文原创表明为原创编译,非声张版权,侵删!
关于集思慧远
1.基因/转录/蛋白/代谢/微生物等常规高通量组学及单细胞和空间转录组等时空组学;
2.表观组学:WGBS/Ribo-seq/CUT&Tag/ATAC-seq/Hi-c/m6A/m5C/ac4C等各类修饰)的表观遗传研究,助力新靶点发现、药物作用机制研究及疾病表观调控机制探索;
3.蛋白修饰:磷酸化、乙酰化、泛素化、乳酸化、组蛋白甲基化等修饰
4.专业的医学方案整体设计,利用生物信息学对公共数据进行深入挖掘分析,并提供干湿结合实验;
5.新靶点发现及验证服务,通过ABPP/TPP/DARTS等技术加速小分子药物靶点发现;
6.难成药靶点降解剂开发技术PROTAC;
7.基于AI的药物筛选/设计/优化/抑制剂开发等;
8.无需抗体的临近标记(PLA)技术提供蛋白互作研究。
9.纳米材料递送药物系统开发,定制化纳米载体设计与制备,解决药物靶向递送至病灶组织/细胞等药物递送难题。
