南昌大学江西医学院丨多孔微球联合姜黄素与骨髓间充质干细胞:糖尿病创面修复的新策略
- 2026-03-31 20:27:06
前言
针对糖尿病创面微环境紊乱、干细胞增殖能力有限、药物利用不足的治疗难题,本研究通过气体辅助挥发微乳技术结合表面碱处理制备 PLGA 开放多孔微球,将姜黄素包封于 BSA 纳米粒并接枝到微球上,同时负载骨髓间充质干细胞(BMSCs)构建 BMSC@COPM 复合体系,利用微球大孔结构支撑 BMSCs、实现姜黄素 35 天持续释放;该体系通过姜黄素缓释促进干细胞增殖并激活细胞线粒体自噬,重塑创面免疫微环境、缓解慢性炎症,同时调控 HIF-1α 表达促进血管生成,协同 BMSCs 实现血管再生与胶原网络重建,体外实验验证了体系的生物相容性、促细胞迁移及血管生成能力,体内实验证实其可显著加速糖尿病创面愈合,最终表明药物 - 干细胞 - 微球的整合策略为糖尿病创面治疗提供了极具潜力的新方法。

研究要点解析
研究方法
首先采用气体辅助挥发微乳技术结合碱处理制备具有开放互连孔结构的 PLGA 微球(OPM),通过脱溶剂法制备姜黄素 @BSA 纳米粒(CNPs)并接枝到 OPM 上得到 COPM,再负载 BMSCs 构建 BMSC@COPM 复合体系;随后对微球的理化性质、降解性、药物负载与释放能力进行表征,通过体外实验验证体系的生物相容性、对 BMSCs 的保护作用,以及促成纤维细胞迁移、血管内皮细胞血管生成的能力;接着构建糖尿病小鼠创面模型,通过体内实验评估体系的创面愈合效果,结合组织学染色、免疫组化等手段探究其作用机制;最后从细胞自噬、巨噬细胞极化、PI3K/Akt/mTOR 信号通路等角度,阐明复合体系通过调控创面微环境、促进血管生成与胶原再生加速糖尿病创面愈合的分子机制。
研究结果
成功制备的 PLGA 开放多孔微球粒径均一(230-290μm),具有互连孔结构,水吸收性显著提升,姜黄素包封率 79.57%、载药量 7.62%,可实现 35 天持续缓释;该微球对 BMSCs 具有高负载能力和保护作用,能显著提高干细胞在高糖、氧化应激环境下的存活率;体外实验显示 BMSC@COPM 可显著促进高糖环境下成纤维细胞的迁移与增殖,增强人脐静脉内皮细胞的血管生成能力,上调 HIF-1α、VEGF 等血管生成相关因子表达;体内实验证实 BMSC@COPM 可显著加速糖尿病小鼠创面愈合,第 14 天愈合率达 82%、第 21 天达 97%,促进创面再上皮化、肉芽组织形成与胶原沉积及成熟;机制研究发现该体系可激活细胞自噬,诱导巨噬细胞从 M1 向 M2 极化,缓解慢性炎症,且通过非经典的 PI3K/Akt/mTOR 通路调控自噬,协同实现创面免疫微环境重塑、血管生成与组织再生。
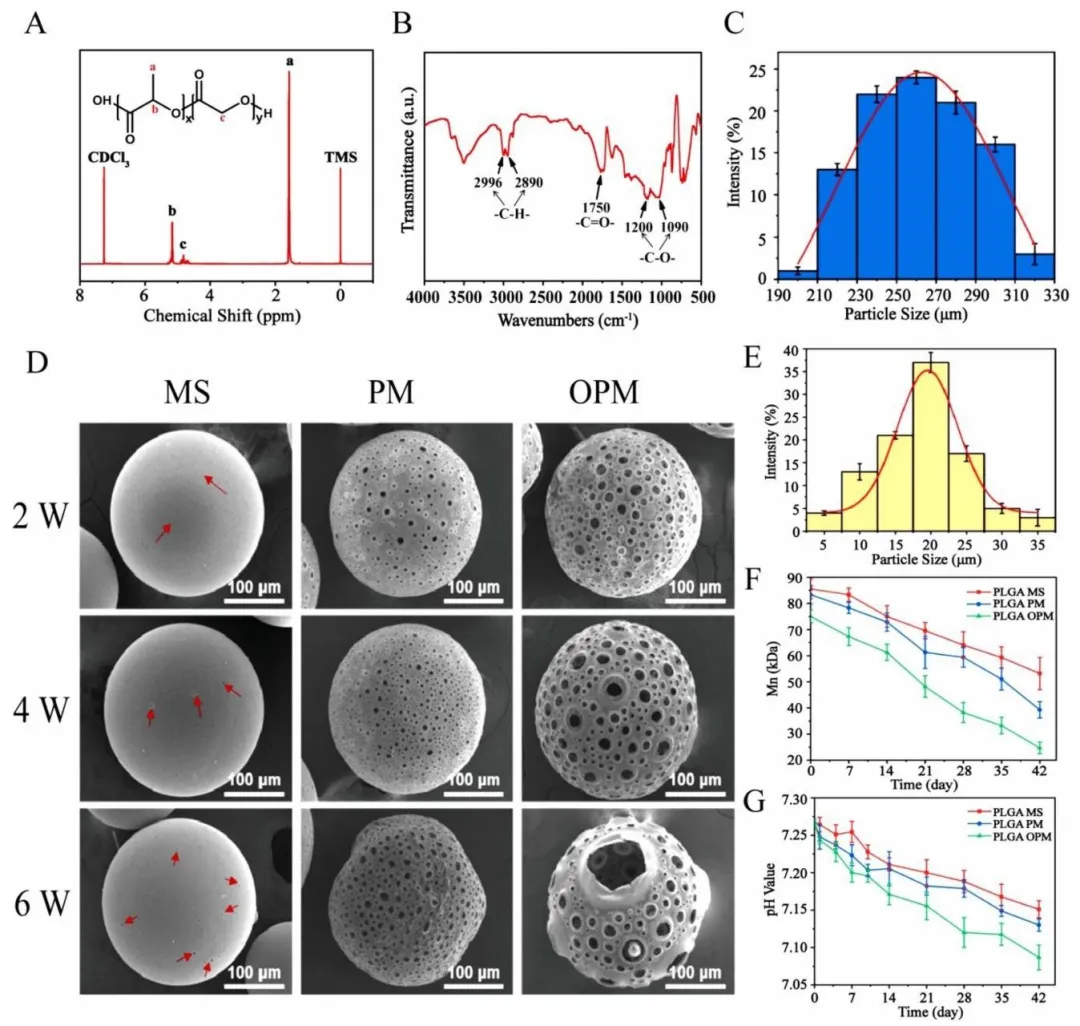
Figure 1:通过氢谱、红外光谱验证了 PLGA 微球的化学结构,粒径分布实验证实微球粒径均一且符合细胞负载与注射要求;SEM 观察显示不同制备条件下微球呈现实心、多孔、开放多孔的表面形态差异,碱处理可实现微球孔结构的调控;降解实验表明开放多孔微球(OPM)降解速率最快,且降解过程中上清液 pH 稳定在 7 以上,不会破坏机体酸碱平衡,同时明确了微球降解过程中的分子量变化规律。
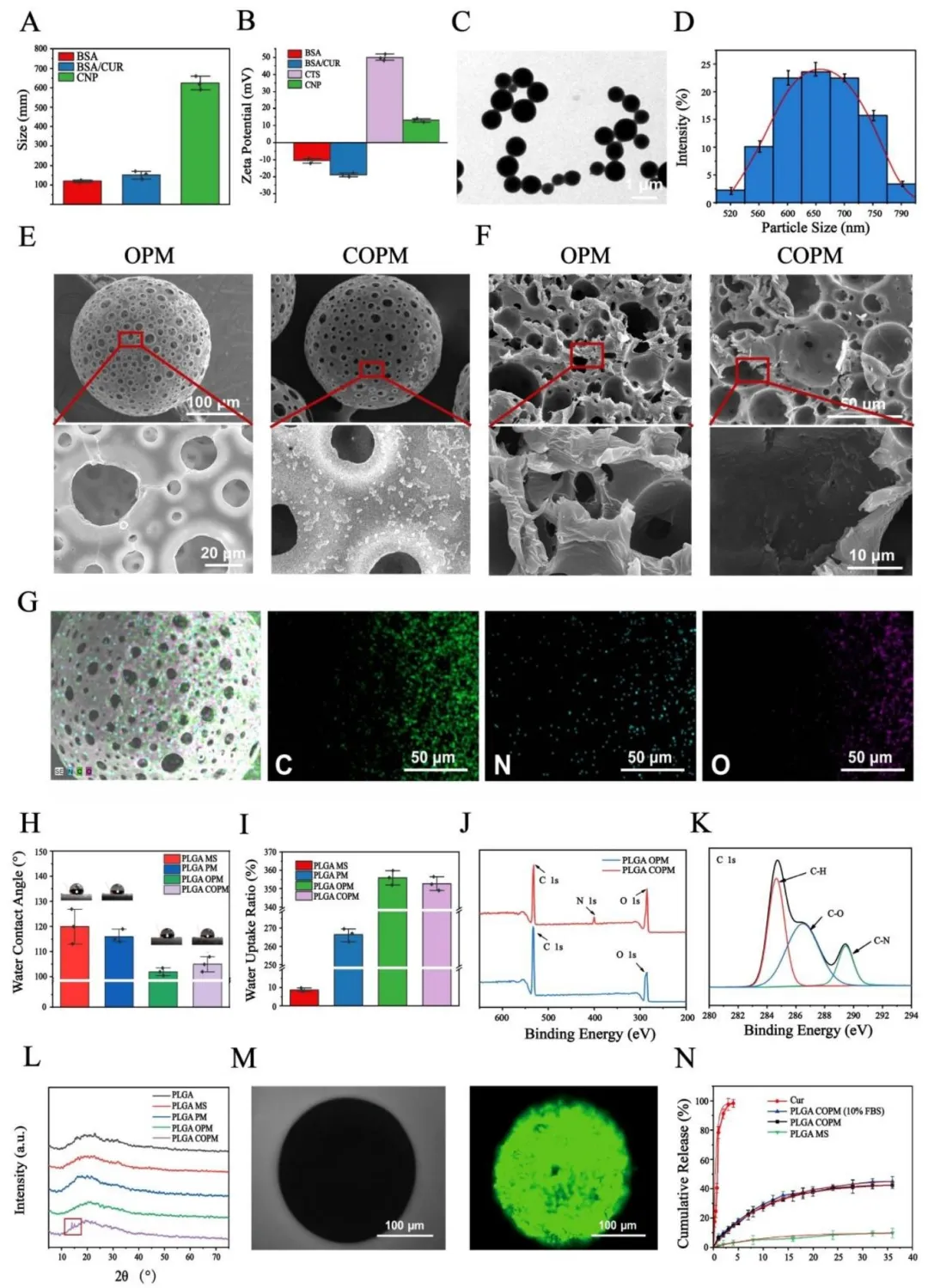
Figure 2:表征了姜黄素 @BSA 纳米粒(CNPs)的粒径、电位与形貌,证实壳聚糖修饰实现了纳米粒表面电荷的反转与结构稳定;SEM 与 EDS 验证了 CNPs 成功接枝到 PLGA OPM 上形成 COPM,且 N 元素分布均匀;接触角与水吸收实验表明开放多孔结构显著提升了微球的亲水性;XPS、XRD 与荧光成像进一步证实 COPM 的成功制备及姜黄素的有效负载;药物释放实验表明 COPM 可实现姜黄素的 35 天持续缓释,为创面长期治疗提供基础。
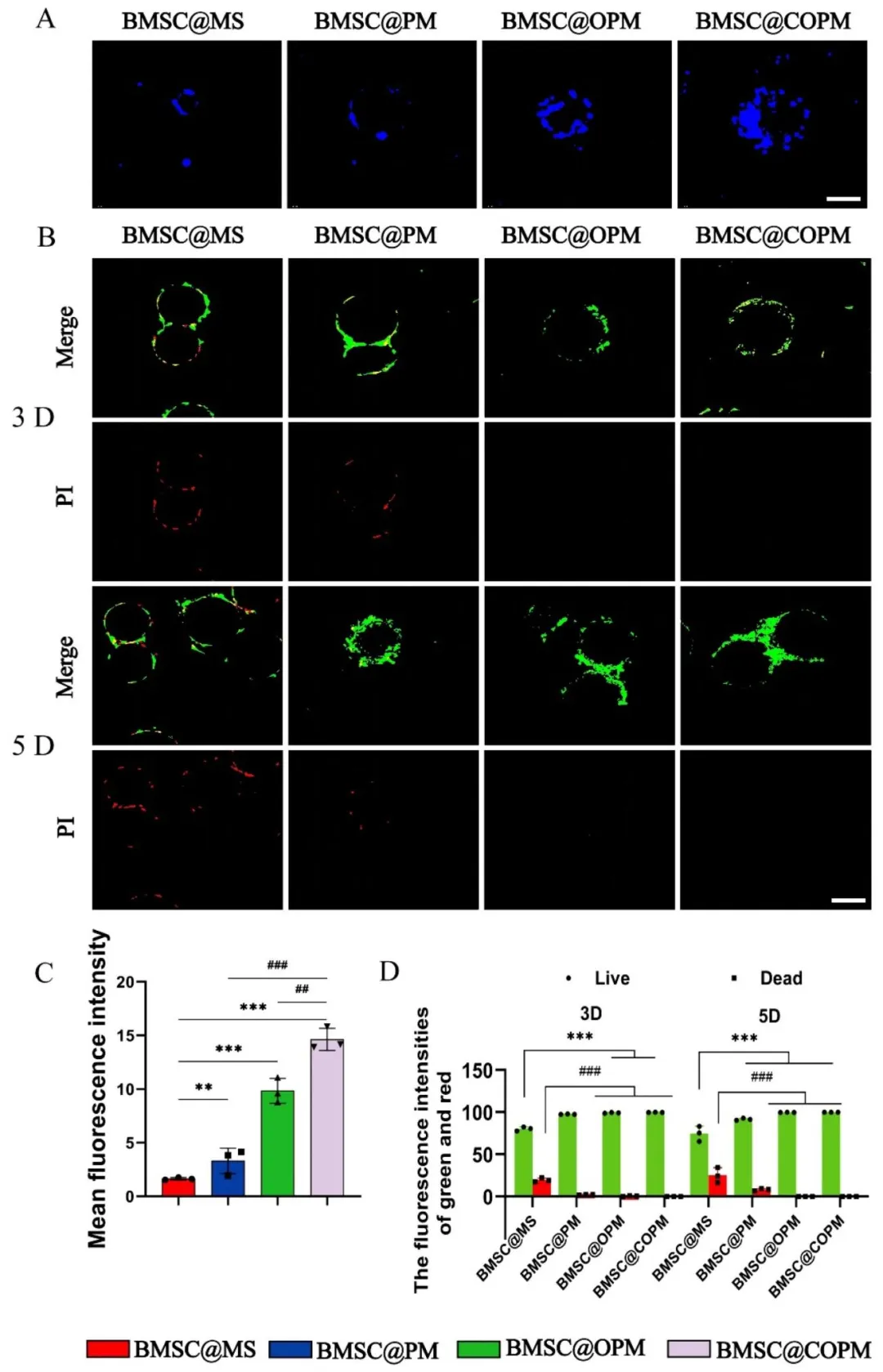
Figure 3:DAPI 染色显示微球的孔结构越开放,BMSCs 的黏附能力越强,COPM 可实现干细胞的内部黏附与高负载;活 / 死细胞染色与荧光定量分析证实,开放多孔微球能显著提高 BMSCs 的存活率,且姜黄素的引入进一步增强了对干细胞的保护作用,3 天和 5 天均无明显死细胞,证明 BMSC@COPM 为干细胞提供了良好的存活微环境。
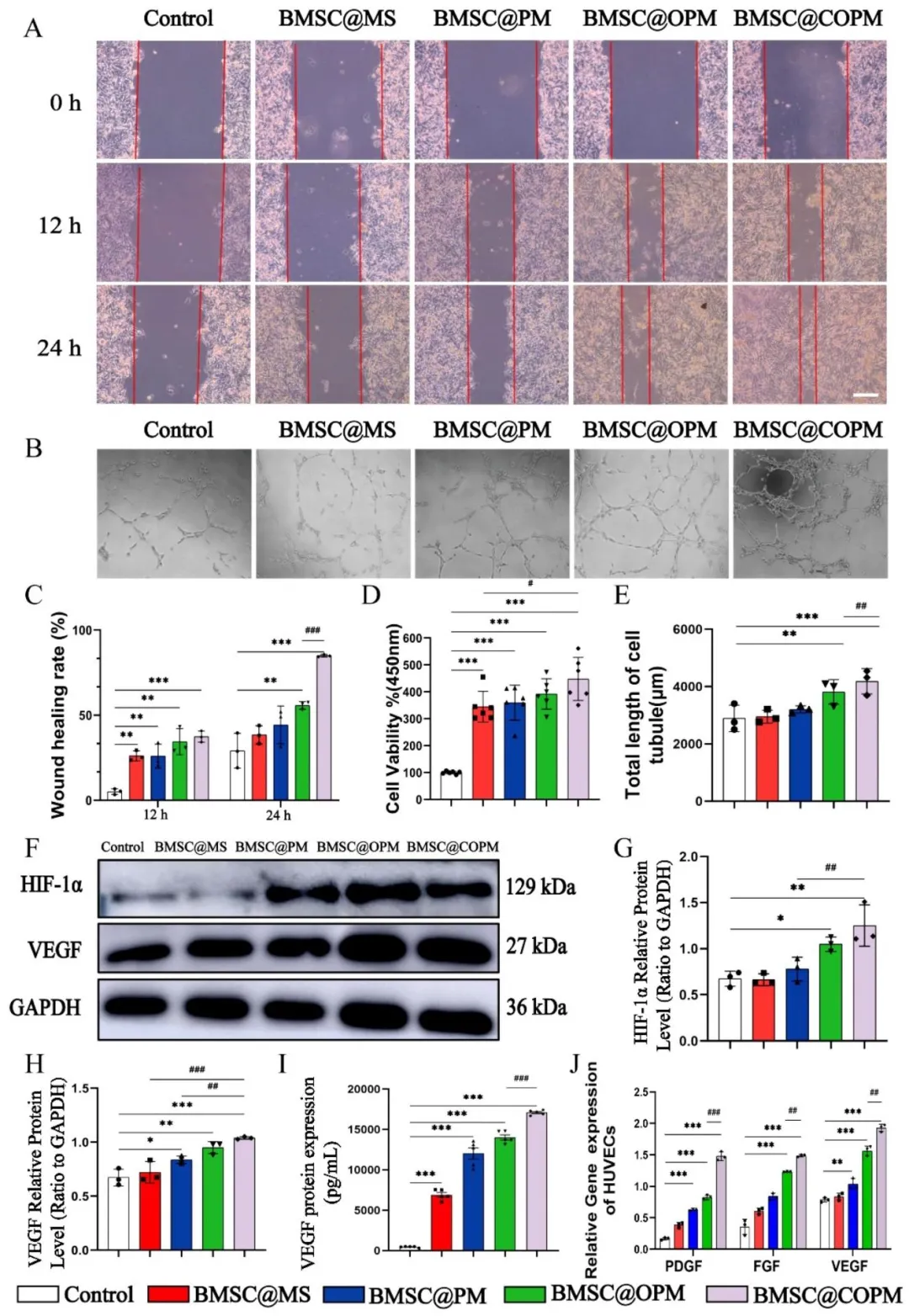
Figure 4:划痕实验证实 BMSC@COPM 在高糖环境下能显著促进成纤维细胞的迁移;管形成实验与 CCK-8 实验表明该体系可增强人脐静脉内皮细胞的增殖与血管生成能力,总血管长度显著增加;Western blot、ELISA 与 qRT-PCR 实验证实,BMSC@COPM 可显著上调 HIF-1α、VEGF、PDGF、FGF 等血管生成相关因子的蛋白与 mRNA 表达,阐明其促血管生成的分子基础。
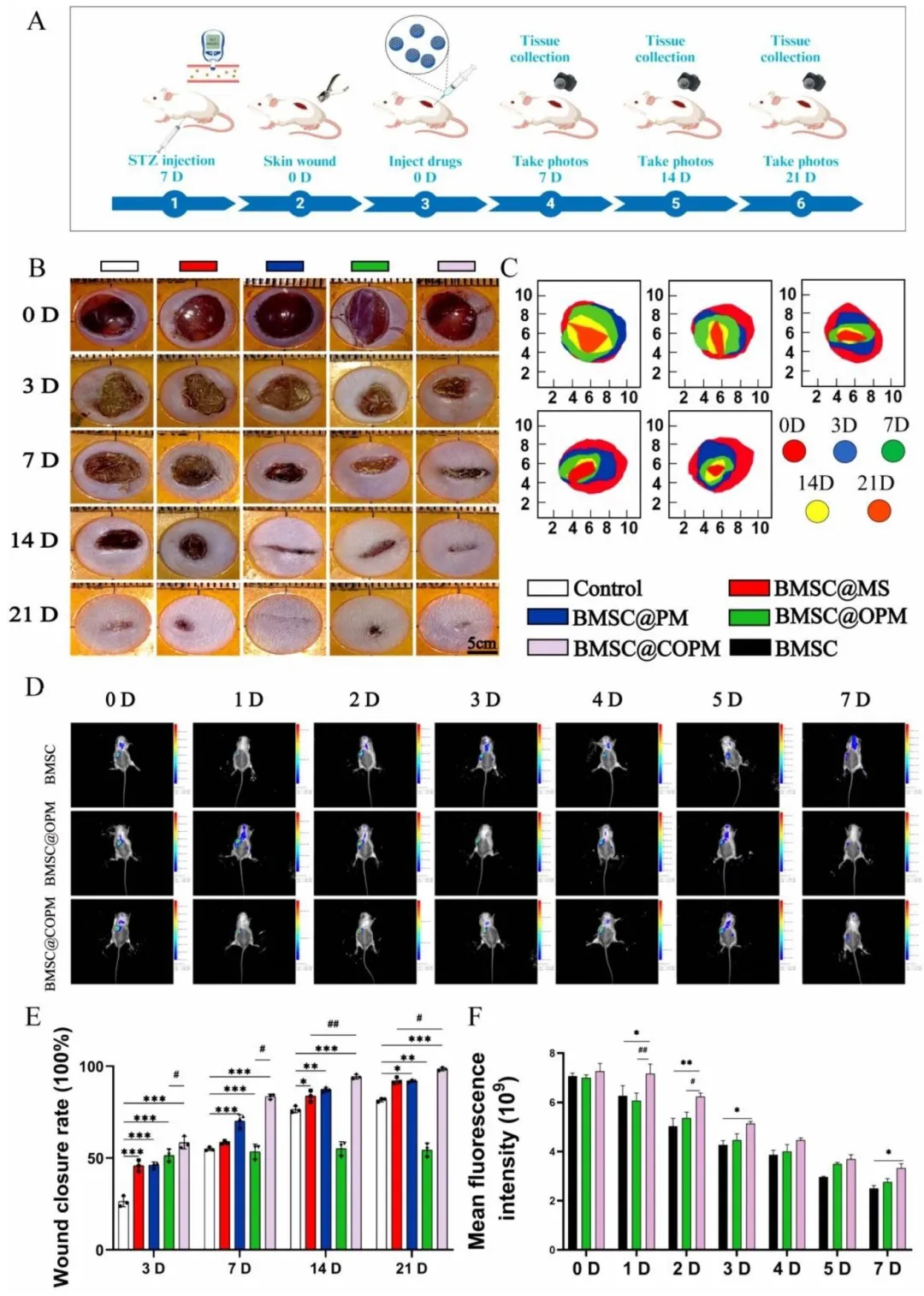
Figure 5:展示了糖尿病小鼠创面治疗的动物实验流程,创面愈合拍照结果与定量分析证实 BMSC@COPM 能显著加速创面收缩与愈合,愈合率显著高于其他组;小动物活体成像实验表明 COPM 可显著提高 BMSCs 在创面的定植与存活能力,为创面愈合提供持续的干细胞作用,是其高效治疗的重要原因。
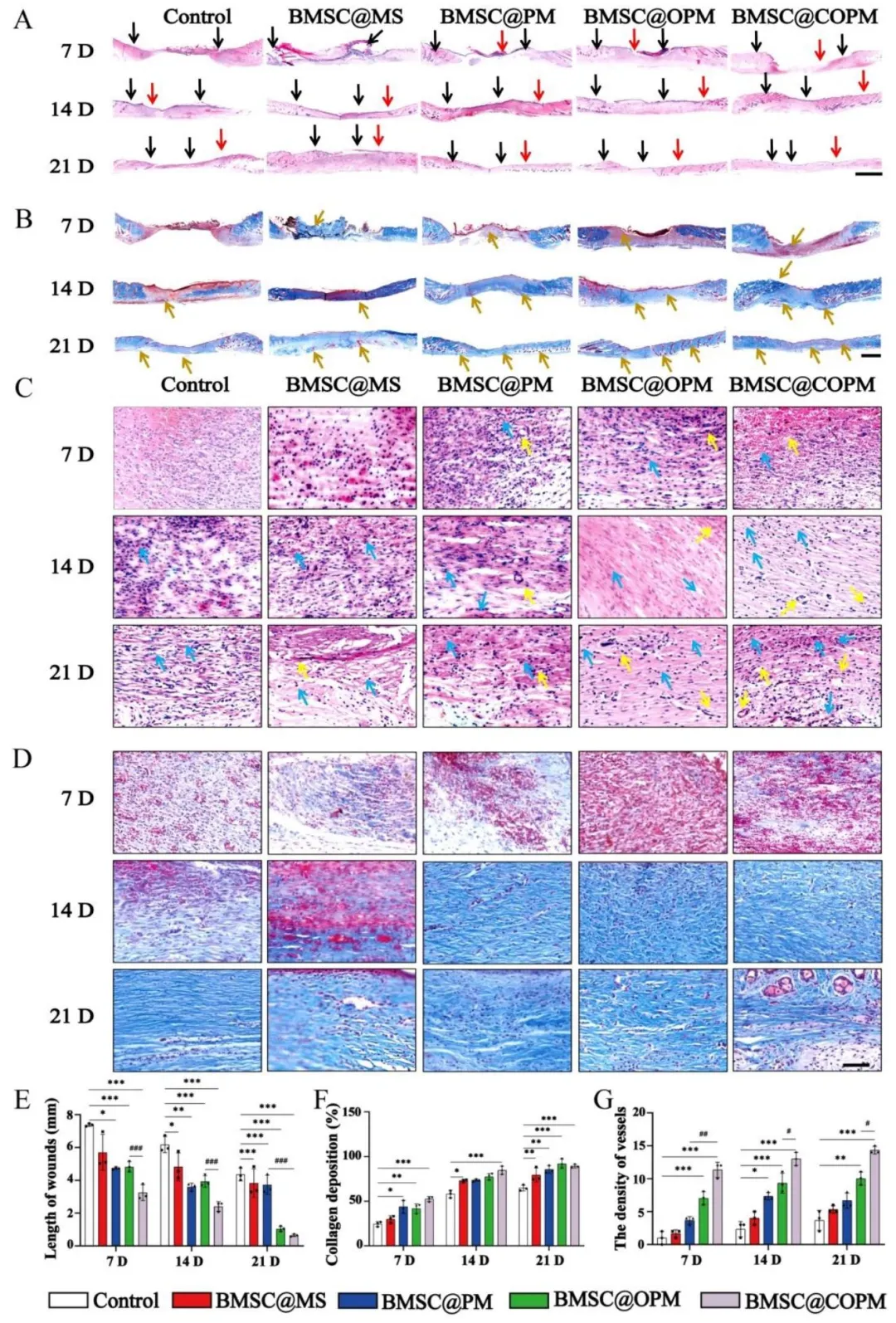
Figure 6:H&E 染色显示 BMSC@COPM 能显著促进创面再上皮化、肉芽组织形成,缩短创面长度,组织病理学评分显著高于其他组;Masson 三色染色与天狼星红染色证实该体系可显著促进创面胶原沉积与成熟,胶原排列更规则;定量分析表明 BMSC@COPM 能显著增加创面新生血管数量,促进胶原网络重建,实现高质量的创面组织重塑。
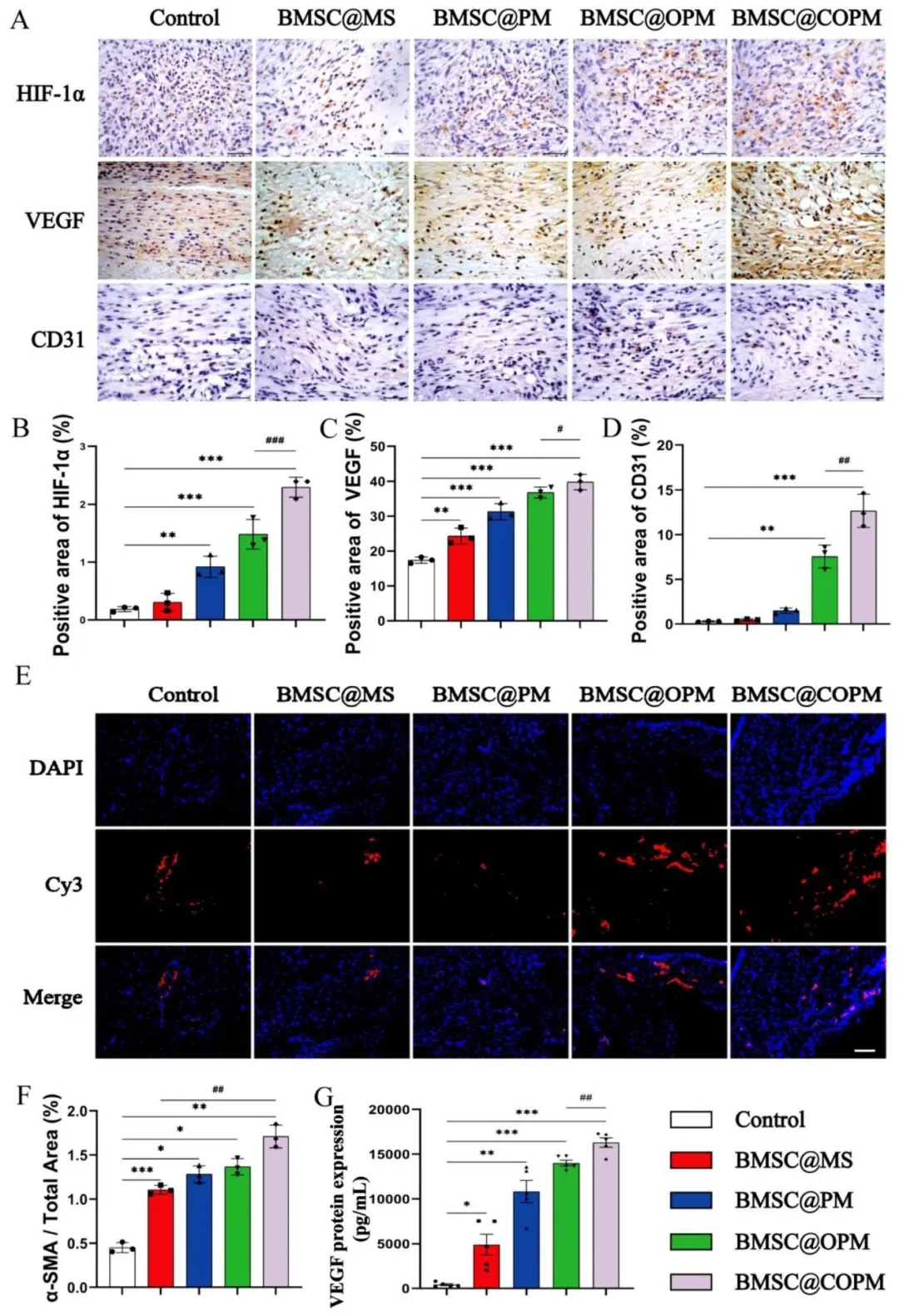
Figure 7:免疫组化实验证实 BMSC@COPM 可显著上调创面组织中 HIF-1α、VEGF、CD31 的蛋白表达,免疫荧光实验表明 α-SMA 表达显著增加;蛋白定量与 ELISA 实验进一步验证了血管生成相关因子的高表达,阐明 BMSC@COPM 通过激活 HIF-1α/VEGF 通路促进创面血管生成,改善创面血供,加速糖尿病创面愈合。
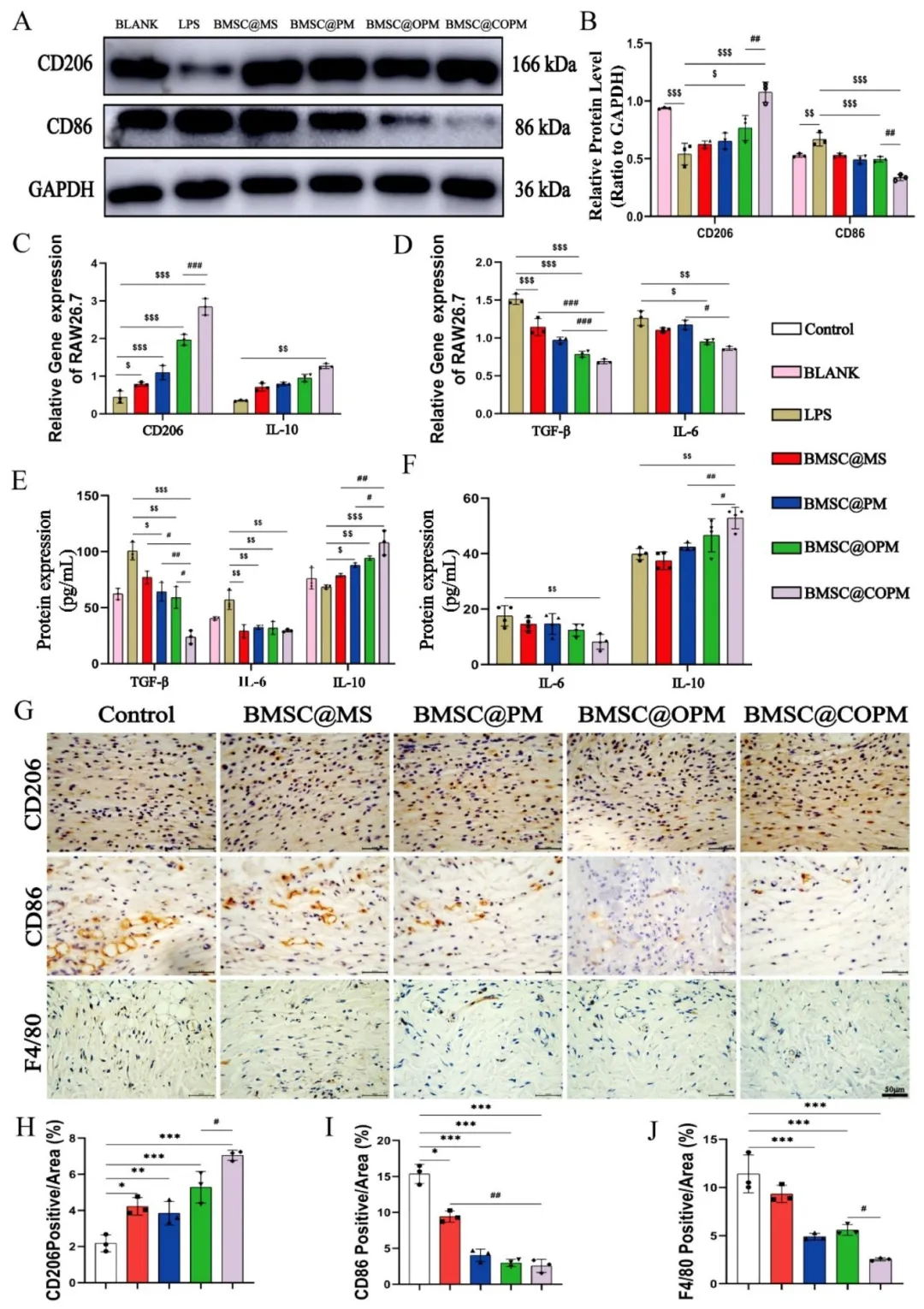
Figure 8:Western blot 与 qRT-PCR 实验表明 BMSC@COPM 可显著下调 RAW264.7 巨噬细胞中 M1 型标志物(IL-6、CD86),上调 M2 型标志物(IL-10、CD206)的蛋白与 mRNA 表达;ELISA 实验证实该体系可降低小鼠血清中促炎因子、升高抗炎因子;体内免疫组化实验表明 BMSC@COPM 能减少创面 F4/80 + 巨噬细胞浸润,促进 CD206+M2 型巨噬细胞极化,缓解创面慢性炎症,重塑创面免疫微环境。
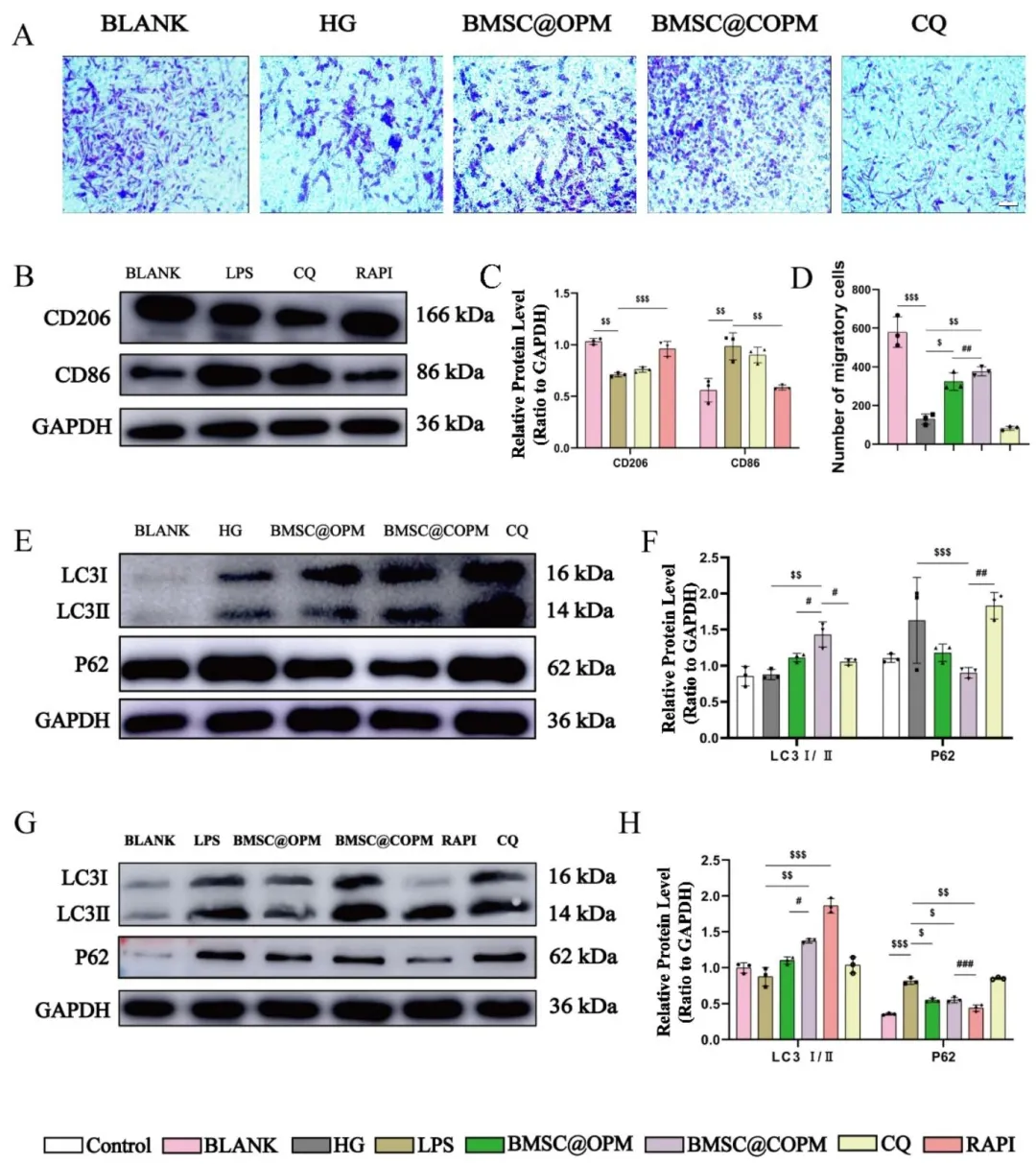
Figure 9:Transwell 实验证实 BMSC@COPM 可促进高糖环境下成纤维细胞的迁移,而自噬抑制剂氯喹可逆转该效应;Western blot 实验表明 BMSC@COPM 能上调 LC3II/LC3I 比值、下调 P62 表达,激活成纤维细胞自噬;同时该体系可逆转 LPS 诱导的巨噬细胞 M1 极化,自噬诱导剂雷帕霉素可促进 M2 极化、抑制剂氯喹则抑制,证实 BMSC@COPM 通过激活自噬促进成纤维细胞增殖迁移,并诱导巨噬细胞 M2 极化。
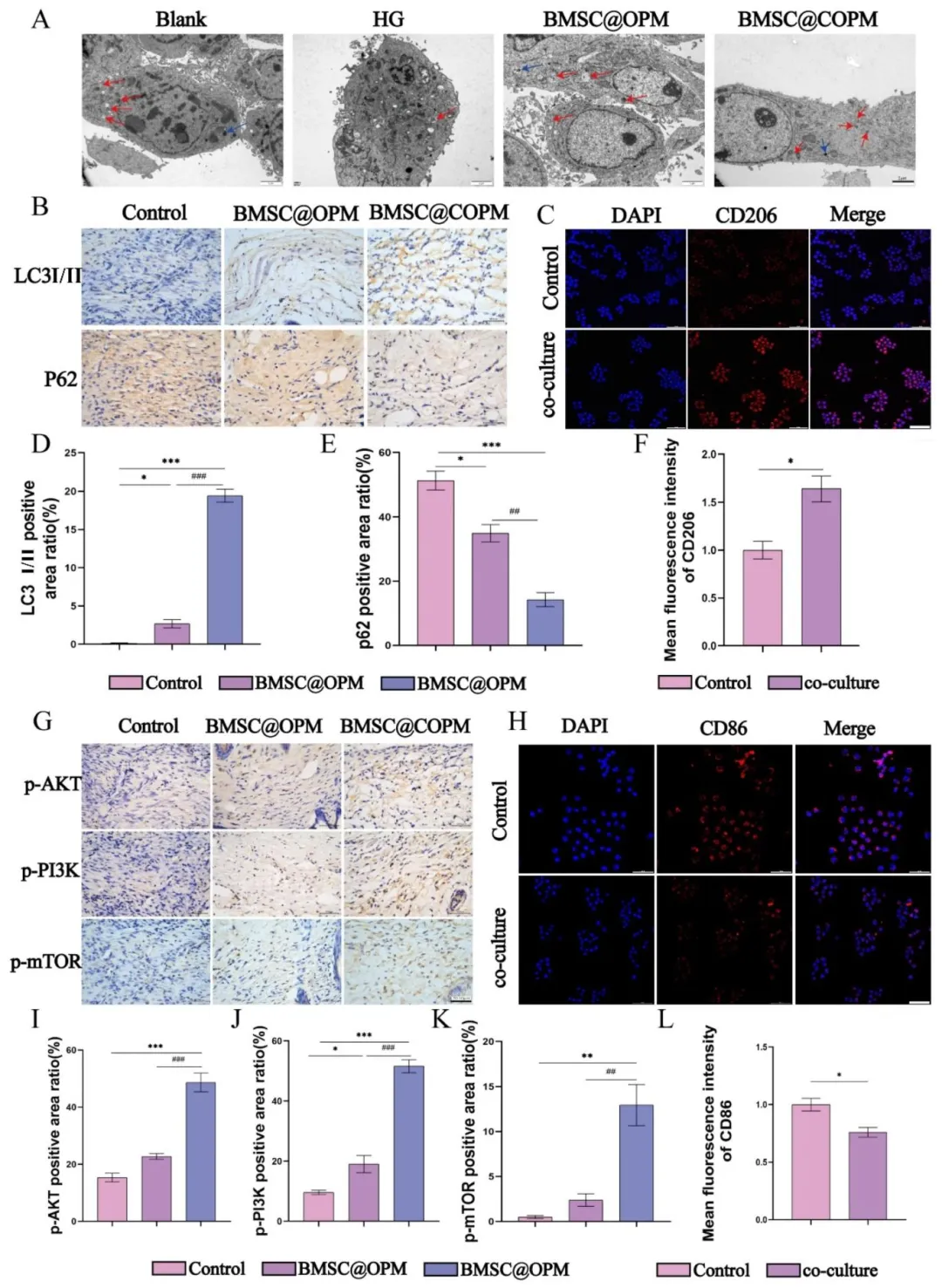
Figure 10:TEM 观察证实 BMSC@COPM 可在高糖环境下诱导成纤维细胞形成自噬体,激活细胞自噬;体内免疫组化实验表明该体系可上调创面组织中 LC3I/II、下调 P62,验证了体内自噬激活效应;Western blot 实验证实 BMSC@COPM 通过激活 PI3K/Akt/mTOR 信号通路调控自噬,为非经典的自噬调控机制;共培养实验表明 BMSCs 与巨噬细胞的相互作用可进一步促进 M2 极化,协同实现抗炎与创面修复。
研究结论
本研究证实 BMSC@COPM 复合体系通过多机制协同实现糖尿病创面的高效修复,开放多孔 PLGA 微球为 BMSCs 提供了良好的黏附与存活微环境,姜黄素的持续缓释不仅保护干细胞、促进其增殖,还能激活细胞自噬,通过 PI3K/Akt/mTOR 非经典通路调控自噬,一方面促进成纤维细胞迁移增殖、血管内皮细胞血管生成,另一方面诱导巨噬细胞从 M1 向 M2 极化,缓解慢性炎症,重塑创面免疫微环境,同时调控 HIF-1α/VEGF 通路促进血管生成,加速胶原沉积与成熟,实现创面组织的再生与重塑;该复合体系相比传统单一治疗或简单材料复合,在药物缓释、干细胞保护、微环境调控等方面具有显著优势,其制备的 PLGA 开放多孔微球解决了传统微球疏水性药物负载效率低、干细胞黏附能力差的问题,为干细胞与药物的协同递送提供了新的载体平台。但本研究仍存在一定局限性,一是该体系的临床转化面临产品价格、稳定性与运输的挑战,需要进一步优化制备工艺以降低成本、提升产品稳定性;二是干细胞体内应用的伦理问题仍需进一步规范,需符合相关市场与临床监管规定;三是研究仅探究了小鼠模型中的治疗效果,尚未开展大动物实验与临床研究,其在人体中的安全性与有效性仍需进一步验证;四是对 PI3K/Akt/mTOR 非经典调控自噬的具体分子机制探究仍不够深入,后续需开展更细致的机制研究以明确关键调控靶点。
本文中使用的图片来Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

生物信息学课题设计及指导实录,目前生信是否还适用于课题及文章?看专家给你解答
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
科研信息合集
国内外医学博后招聘
国自然课题设计思路
各大学校及医院国自然立项信息
骨科科研最新分享
泌尿外科科研最新分享
消化领域科研最新分享