JEV|南昌大学刘琼、黄孝天教授团队:一种用于细胞因子递送的工程化纳米囊泡佐剂平台(ENAP)可作为针对幽门螺杆菌的新型抗原协同疫苗
幽门螺杆菌感染是慢性胃炎、消化性溃疡及胃癌的主要病因。由于抗生素耐药性问题日益严重,疫苗接种成为有前景的防控策略。然而,传统佐剂主要诱导Th2型免疫应答,难以有效清除定植于胃黏膜的病原体;而强效佐剂如霍乱毒素存在安全隐患。因此,精准调控黏膜免疫应答成为该领域长期未解的瓶颈。
近日,南昌大学基础医学院刘琼教授、黄孝天教授团队在Journal of Extracellular Vesicles上发表了题为“An engineered nano-vesicle adjuvant platform (ENAP) for cytokine delivery enables a novel antigen coordinated vaccine against Helicobacter pylori”的研究成果,在幽门螺杆菌疫苗佐剂研发方面取得重要进展。 博士研究生尚银攀为第一作者,刘琼教授和黄孝天教授为通讯作者。
该研究表明,基于基因工程改造的幽门螺杆菌(H. pylori)外膜囊泡(OMVs)构建的工程化纳米囊泡佐剂平台(ENAP),通过递送IL-17A和IFN-γ表达质粒,可作为新型抗原协调疫苗的佐剂系统。ENAP利用AI筛选最优细胞因子组合,将质粒电穿孔封装至LPS修饰的低毒重组OMVs(rOMVs)中(实验室前期研究构建的低毒菌株,JEV. 2025;14(5):e70085.),实现了细胞因子的靶向递送和局部微环境重编程。该平台经口服免疫后,显著增强抗原特异性全身及黏膜免疫应答(IgG和IgA),诱导平衡的Th1/Th2/Th17细胞免疫,并有效降低攻毒后胃内H. pylori定植量。ENAP克服了传统佐剂(铝佐剂Th2偏倚、CT/LT毒性)的局限,是一种可编程、模块化的下一代黏膜疫苗佐剂平台。
主要内容:
1.AI驱动的细胞因子筛选与ENAP平台构建
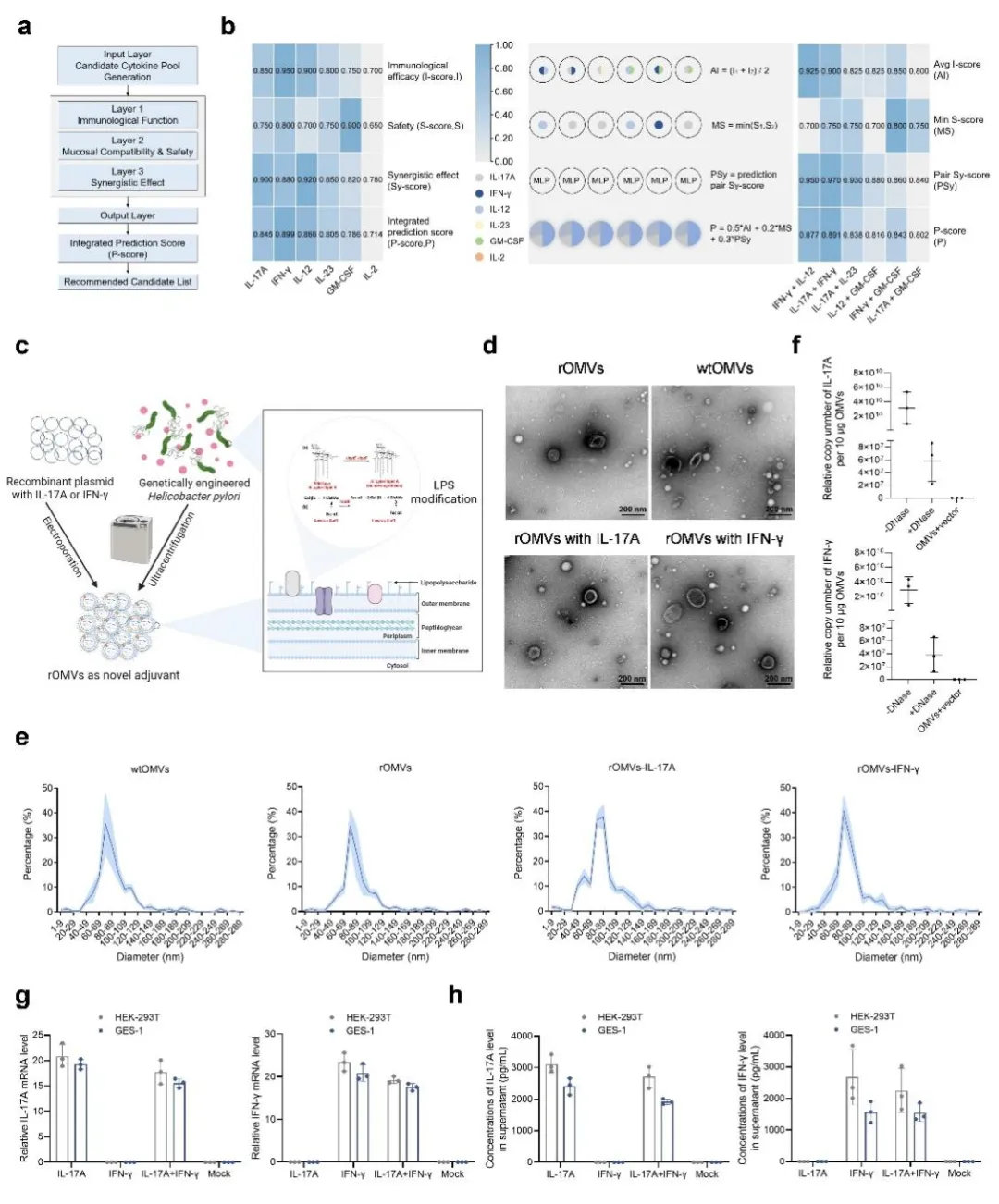
研究的一个核心亮点在于作者利用AI分析适用于H. pylori疫苗的细胞因子佐剂,并装载于rOMVs平台。首先利用AI进行多步筛选,从公共数据库和文献中挖掘候选细胞因子,结合免疫功效、黏膜安全性和协同潜力,通过XGBoost、SVM和MLP模型预测,最终选定IL-17A和IFN-γ作为最优组合。随后,将编码IL-17A和IFN-γ的质粒通过电穿孔装载至经LPS修饰(ΔlpxEΔlpxFΔfutB)的H. pylori 的rOMVs中,形成ENAP。透射电镜显示,LPS修饰和质粒装载均未改变OMVs的球形形态(直径约20-200 nm),qPCR证实质粒被有效包封于囊泡内部。将ENAP与HEK-293T或GES-1细胞共孵育后,qRT-PCR和ELISA检测到IL-17A和IFN-γ水平显著升高,证明rOMVs可将质粒高效递送至细胞并驱动细胞因子表达。
2.ENAP诱导持久的全身及黏膜免疫应答
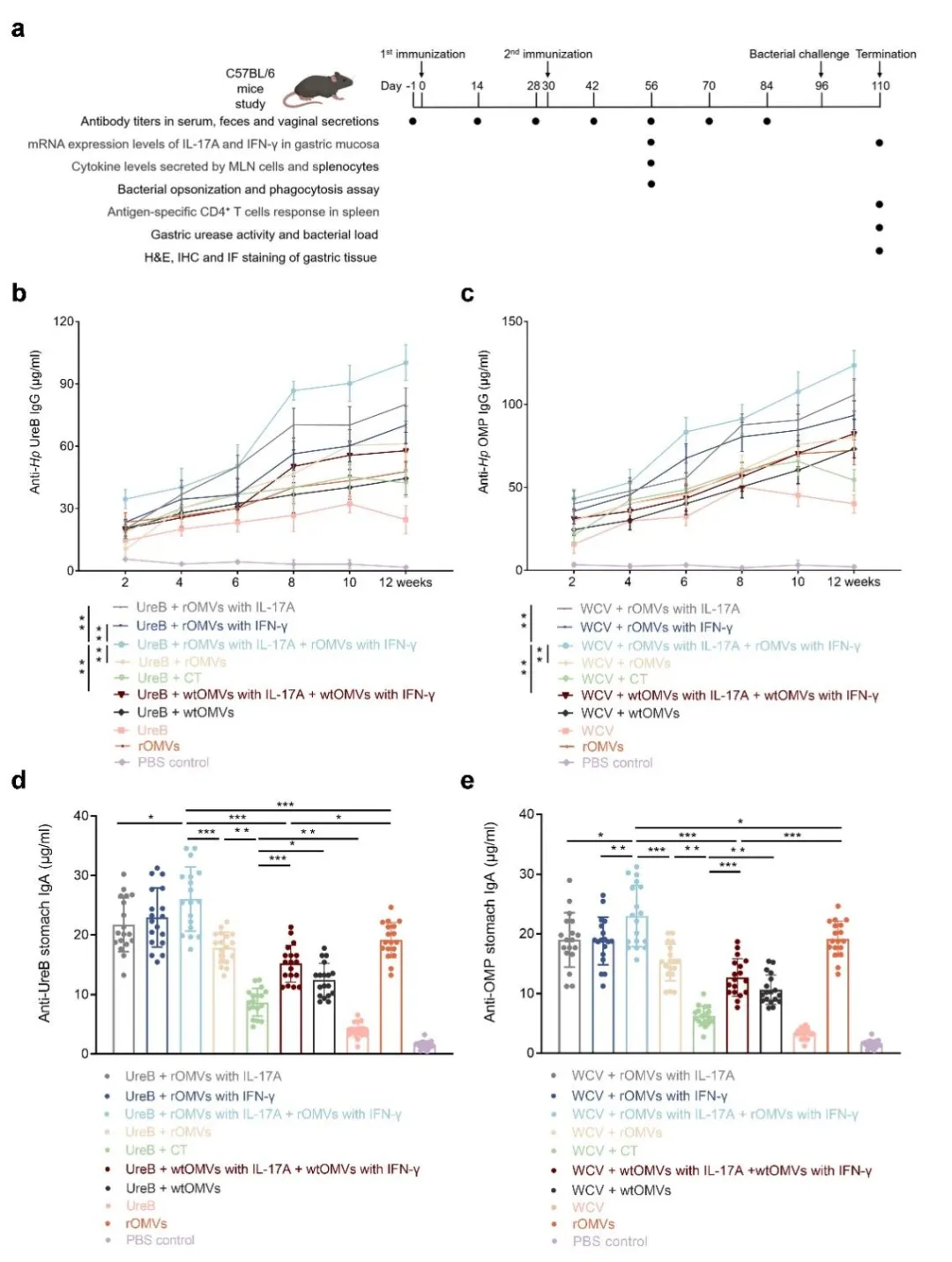
将ENAP分别与重组UreB亚单位抗原或灭活全菌抗原(WCV)联合,经口免疫C57BL/6小鼠。ELISA结果显示,ENAP佐剂组在第8周(攻毒前)和第12周(攻毒后)均维持最高的抗原特异性血清IgG滴度,显著优于CT佐剂或野生型OMVs组。同时,胃黏膜IgA、阴道洗液及粪便中分泌型IgA水平也明显升高,且持续时间更长。组织学检查发现ENAP组胃黏膜CD45⁺免疫细胞浸润显著增加,表明ENAP成功激活了局部黏膜免疫。
3.ENAP协同抗原激发平衡型Th1/Th2/Th17保护性免疫,有效降低H. pylori定植
在攻毒保护实验中,ENAP佐剂组小鼠胃内细菌载量最低,尿素酶活性显著下降,胃黏膜病理评分显著改善。机制上,血清抗体亚型分析显示ENAP同时提高IgG1和IgG2c水平,表明诱导了平衡的Th1/Th2应答。细胞因子ELISA和流式细胞分析证实,ENAP组小鼠MLN细胞和脾细胞中IL-12p40、IL-4和IL-17A分泌均显著增强,且CD4⁺CD154⁺IL-17A⁺和CD4⁺CD154⁺IFN-γ⁺ T细胞水平增加。
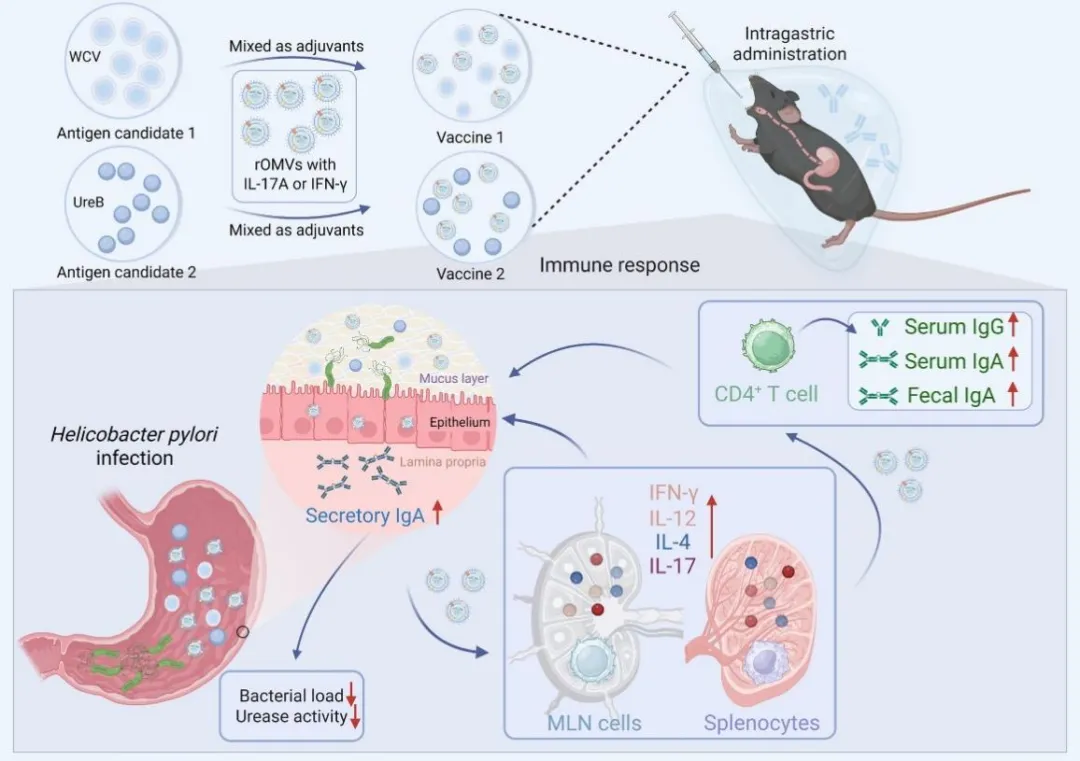
综上所述,ENAP通过创建局部细胞因子微环境,协同激活黏膜屏障和系统性Th1/Th17/Th2免疫,为抗H. pylori及其他黏膜病原体疫苗提供了可编程的下一代佐剂平台。该平台具有模块化、可编程特点,将传统佐剂发展为局部微环境重编程系统,为幽门螺杆菌疫苗研发提供了新工具,并具备良好的通用性,可快速适配其他黏膜病原体的疫苗开发需求。
参考文献:
An Engineered Nano-Vesicle Adjuvant Platform (ENAP) for Cytokine Delivery Enables a Novel Antigen-Coordinated Vaccine Against Helicobacter pylori. J Extracell Vesicles. 2026;15(4):e70274. doi:10.1002/jev2.70274.
Development of a Recombinant Outer Membrane Vesicles (OMVs)-Based Vaccine Against Helicobacter pylori Infection in Mice. J Extracell Vesicles. 2025;14(5):e70085. doi:10.1002/jev2.70085.
