南昌大学第二附属医院 | 滑膜液微生物驱动骨关节炎,TLR2 / JNK / AP-1 通路是关键
- 2026-04-22 14:27:16

导读
本研究针对传统认为关节腔无菌、骨关节炎发病机制未完全阐明的问题,先通过 16S rRNA 高通量测序与培养组学分析骨关节炎患者滑膜液微生物,筛选出与疾病进展正相关的藤黄微球菌 G18;再构建大鼠骨关节炎模型,开展滑膜液微生物移植与藤黄微球菌 G18 干预实验,验证其促炎促软骨降解作用;随后通过软骨细胞体外实验,明确细菌细胞壁肽聚糖为关键效应分子,并探索其作用通路;最后用 JNK 抑制剂反向验证通路,最终证实藤黄微球菌 G18 通过肽聚糖激活 TLR2/JNK/AP-1 通路,破坏软骨细胞合成与降解平衡,加剧软骨损伤与骨关节炎进展,为骨关节炎的微生物靶向诊疗提供新方向。
注:该文章发表于《Advanced Science》,最新影响因子为14.1,位列JCR和中科院分区Q1/1区。
首次系统证实人类膝关节腔存在稳定微生物群,颠覆关节无菌传统认知;鉴定出藤黄微球菌 G18 为骨关节炎进展核心驱动菌;阐明其通过肽聚糖激活 TLR2/JNK/AP-1 通路加剧软骨降解的机制,为骨关节炎提供微生物标志物与靶向治疗新思路。
临床层面纳入 40 例不同分期骨关节炎患者,按 K-L 分级分轻、重度组,采集滑膜液,用扫描电镜观察微生物,16S rRNA 高通量测序分析菌群多样性与组成,培养组学分离鉴定菌株;动物层面构建 MIA 诱导大鼠骨关节炎模型,设抗生素预处理、滑膜液微生物移植、藤黄微球菌 G18 注射、JNK 抑制剂干预组,检测关节肿胀、步态、病理、骨微结构及炎症因子;细胞层面用原代软骨细胞与活菌、灭活菌、肽聚糖、JNK 抑制剂共培养,检测细胞活力、基质合成降解、通路蛋白与基因表达。
临床检测显示重度骨关节炎患者滑膜液微生物多样性更高,变形菌门、厚壁菌门、放线菌门占主导,藤黄微球菌显著富集且与病情严重程度、病程正相关;大鼠实验中,重度患者滑膜液微生物或藤黄微球菌 G18 移植会加重关节肿胀、软骨损伤、炎症反应与软骨细胞凋亡;体外实验证实藤黄微球菌细胞壁肽聚糖为关键致病因子,可降低软骨细胞活力、抑制基质合成、促进降解;机制上肽聚糖激活 TLR2/JNK/AP-1 通路,抑制该通路可逆转软骨损伤与炎症,阻断骨关节炎恶化。
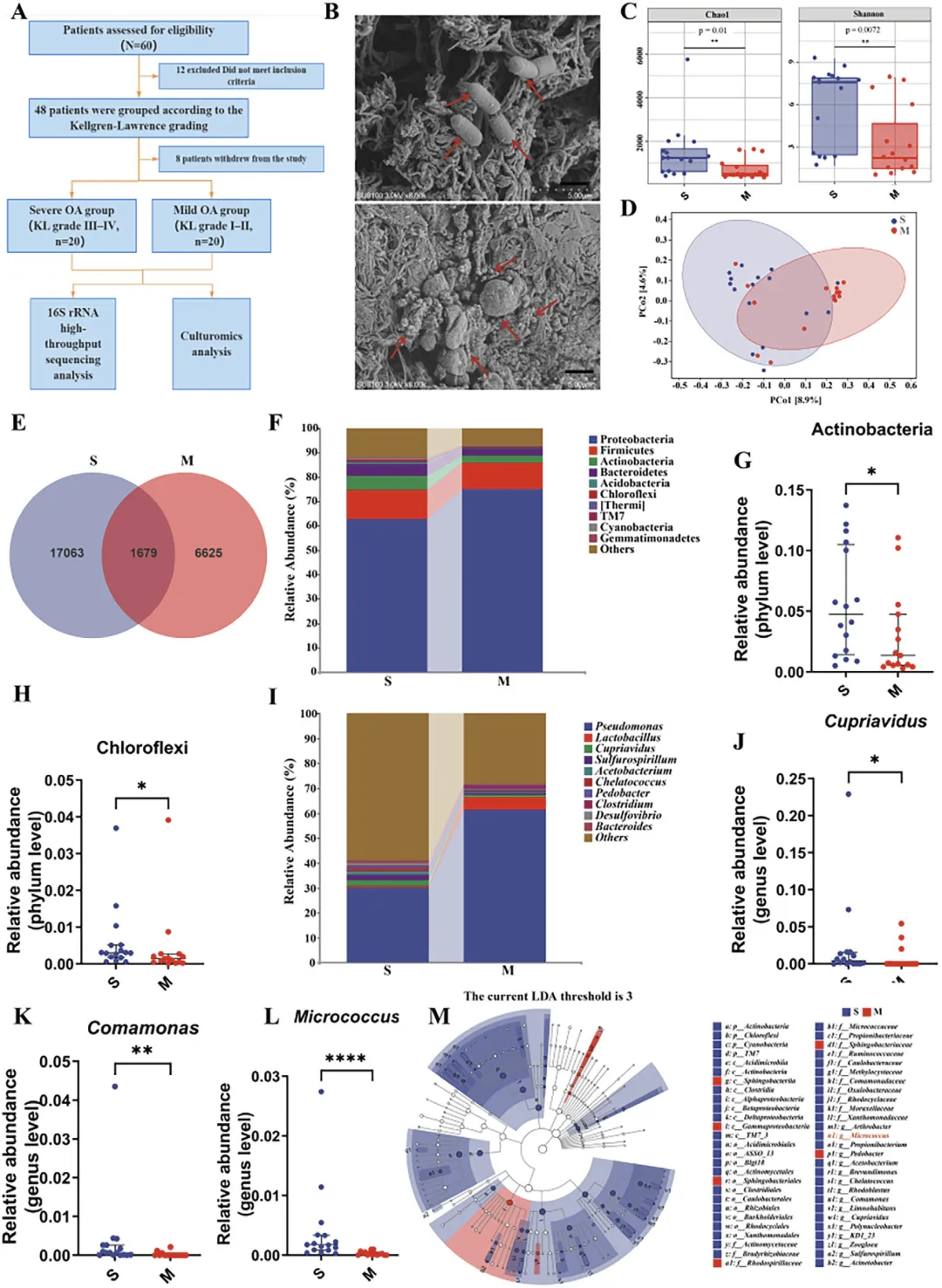
Figure 1 骨关节炎患者入组与滑膜液微生物组分析
这张图围绕骨关节炎患者滑膜液微生物的筛选与鉴定展开,首先展示了 60 例候选患者最终纳入 40 例并按 K-L 分级分为轻度与重度骨关节炎组的流程,通过扫描电镜在滑膜液中观察到球菌与杆菌形态的微生物,直观证明关节腔存在微生物定植;随后的 α 多样性分析显示重度骨关节炎组菌群丰富度与均匀度显著更高,β 多样性分析表明轻、重度患者菌群整体结构存在明显差异,Venn 图呈现两组独有与共有菌群数量差异;门水平分析确定变形菌门、厚壁菌门、放线菌门、拟杆菌门为优势菌门,且重度组放线菌门、绿弯菌门等丰度显著上升,属水平分析发现重度组卡氏菌属、丛毛单胞菌属、微球菌属丰度显著升高,LEfSe 分析进一步筛选出重度组富集的多个差异菌属,整体证明滑膜液微生物组成与骨关节炎严重程度密切相关,微球菌属是重度骨关节炎的关键富集菌属。
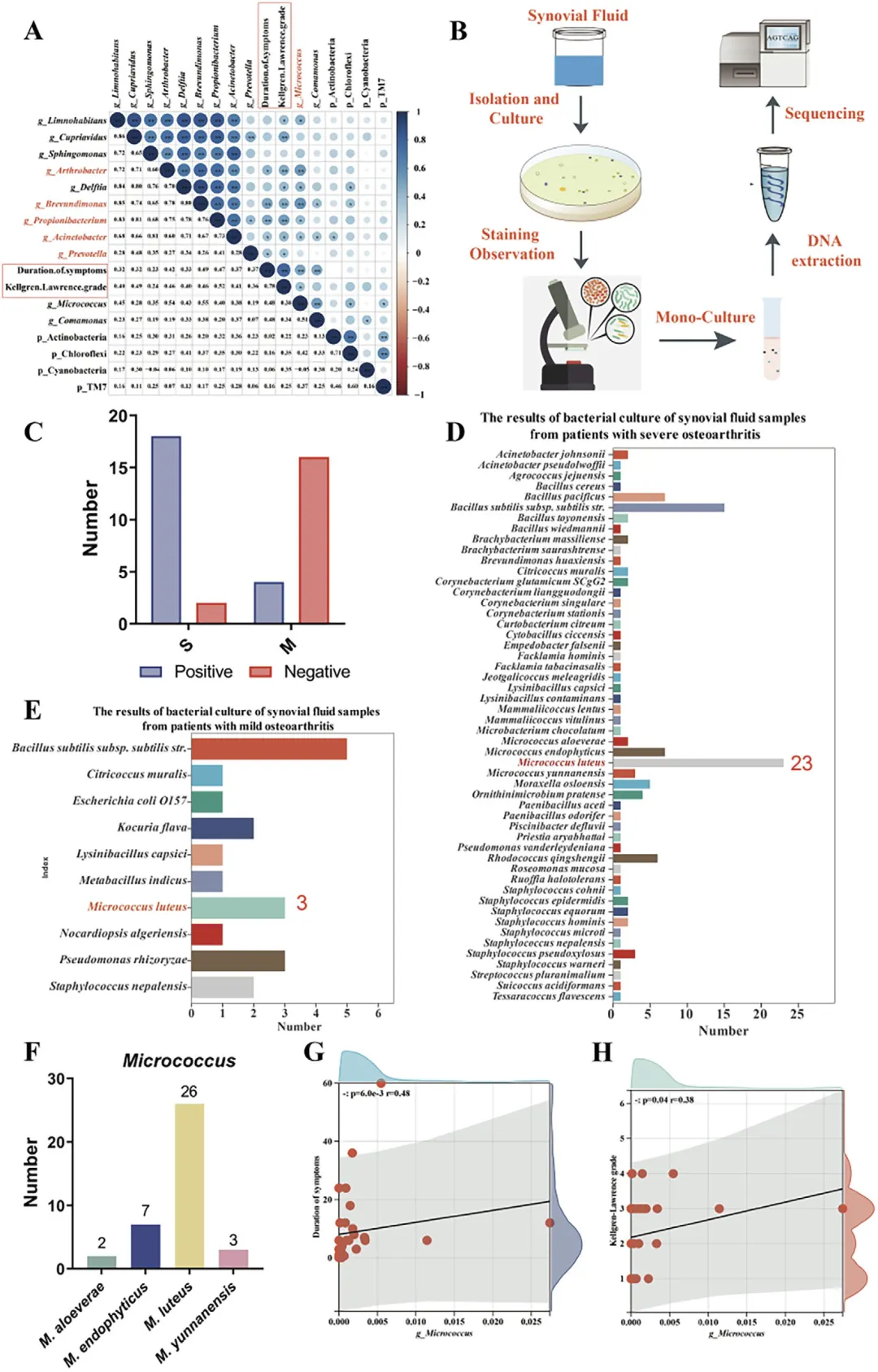
Figure 2 骨关节炎患者滑膜液培养组学分析
这张图聚焦滑膜液微生物的分离培养与关联验证,首先通过相关性热图显示普雷沃氏菌属、不动杆菌属、微球菌属等菌属丰度与骨关节炎严重程度、病程呈显著正相关,明确这些菌属与疾病进展的关联;接着展示滑膜液微生物培养的实验流程,统计发现重度骨关节炎患者滑膜液细菌培养阳性率远高于轻度组,且分离得到的菌株数量与种类更丰富,在所有培养菌株中,藤黄微球菌是分离频率最高的菌株,且主要来自重度骨关节炎患者,进一步的线性相关分析证实微球菌属丰度与骨关节炎临床分级、病程持续时间呈显著正相关,综合测序、培养与关联分析结果,锁定藤黄微球菌为参与骨关节炎进展的核心候选菌株。
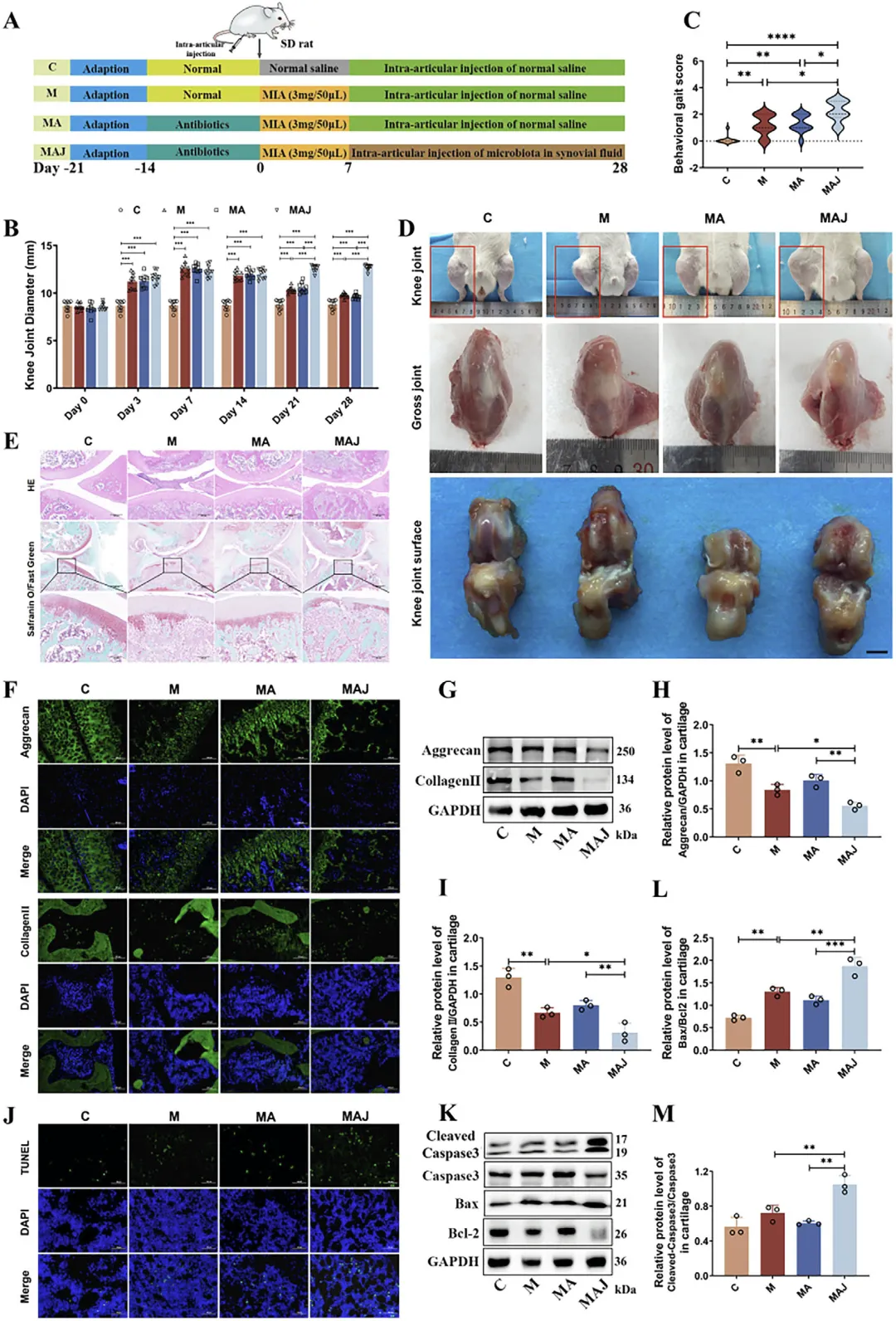
Figure 3 滑膜液微生物加速大鼠膝骨关节炎进展
这张图验证重度骨关节炎患者滑膜液微生物对大鼠骨关节炎的影响,先展示大鼠造模与抗生素预处理、微生物移植的实验设计,结果显示骨关节炎模型大鼠出现关节肿胀、活动受限、步态异常,而移植重度患者滑膜液微生物的大鼠上述症状显著加重;大体观察与组织病理显示移植组大鼠关节充血水肿更严重,软骨表面粗糙、缺损更明显,免疫荧光与蛋白检测发现该组软骨中 Ⅱ 型胶原、蛋白聚糖的表达进一步降低,TUNEL 染色与凋亡蛋白检测显示软骨细胞凋亡显著增加,血清炎症因子与软骨降解标志物水平也显著升高,证明重度骨关节炎患者滑膜液微生物可加剧大鼠关节炎症、软骨破坏与细胞凋亡,加速骨关节炎病理进程。
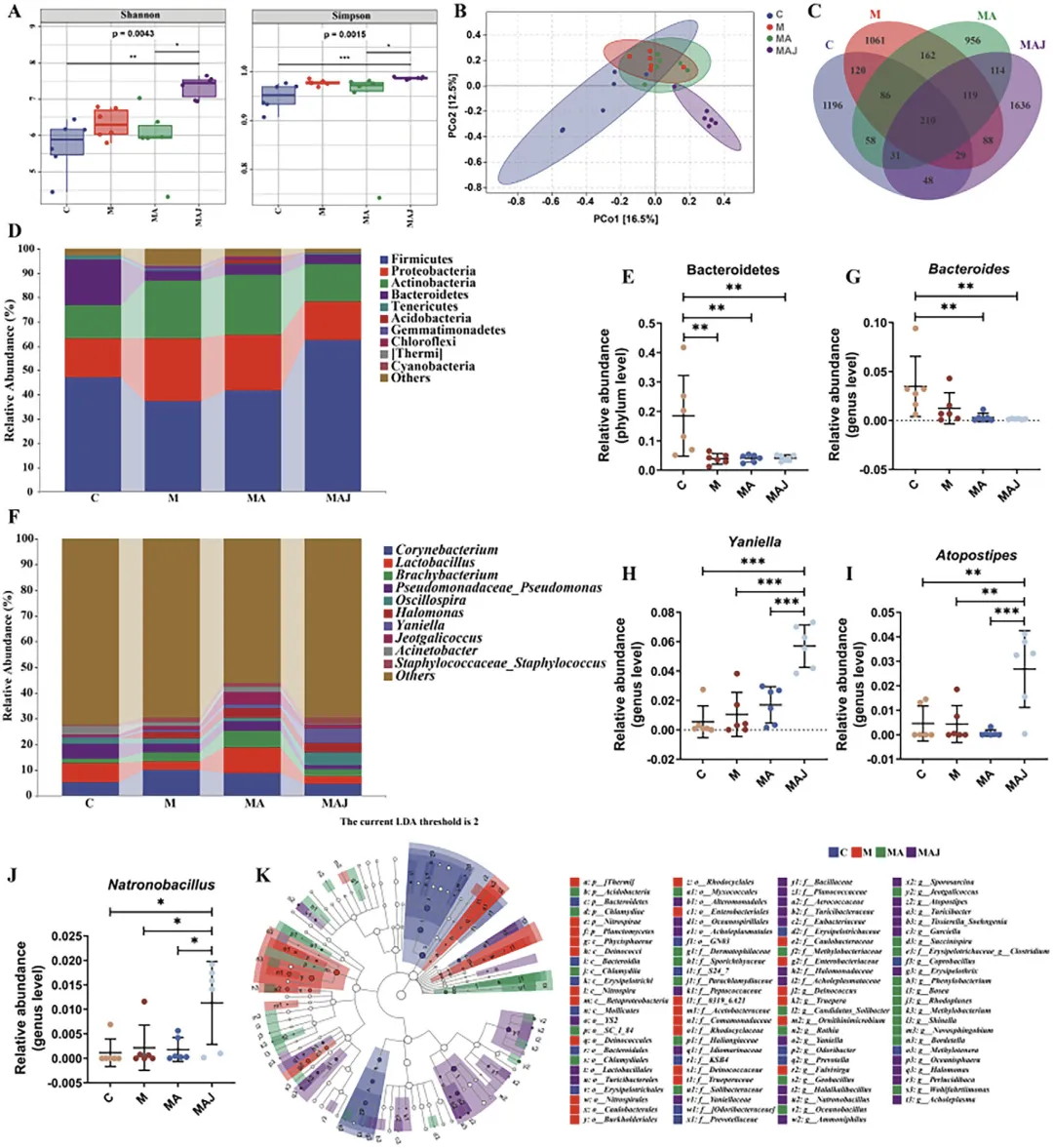
Figure 4 骨关节炎大鼠膝关节腔微生物群落分析
这张图解析微生物移植对大鼠关节腔菌群结构的重塑作用,α 多样性分析显示骨关节炎模型大鼠关节腔菌群多样性高于正常组,移植重度患者滑膜液微生物后多样性进一步提升,β 多样性分析表明该组菌群结构与其他组存在显著差异,Venn 图显示其独有菌群数量最多;门水平优势菌为厚壁菌门、变形菌门等,移植组厚壁菌门丰度显著上升,属水平分析发现移植组拟杆菌属、亚尼氏菌属等潜在致病菌丰度显著升高,LEfSe 分析也证实该组有大量特异性富集菌群,说明移植外源滑膜液微生物会显著改变大鼠关节腔菌群组成,增加致病菌丰度,菌群结构重塑是其加重骨关节炎的重要原因。
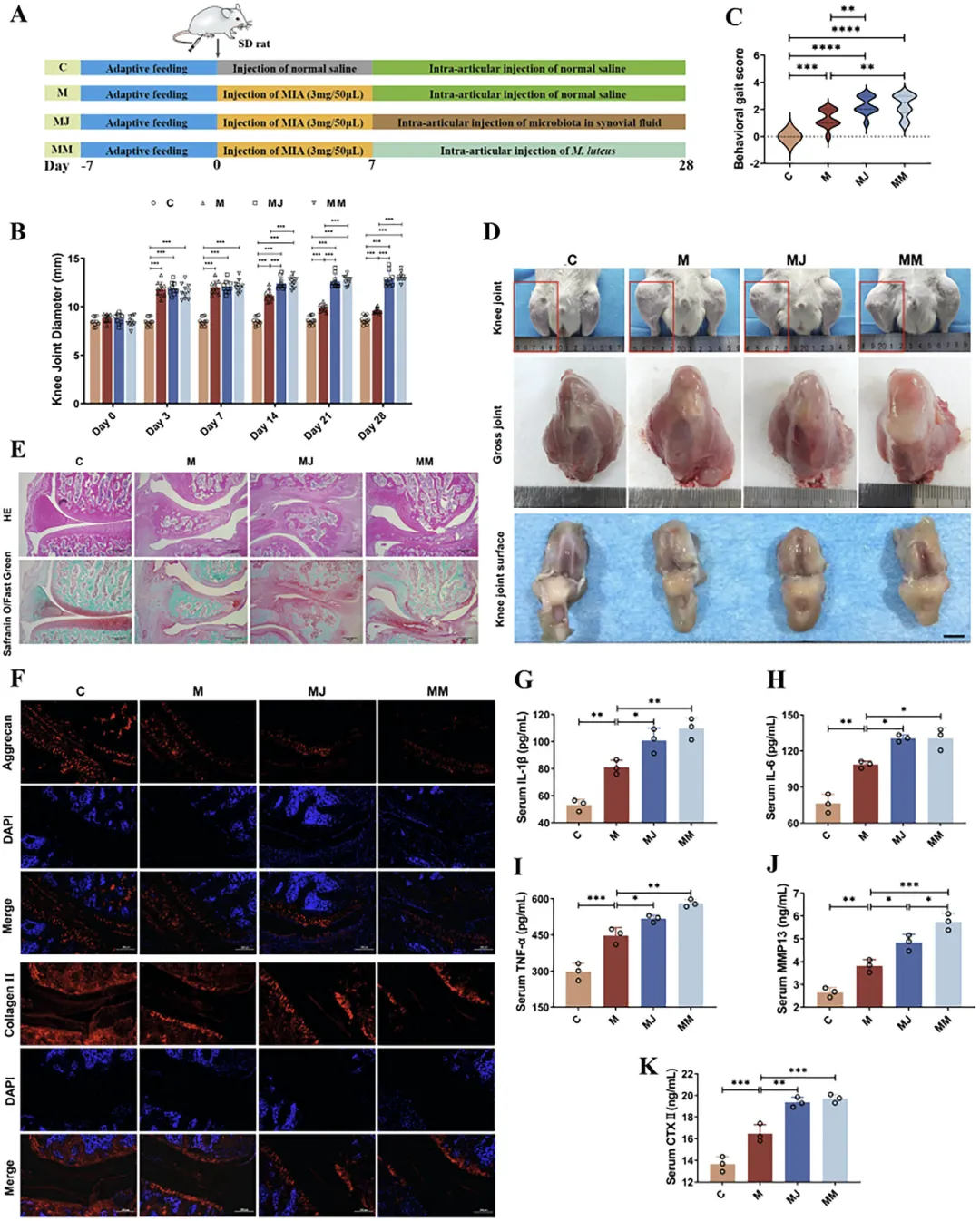
Figure 5 滑膜液来源藤黄微球菌 G18 加重大鼠骨关节炎
这张图直接验证藤黄微球菌 G18 对骨关节炎的致病作用,按照造模与细菌注射的实验设计处理大鼠,结果显示注射藤黄微球菌 G18 的骨关节炎大鼠,关节肿胀、步态障碍程度与移植滑膜液微生物组相近,均显著重于单纯模型组;大体与病理观察发现该组大鼠关节软骨糜烂、缺损更严重,软骨基质大量丢失,免疫荧光检测显示 Ⅱ 型胶原、蛋白聚糖表达大幅降低,血清中 IL-1β、IL-6、TNF-α 等促炎因子以及 MMP13、CTX-II 等软骨降解标志物水平显著升高,明确藤黄微球菌 G18 可独立诱发关节炎症、促进软骨基质降解,是驱动骨关节炎恶化的关键致病菌。
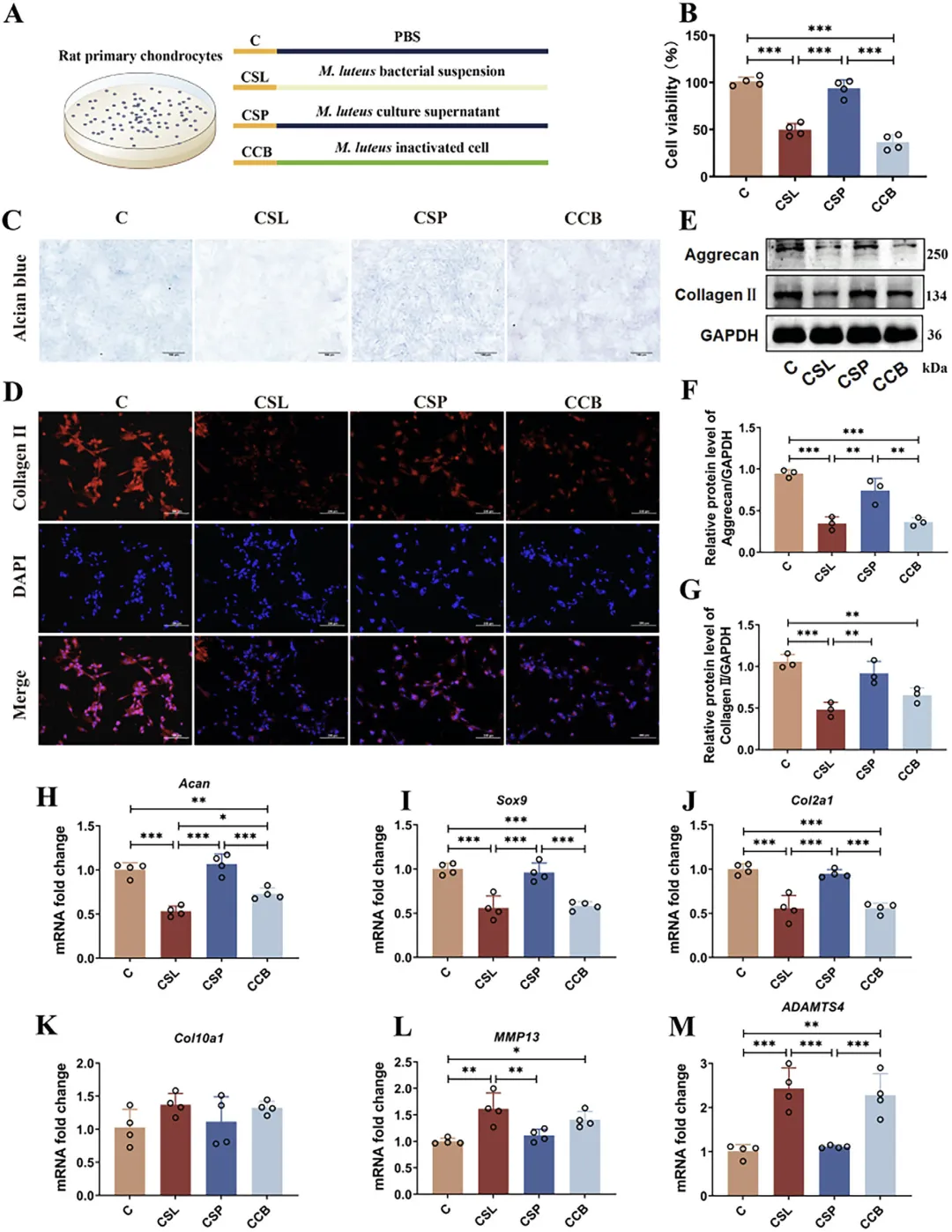
Figure 6 藤黄微球菌 G18 通过菌体成分损伤软骨细胞
这张图探究藤黄微球菌 G18 损伤软骨细胞的关键效应成分,将原代软骨细胞分别与活菌、菌上清、热灭活菌共培养,结果显示活菌与热灭活菌均显著降低软骨细胞活力,而菌上清影响较小,阿利新蓝染色与免疫荧光显示活菌与热灭活菌组软骨细胞酸性蛋白聚糖、Ⅱ 型胶原含量明显减少,蛋白与基因检测证实这两组细胞中软骨合成相关基因 Acan、Sox9、Col2a1 显著下调,降解相关基因 Col10a1、Mmp13、Adamts4 显著上调,说明藤黄微球菌 G18 的致病作用不依赖活菌状态,其菌体细胞壁结构成分是破坏软骨细胞代谢平衡、抑制基质合成并促进降解的关键物质。
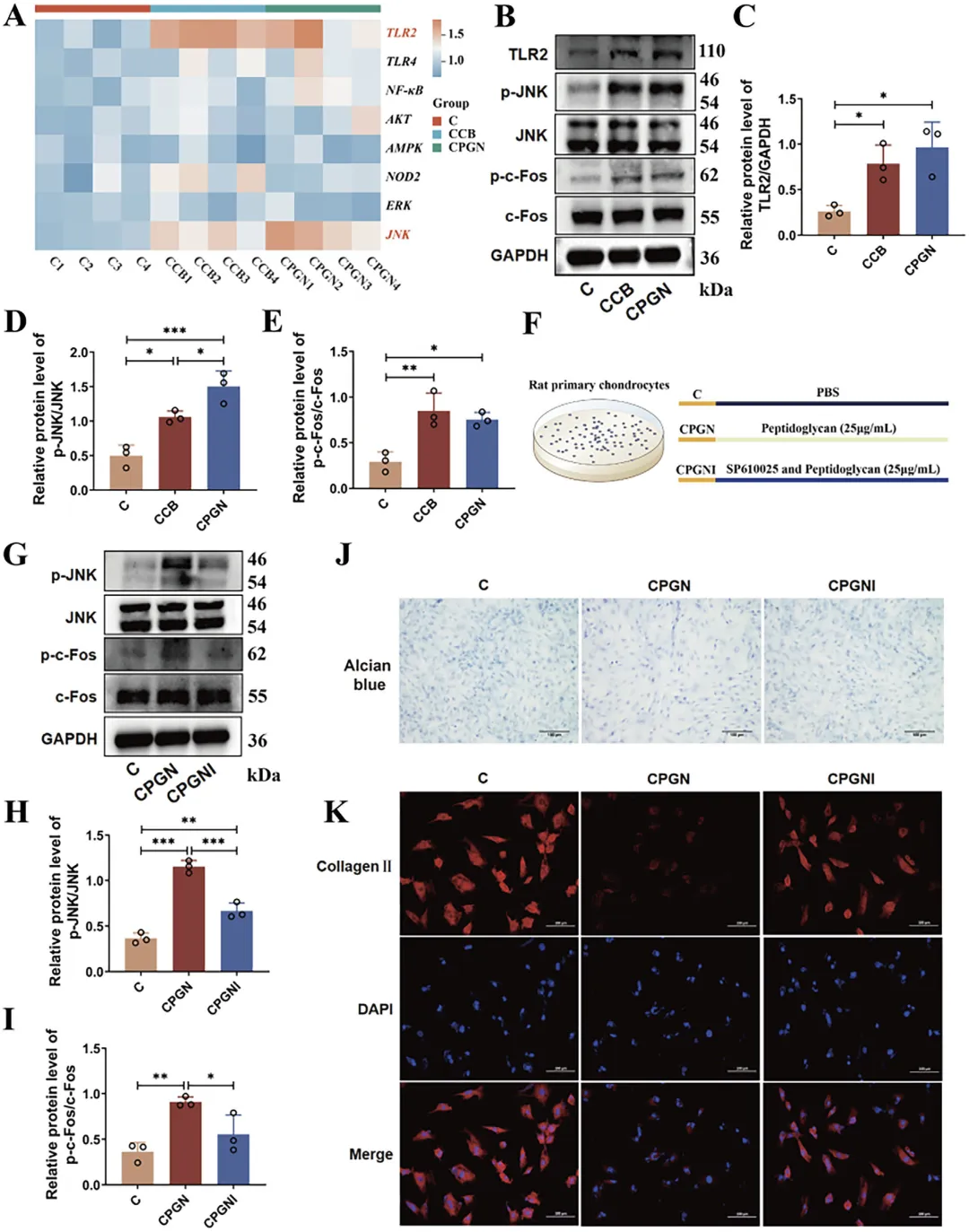
Figure 7 藤黄微球菌肽聚糖通过 TLR2/JNK/AP-1 通路扰乱软骨细胞代谢
这张图揭示藤黄微球菌致病的分子通路,首先检测发现热灭活菌与肽聚糖处理后,软骨细胞 TLR2、JNK 通路基因显著上调,蛋白检测证实 TLR2、磷酸化 JNK、磷酸化 c-Fos 表达显著升高,证明肽聚糖可激活 TLR2/JNK/AP-1 通路;随后加入 JNK 抑制剂 SP600125 干预,结果显示抑制剂可显著降低磷酸化 JNK 与 c-Fos 水平,恢复软骨细胞蛋白聚糖与 Ⅱ 型胶原的表达,逆转肽聚糖对软骨细胞合成与降解基因的调控失衡,明确藤黄微球菌的肽聚糖通过激活 TLR2/JNK/AP-1 信号轴,破坏软骨细胞代谢稳态,是其诱导软骨损伤的核心分子机制。
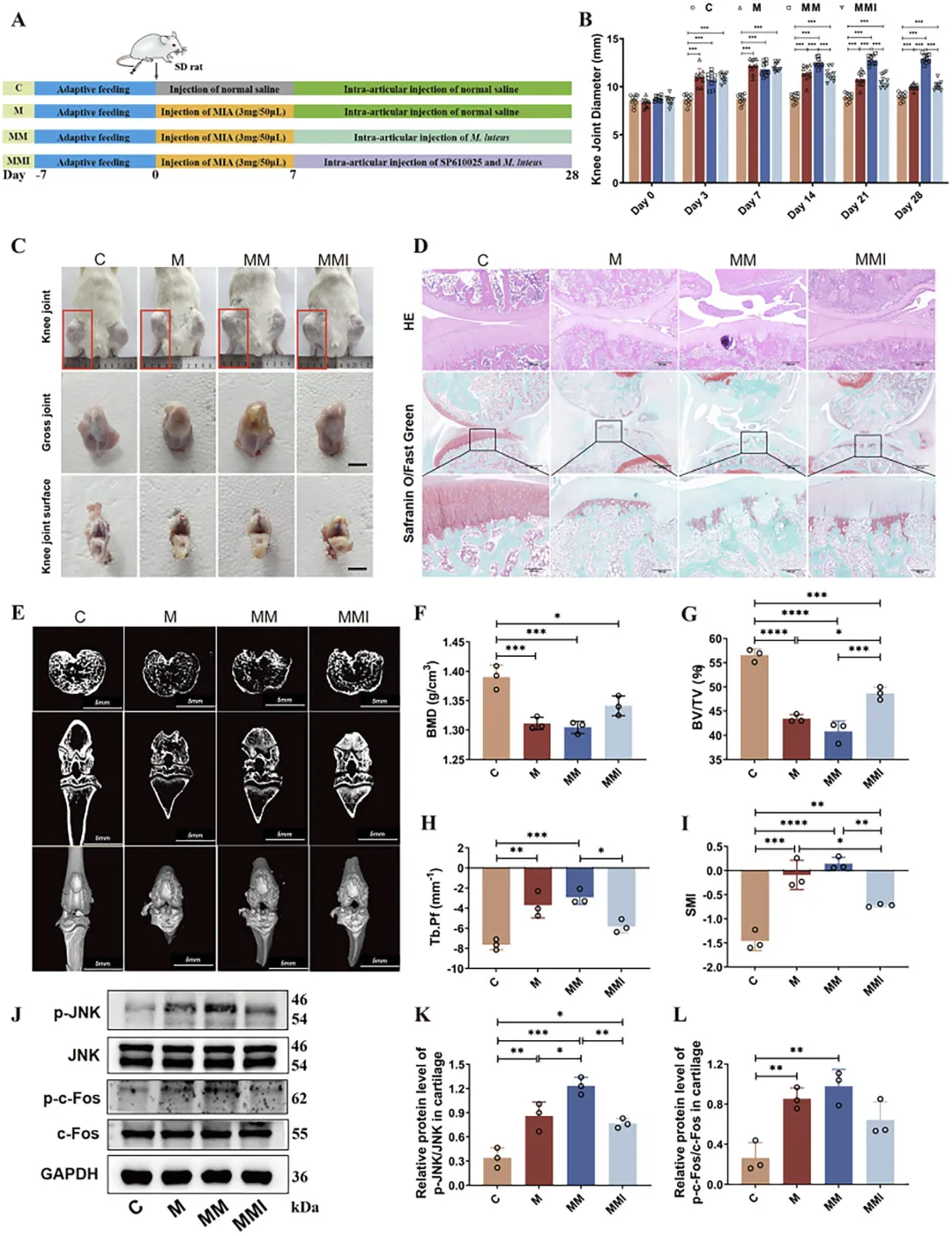
Figure 8 抑制 JNK 通路缓解藤黄微球菌 G18 诱导的骨关节炎加重
这张图在动物体内验证 JNK 通路的关键作用,对藤黄微球菌 G18 干预的骨关节炎大鼠注射 JNK 抑制剂,结果显示抑制剂可显著减轻大鼠关节肿胀与步态损伤,大体与病理观察发现软骨结构完整性、基质含量得到明显保护,Micro-CT 显示大鼠骨密度、骨体积分数等骨微结构指标显著改善,骨破坏参数降低;蛋白检测证实抑制剂可有效降低软骨中磷酸化 JNK 与 c-Fos 的表达,血清炎症因子与软骨降解标志物水平也显著下降,体内实验进一步证实藤黄微球菌 G18 通过激活 JNK/AP-1 通路加重骨关节炎,抑制该通路可有效阻断其致病作用,缓解疾病进展。
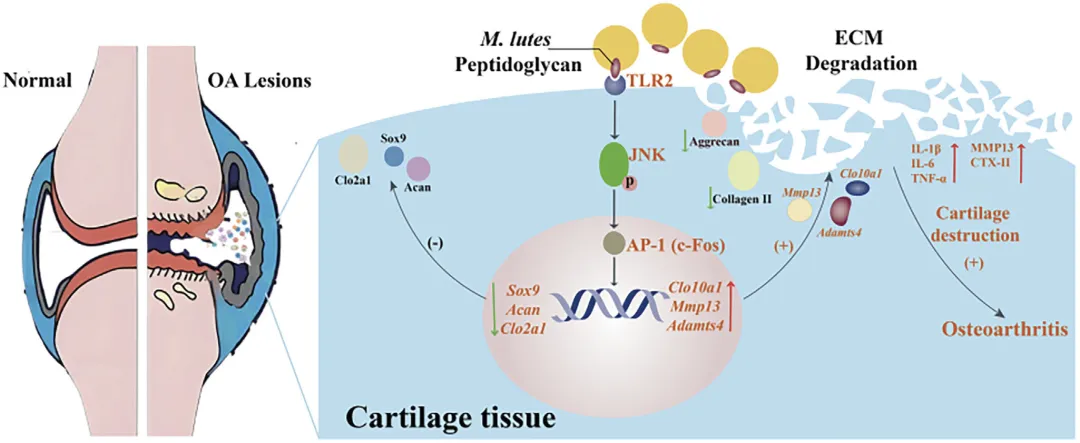
Figure 9 滑膜液藤黄微球菌 G18 在骨关节炎软骨退变中的作用模式图
这张图以模式图形式总结全文核心机制,正常关节软骨细胞维持基质合成与降解的平衡,而骨关节炎状态下,滑膜液中的藤黄微球菌 G18 释放细胞壁肽聚糖,肽聚糖结合软骨细胞表面的 TLR2 受体,激活下游 JNK/AP-1 信号通路,进而下调 Sox9、Acan、Col2a1 等软骨合成相关基因,上调 Col10a1、Mmp13、Adamts4 等降解相关基因,打破软骨细胞代谢平衡,导致细胞外基质合成减少、降解加剧,最终引发软骨破坏、骨关节炎持续进展,清晰呈现了微生物 — 信号通路 — 软骨损伤的完整调控链条。
本研究首次系统证明人类膝关节腔存在稳定微生物群落,彻底颠覆关节腔无菌的传统认知;滑膜液微生物多样性与骨关节炎进展呈正相关,藤黄微球菌 G18 是驱动疾病恶化的核心微生物;其通过细胞壁肽聚糖激活软骨细胞 TLR2/JNK/AP-1 信号通路,打破细胞外基质合成与降解平衡,诱发炎症与软骨破坏,加速骨关节炎进程;该研究重塑骨关节炎发病机制认知,为基于微生物的诊断标志物开发与靶向治疗提供全新理论与实验基础。
局限性:临床样本量较小,培养组学条件有限,未全面解析微生物 - 宿主免疫互作网络。展望:扩大多中心临床队列,优化微生物培养技术,深入探索菌群 - 免疫 - 炎症调控网络,开发靶向藤黄微球菌与 JNK 通路的骨关节炎干预策略。
文章来源: Chen T, Zeng Q, Xu T, Qi X, Li K, Wei J, Hao L. Synovial Fluid-derived Micrococcus Luteus G18 Exacerbates Osteoarthritis Progression by Promoting Chondrocyte Degradation via TLR2/JNK/AP-1 Signaling Pathway. Adv Sci (Weinh). 2026 Jan;13(6):e14220. doi: 10.1002/advs.202514220. Epub 2025 Nov 16. PMID: 41243495; PMCID: PMC12866835.

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究