南昌大学食品学院特聘研究员李志鹏老师课题组:葡甘露聚糖通过肠道菌群-代谢物-谷氨酸能突触轴改善高脂饮食诱导的认知功能障碍
- 2026-05-06 06:21:52

长期吃得太油腻真的会“变笨”吗?南昌大学食品学院特聘研究员李志鹏老师课题组在国际期刊International Journal of Biological Macromolecules发表了题为《Supplementation of glucomannans ameliorate high-fat diet-induced cognitive impairment via a gut microbiota-metabolite-glutamatergic synapse axis》的研究论文,为预防和改善与肥胖相关的记忆力下降提供了全新的膳食干预思路。

研究背景
长期的高脂饮食不仅会导致肥胖,还会诱发大脑海马区的神经损伤,从而增加认知功能障碍甚至阿尔茨海默病的风险。葡甘露聚糖(GMs)作为一种优质的水溶性膳食纤维,广泛存在于铁皮石斛、魔芋和芦荟等植物中。虽然它们的基本结构相似,但由于乙酰化程度和成分比例的不同,对大脑的保护效果也存在差异。该研究旨在探究这些不同来源的多糖是如何跨越肠道,通过影响全身代谢来“拯救”大脑的。

结果与讨论
01
缓解高脂饮食诱导的认知衰退与焦虑样行为
通过构建长期高脂饮食(HFD)小鼠模型,研究团队评估了铁皮石斛多糖(DOP)、魔芋多糖(KGM)和芦荟多糖(AVP)的干预效果。在Y迷宫和旷场实验等行为学测试中可以直观地看到,补充葡甘露聚糖大幅提升了小鼠的空间工作记忆,增加了自发交替的正确率,并有效缓解了HFD带来的焦虑样情绪,激发了小鼠的探索活力。
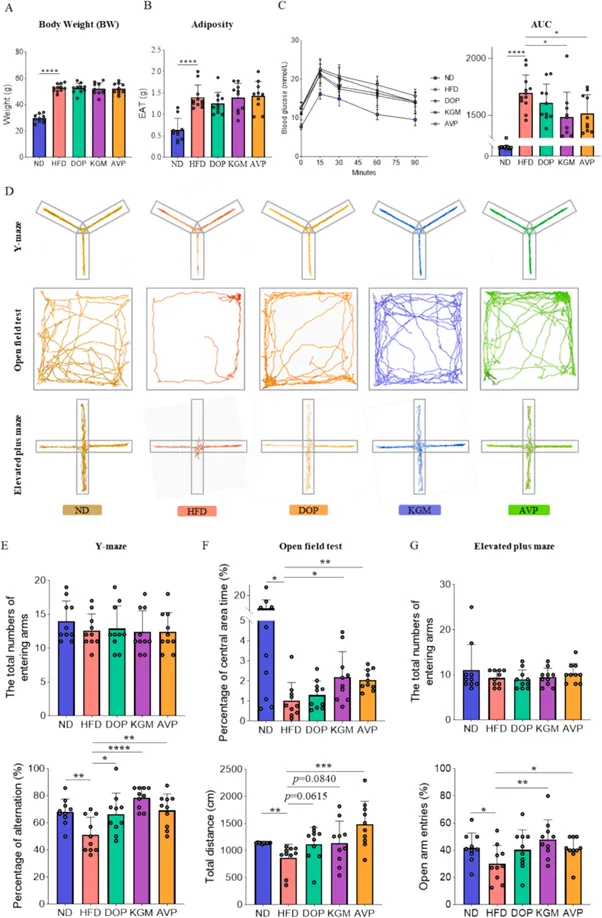
图 葡甘聚糖改善高脂饮食诱导的认知功能障碍和焦虑。(A)体重;(B)附睾脂肪组织重量;(C)口服葡萄糖耐量试验(OGTT)曲线及曲线下面积(AUC);(D)Y-迷宫实验中的总进臂次数和自发交替百分比;(E)旷场实验中的中心区域停留时间百分比和总移动距离;(F)高架十字迷宫中的总进臂次数和进入开放臂次数比例
02
葡甘露聚糖减轻海马神经元与突触损伤
组织学观察发现,高脂饮食会导致小鼠海马CA1和CA3区神经元出现形态萎缩等结构改变。而多糖干预可改善这些神经元的形态,并提高了神经元标记物(NeuN)的表达水平。此外,多糖还提升了突触前后关键蛋白(SYN-1和PSD95)的丰度,减轻了突触结构的物理损伤。
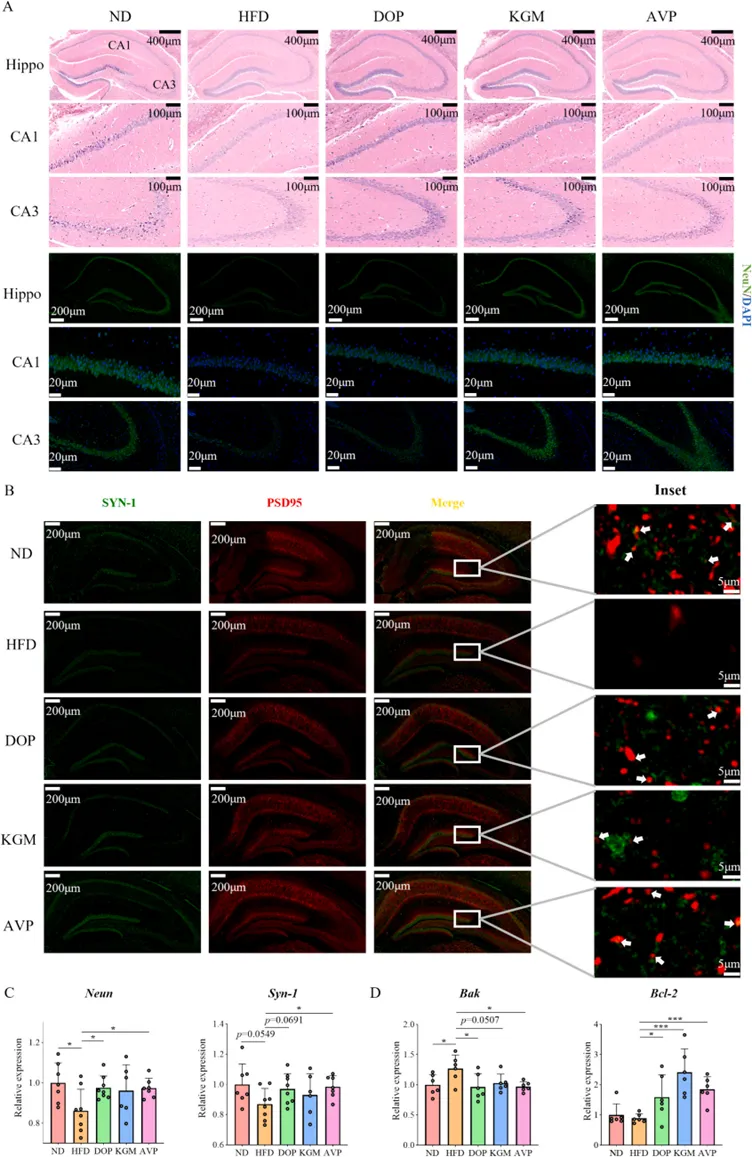
图 组织病理学分析揭示葡甘露聚糖减轻HFD诱导的海马神经元损伤。(A)H&E染色及海马(包括CA1和CA3区)NeuN免疫荧光染色的代表性图像;(B)PSD95(红色)和SYN-1(绿色)的免疫荧光染色;(C)Neun和Syn-1的表达水平;(D)Bak和Bcl-2的表达水平。
03
葡甘露聚糖逆转海马转录组变化并激活谷氨酸能突触通路
基因层面的分析显示,多糖干预能够有效逆转高脂饮食引起的大部分海马基因表达异常。通路富集分析进一步指出,DOP、KGM和AVP共同上调了与“谷氨酸能突触”以及“突触可塑性调节”密切相关的基因网络。
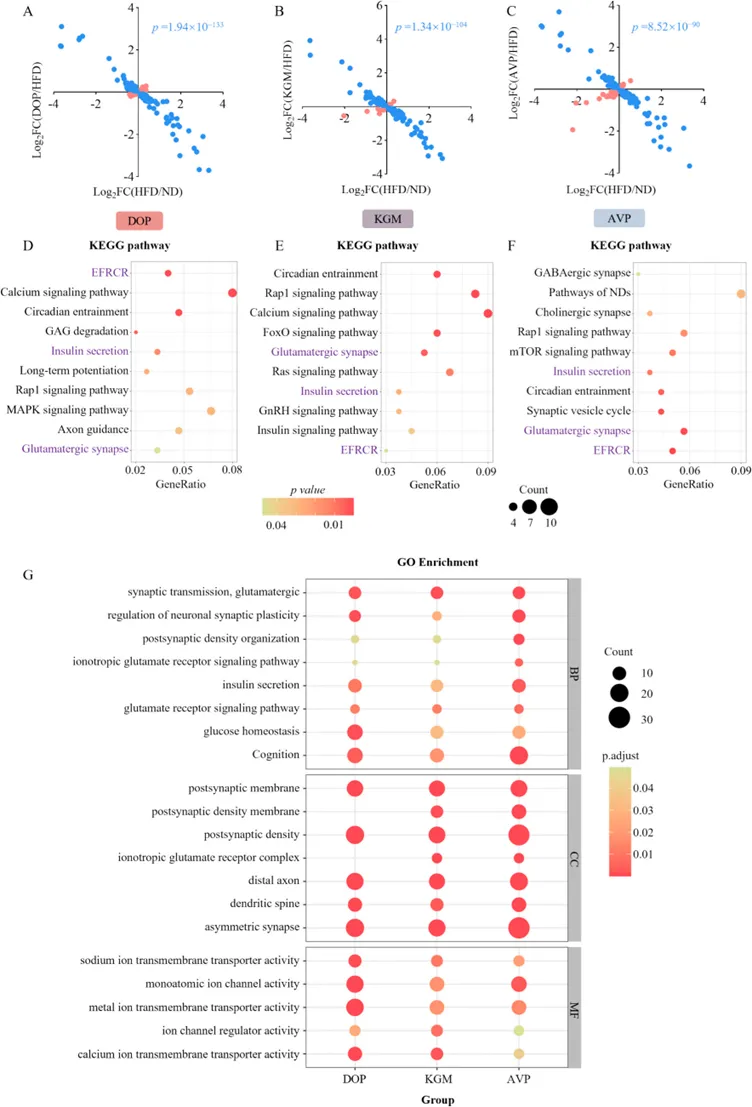
图 葡甘聚糖逆转HFD诱导的转录组变化并促进海马谷氨酸能突触信号传导。(A–C)散点图展示了各葡甘露聚糖(GMs)的调控作用与HFD对基因表达的调控作用之间的关系;(D–F)分别展示了被DOP、KGM和AVP上调基因的KEGG通路富集分析(高亮显示的通路为三种GMs共同富集的通路);(G)分别展示了被DOP、KGM和AVP上调基因的GO富集分析。
04
葡甘露聚糖增强突触受体及下游信号传导
多糖不仅增加了突触囊泡转运蛋白VGLUT1与支架蛋白PSD95的表达密度,还上调了NMDA受体(Grin1、Grin2b)及其下游激酶CaMKII的表达水平。这有助于恢复神经元之间突触信号的传递效率。
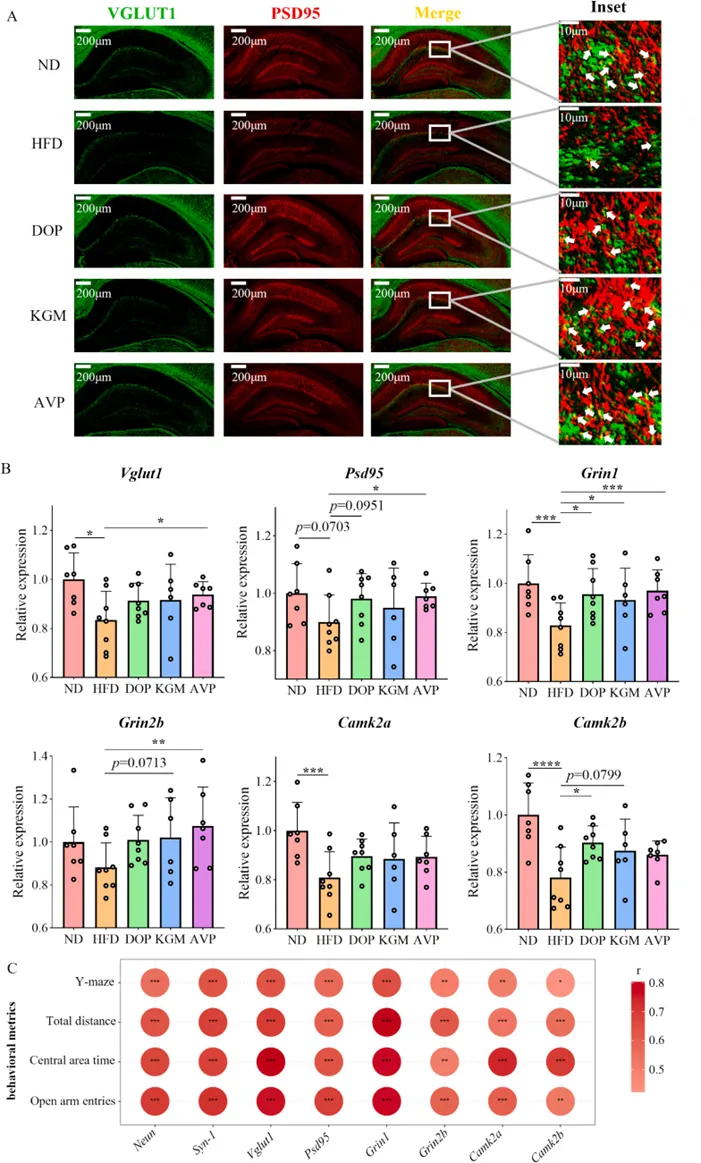
图 葡甘聚糖缓解高脂饮食(HFD)诱导的小鼠海马谷氨酸能突触损伤,并增强NMDA受体信号传导。(A)小鼠海马中PSD95(红色)和VGLUT1(绿色)的免疫荧光染色;(B)海马中Vglut1、Psd95、Grin1、Grin2b、Camk2a和Camk2b的表达水平;(C)谷氨酸能突触相关基因表达水平与行为学指标之间的Spearman相关性分析。
05
多糖调控通路与阿尔茨海默病(AD)病理学的相关性
研究人员将小鼠数据与公共数据库中人类阿尔茨海默病患者的海马体测序数据进行了对比,发现在AD患者大脑中处于抑制状态的突触囊泡循环、谷氨酸受体复合物等通路,在小鼠模型中可通过多糖干预得到激活,显示出一定的转化医学关联性。
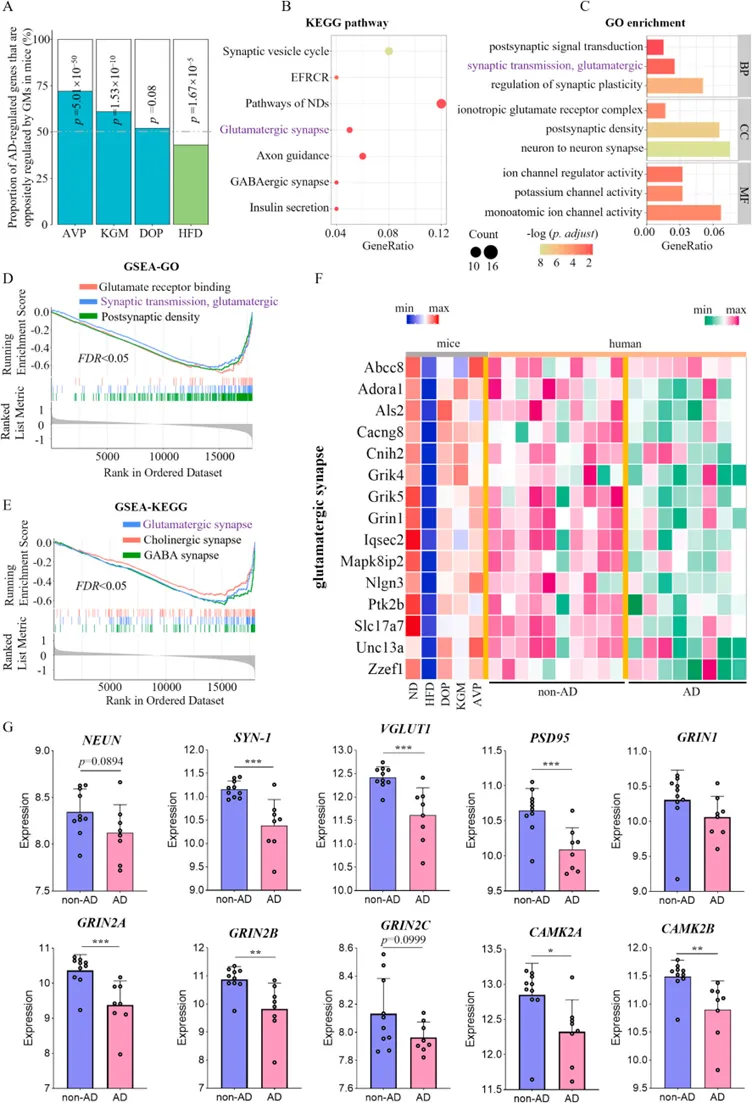
图 人类海马转录组分析显示,葡甘露聚糖调节的通路与阿尔茨海默病(AD)的病理生理学相关。(A)被AD调节但在小鼠中被葡甘聚糖(GMs)反向调节的基因比例;(B)AD组与对照组差异表达基因的KEGG富集分析;(C)AD组与对照组差异表达基因的GO富集分析;(D)GSEA;(E)谷氨酸能突触相关基因表达情况的热图;(F)人类海马中NEUN、SYN-1、VGLUT1、PSD95、GRIN1、GRIN2A、GRIN2B、GRIN2C、CAMK2A和CAMK2B的表达水平。
06
葡甘露聚糖重塑肠道微生态
多糖干预改变了小鼠肠道菌群的组成结构。特别是芦荟多糖(AVP)显著提升了肠道菌群的多样性。多糖干预增加了双歧杆菌(Bifidobacterium)和毛螺菌属(Lachnoclostridium)等益生菌的相对丰度,并抑制了梭菌属(Clostridium)的生长。
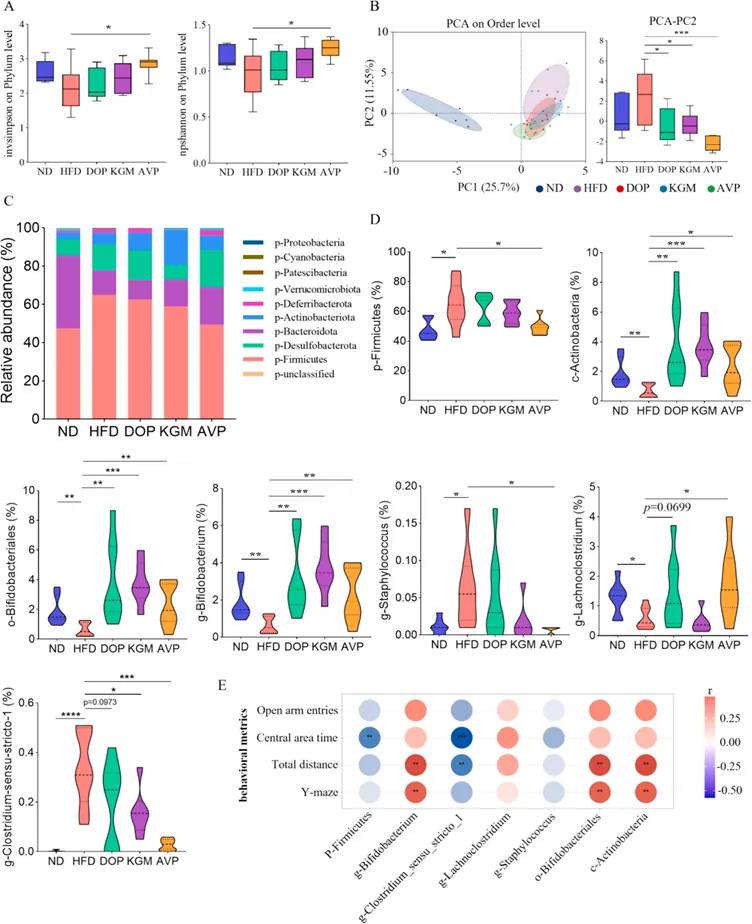
图葡甘聚糖调节 HFD 诱导的认知功能障碍小鼠的肠道微生物群。(A)门水平的InvSimpson和npShannon指数;(B)目水平的主成分分析(PCA);(C)门水平的相对丰度;(D)厚壁菌门(Firmicutes)、放线菌门(Actinobacteria)、双歧杆菌属(Bifidobacterium)、葡萄球菌属(Staphylococcus)、毛螺菌属(Lachnoclostridium)及狭义梭菌属-1(Clostridium-sensu-stricto-1)的相对丰度;(E)肠道微生物丰度与小鼠行为学指标之间的相关性分析。
07
葡甘露聚糖干预调节血清代谢物谱
多糖干预组的血清代谢图谱与高脂饮食模型组存在明显空间分离,即,多糖改变了多种代谢物的丰度,这些差异代谢物主要富集在精氨酸生物合成、丙氨酸、天冬氨酸和谷氨酸代谢等通路中。
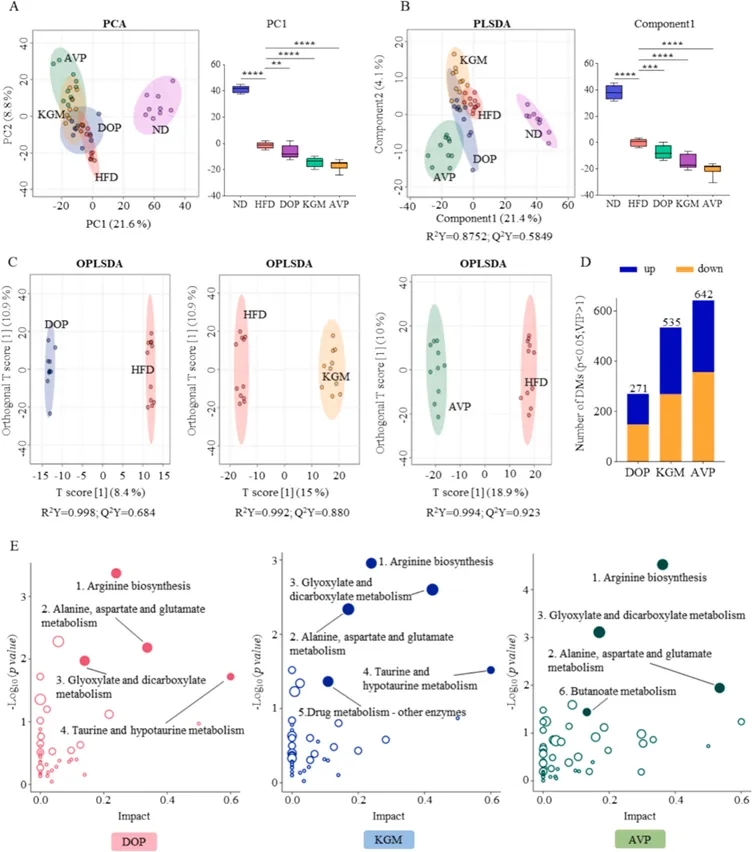
图 葡甘聚糖调节HFD诱导的认知功能障碍小鼠的血清代谢组。(A-B)各组小鼠血清代谢物谱的主成分分析(PCA,图A)和偏最小二乘判别分析(PLS-DA,图B);(C)OPLS-DA评分图展示了各葡甘露聚糖(GM)治疗组与HFD组之间显著差异的血清代谢组谱;(D)在DOP、KGM和AVP组中鉴定出的差异代谢物数量(FDR<0.05);(E)分别对DOP、KGM和AVP组的差异代谢物进行的KEGG通路富集分析。
08
多组学网络整合揭示“肠-脑”调控机制
通过整合肠道菌群、血清代谢物、海马转录组和行为学数据的网络分析发现,多糖的作用路径主要遵循“改变肠道微生态——调节血液循环代谢物——影响海马区谷氨酸能突触基因表达——改善行为学表型”这一级联方向。
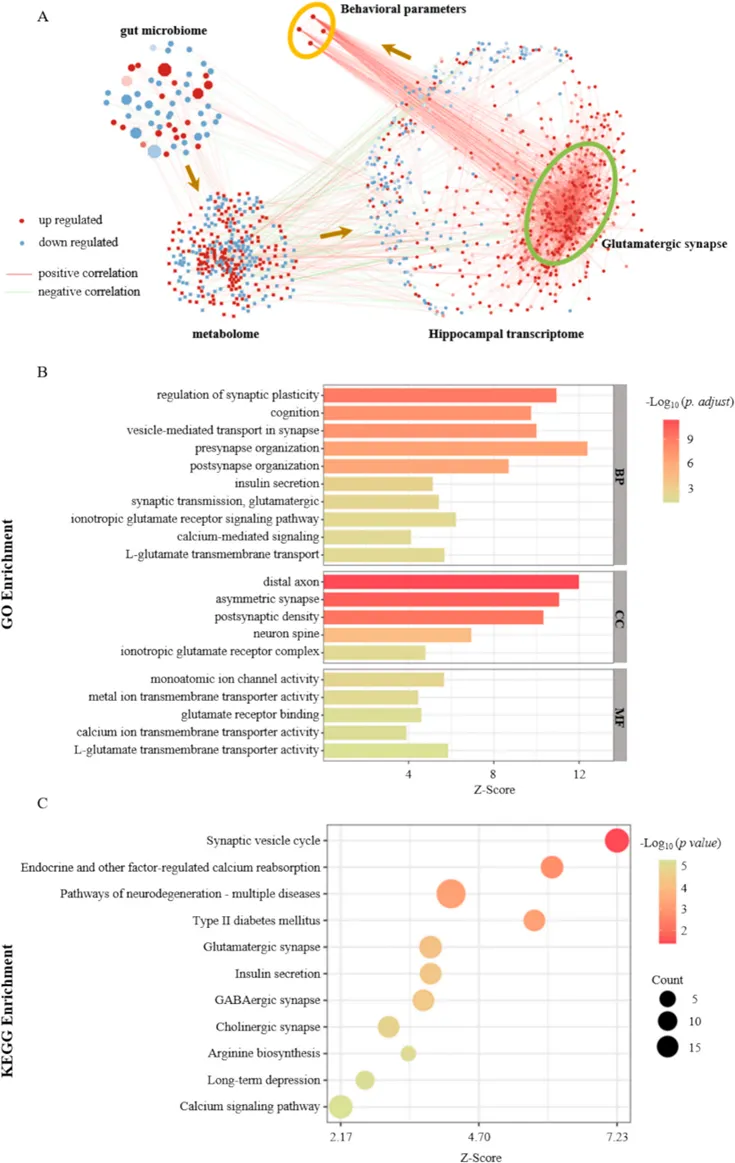
图 多组学网络分析揭示了葡甘露聚糖(GMs)改善高脂饮食(HFD)诱导的小鼠认知功能的潜在机制。(A)多组学关联网络图;(B–C)对海马转录组网络子网络中的基因进行的GO功能富集分析(B)和KEGG通路富集分析(C)。
09
数据驱动锁定NAG与NAA为核心介质
在对比粪便与血清的双重代谢数据后,研究筛选出N-乙酰-L-谷氨酸(NAG)和N-乙酰神经氨酸(NAA)两种核心代谢物。这两种物质在多糖干预后显著增加,并且与小鼠行为学指标的改善呈现正相关。
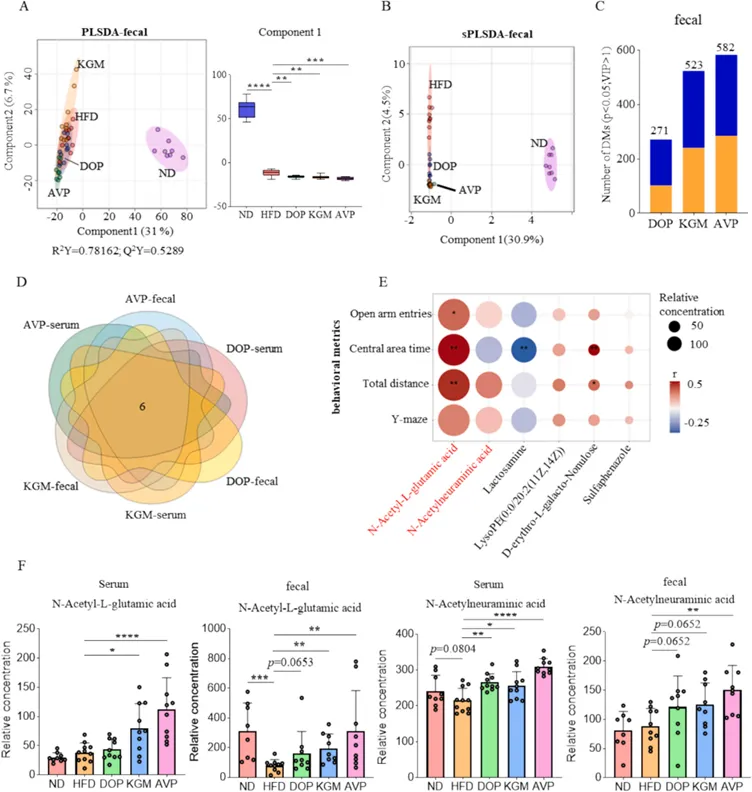
图 整合粪便与血清代谢组学分析,鉴定出 NAG 和 NAA 为潜在的核心介导因子。(A)粪便代谢物谱的PLS-DA评分图;(B)粪便代谢物谱的sPLS-DA评分图;(C)DOP、KGM和AVP组粪便中差异代谢物的数量(p < 0.05,VIP > 1);(D)差异代谢物的韦恩图(Venn diagram);(E)交集代谢物与行为学指标之间的Spearman相关性分析;(F)血清和粪便中N-乙酰-L-谷氨酸(NAG)和N-乙酰神经氨酸(NAA)的相对浓度。
10
核心代谢物单独干预改善肥胖小鼠认知与神经元损伤
为验证上述推测,研究直接对ob/ob肥胖小鼠补充了单体代谢物NAG和NAA。行为学测试证实,这两种代谢物能够提升肥胖小鼠的自发交替正确率和认知指数,并有效减轻海马神经元的形态萎缩。
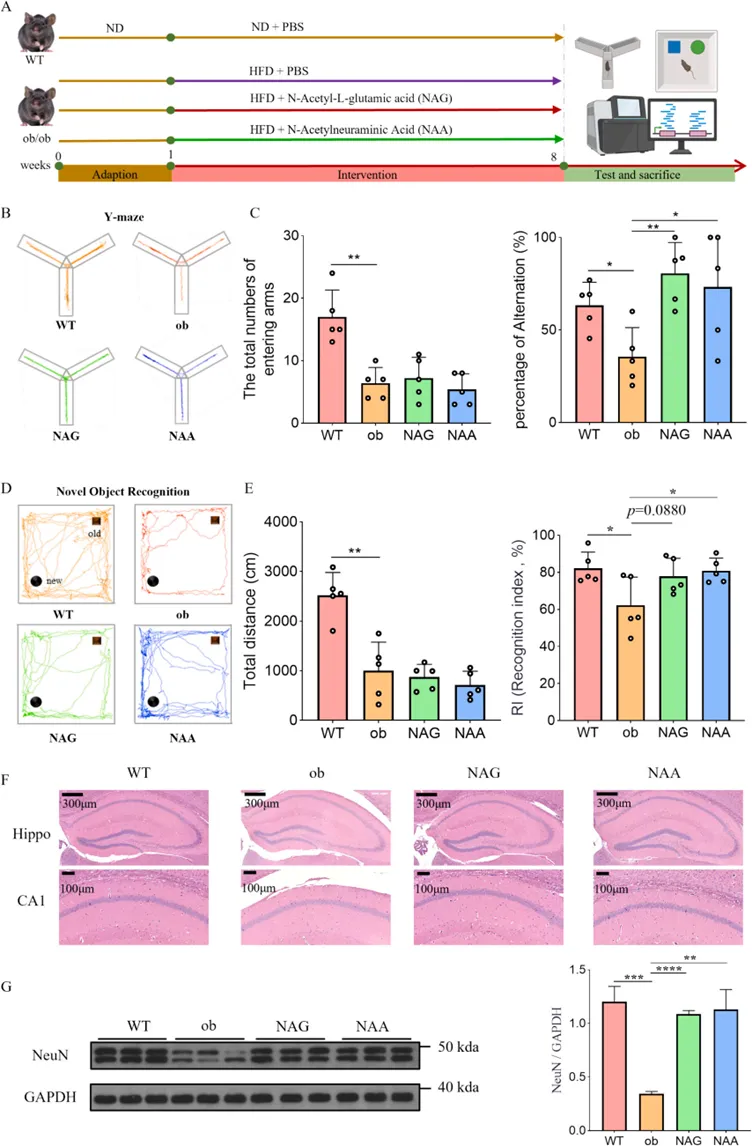
图 N-乙酰-L-谷氨酸(NAG)和N-乙酰神经氨酸(NAA)缓解ob/ob小鼠的认知功能障碍和神经元损伤。(A)实验设计流程图;(B)Y-迷宫实验中小鼠的运动轨迹图;(C)Y-迷宫实验中的总进臂次数和自发交替百分比(n=5);(D)新物体识别实验中小鼠的运动轨迹图;(E)新物体识别实验中的总移动距离和识别指数(%)(n=5);(F)海马(包括CA1区)的H&E染色;(G)通过Western blot检测的海马中NeuN蛋白的表达水平(n=3)。
11
NAG与NAA促进大脑谷氨酸能突触信号传导
NAG和NAA的引入同样逆转了肥胖引发的基因表达异常,靶向上调了突触前后核心蛋白(VGLUT1与PSD95),进一步证实了其对谷氨酸能突触信号传导网络的促进作用。
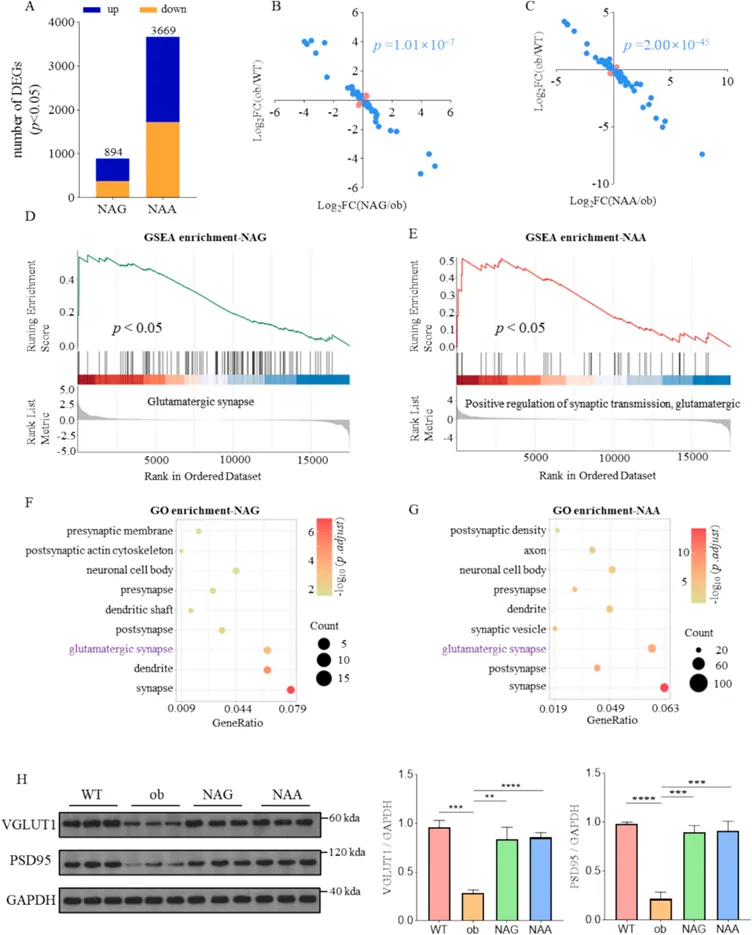
图 N-乙酰-L-谷氨酸(NAG)和 N-乙酰神经氨酸(NAA)促进肥胖小鼠海马中的谷氨酸能突触信号传导。(A)海马中差异表达基因的数量(n = 5);(B–C)散点图展示了两种代谢物的调控作用与肥胖模型对海马基因表达调控作用之间的关系;(D–E)基因集富集分析(GSEA);(F–G)NAG/NAA上调基因的GO富集分析;(H)通过Western blot检测的海马中VGLUT1和PSD95蛋白的表达水平(n = 3)。

结论与展望
研究系统证实,膳食补充天然葡甘露聚糖可通过“肠道菌群-代谢物-谷氨酸能突触”轴,缓解由高脂饮食诱导的神经及认知功能减退。结果表明,多糖分子中较高的乙酰化程度及单糖比例与其神经保护活性具有一定的相关性,同时鉴定出N-乙酰-L-谷氨酸(NAG)与N-乙酰神经氨酸(NAA)作为连接肠道与脑对话、改善肥胖相关认知障碍的潜在活性小分子。上述发现为未来开发靶向肠脑轴的营养干预策略提供了客观的基础数据及参考方向。
(请点击标题查看)
分子对接与分子动力学黄酮类化合物
食品感官科学与分析农产品贮藏与加工
肉与肉制品蛋与蛋制品水产品
奶及奶制品豆及豆制品果蔬及果蔬制品
大米及米制品
炎症性肠病糖尿病肝病神经疾病
(请点击标题查看)
(请点击学者姓名查看)


在线投稿平台链接:https://www.wjx.top/jq/85151447.aspx
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅仅是出于学术交流和传播信息的需要,并不意味着代表本平台观点或证实其内容的真实性;转载文章版权归原作者所有,作者如果不希望被转载或有侵权行为,请联系本平台删除。由于编译水平有限,推文或简历有不妥之处,深感抱歉,请联系本平台修改或者删除。
