南昌大学谢明勇院士团队:多组学视角揭示铁皮石斛多糖通过调节“肠—脂肪轴”抑制脂滴扩张从而缓解饮食诱导的肥胖
- 2026-05-14 12:55:12
点击蓝字

关注我们



肥胖已成为全球性健康挑战。南昌大学谢明勇教授、李志鹏研究员等人在国际期刊Food science and human wellness上发表了题为《 Multi-omics Insights into the Mitigation of Diet-induced Obesity by Dendrobium officinale Polysaccharides via Gut-Adipose Tissue Axis Modulation of Lipid Droplets》的研究,表明铁皮石斛多糖(DOP)可能通过抑制脂滴扩张显著缓解高脂饮食诱导的肥胖。该研究首次阐明了 DOP 跨组织调控脂质代谢的整合机制,为天然多糖开发为抗肥胖功能食品提供了重要科学依据。


研究背景

随着全球肥胖及相关代谢疾病患病率的上升,挖掘具有减脂潜力的活性物质具有重要意义。DOP作为铁皮石斛的核心生物活性成分,虽在糖尿病治疗中展现出潜力,但其对抗肥胖的分子机制仍待厘清。肥胖的核心在于脂肪过度蓄积,而肠道微生物群作为调控宿主脂质代谢的关键枢纽,其构成受膳食纤维等底物的显著影响。白色脂肪组织(WAT)中的脂滴(LD)不仅是储能细胞器,更是调节能量代谢与细胞信号的核心。研究发现,PLIN2 和 PLIN3 等脂滴包被蛋白的过表达直接促进脂质堆积,是代谢紊乱的重要诱因。本研究利用多组学整合分析发现,DOP 能够通过调节“肠道微生物-代谢产物”轴,抑制 WAT 中 PLINs 介导的脂滴扩张,进而改善高脂饮食诱导的肥胖。这种系统生物学视角揭示了 DOP 通过重塑组织微环境实现抗肥胖作用的综合机制。
实验结果

01
DOP 缓解 C57BL/6J 小鼠高脂饮食诱导的肥胖
通过9周高脂饮食(HFD)联合DOP干预发现,DOP显著降低了小鼠的体重增量和附睾脂肪(EAT)重量。虽然EAT指数(EAT/体重比)仅呈下降趋势(无统计学显著性),但H&E染色证实DOP显著缩小了脂肪细胞平均直径并优化了其尺寸分布,有效缓解了脂肪组织肥大。
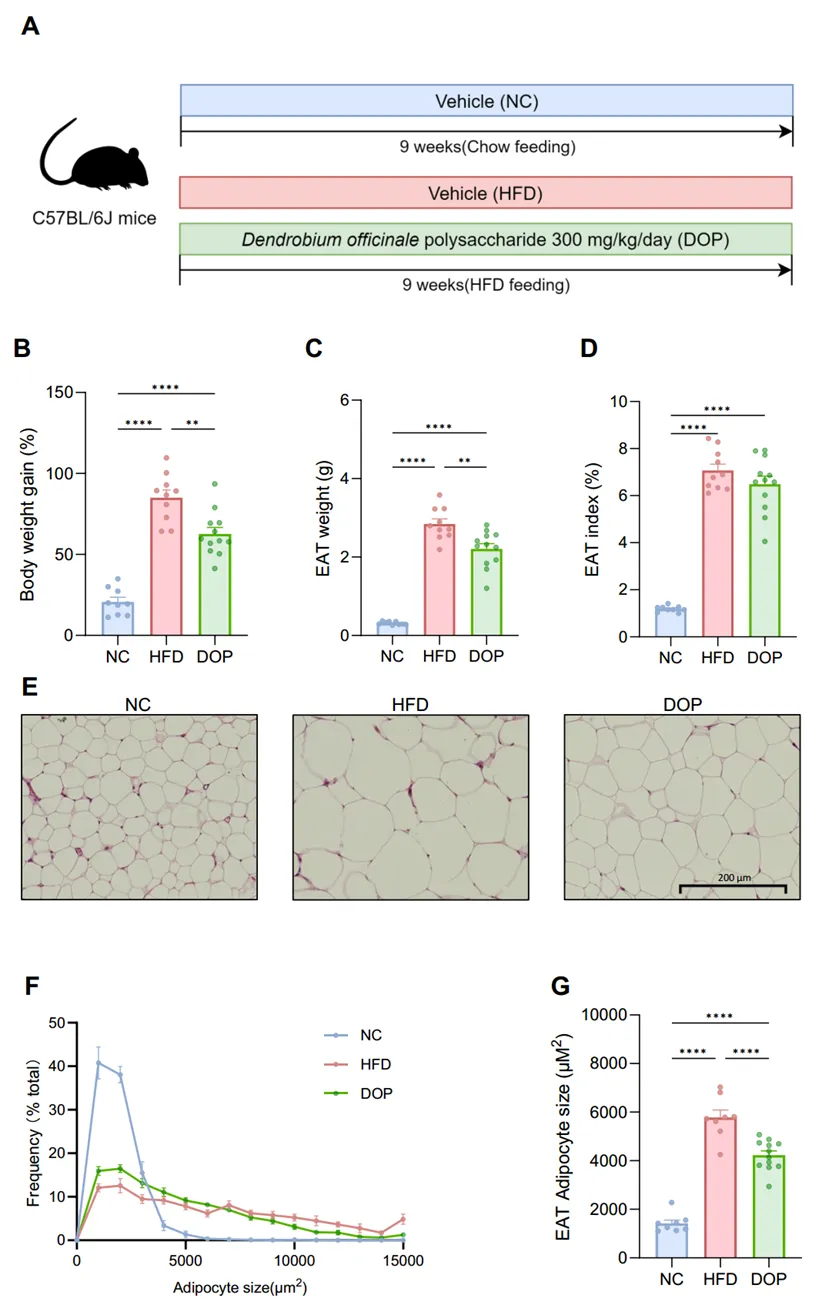
图 DOP 缓解 C57BL/6J 小鼠高脂饮食诱导的肥胖。(A) 实验设计。(B) 体重增长百分比。(C)EAT重量。(D) EAT重量与体重的比值。(E) EAT的苏木精-伊红(H&E)染色。(F) EAT中脂肪细胞大小分布。(G) EAT中平均脂肪细胞大小。
02
DOP调节肥胖小鼠脂肪细胞中的脂滴
DOP显著调节了EAT中的1663个基因,并表现出逆转HFD所致基因表达变化的明确趋势;同时显著下调了与脂滴形成及脂质储存相关的通路。脂滴基因表达得分(LD score)也在DOP干预下显著降低,因此DOP有效抑制了关键脂滴包被蛋白基因Plin2和Plin3的表达,从转录水平证实了其对脂滴扩张的抑制作用。免疫荧光分析显示,DOP也显著降低了PLIN2、PLIN3的蛋白表达和共定位。
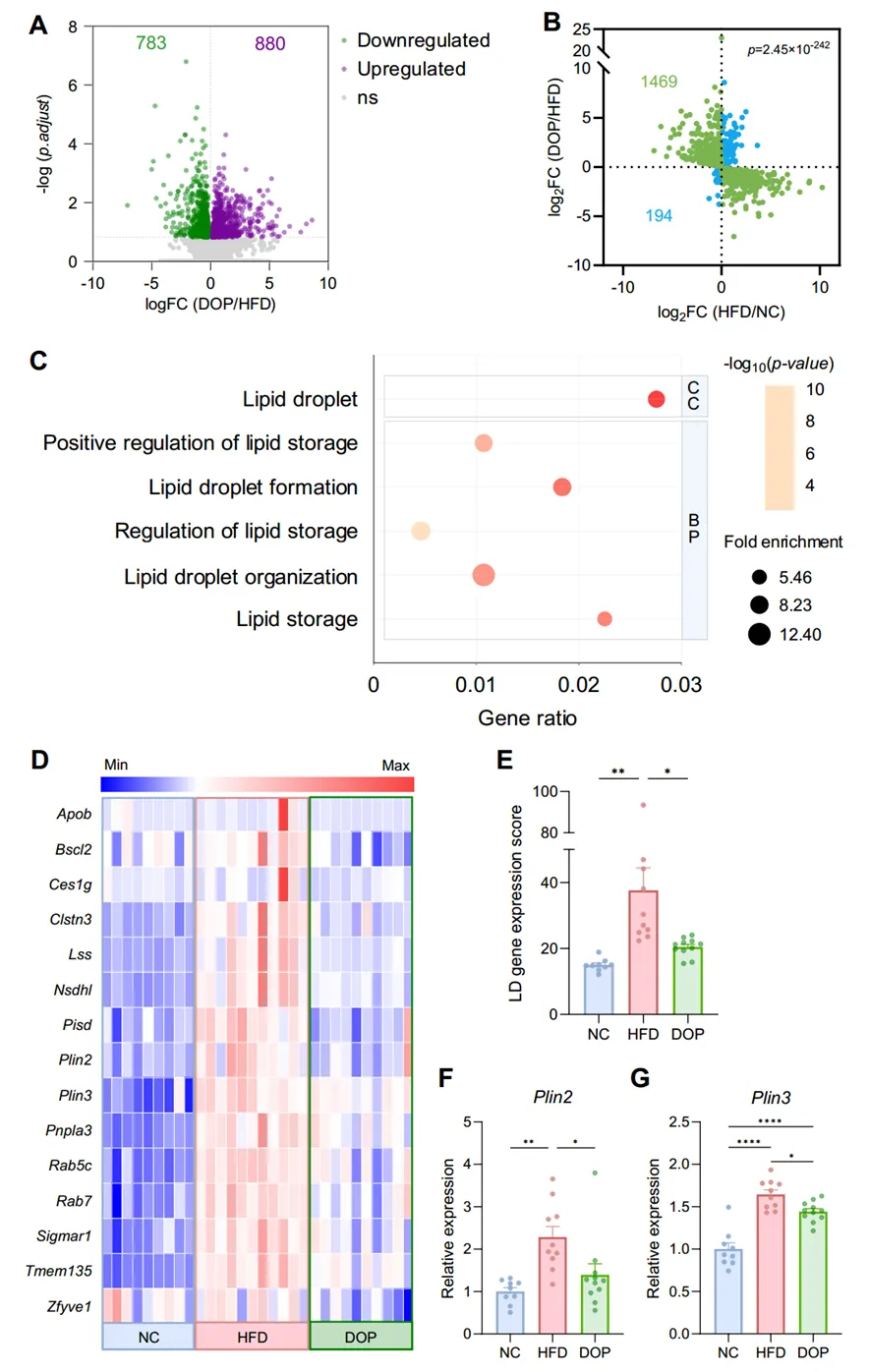
图 DOP 抑制高脂饮食诱导肥胖小鼠附睾脂肪组织中脂滴相关基因的表达。(A)DOP 处理调控的基因火山图(FDR<15%)。(B)DOP 与高脂饮食(HFD)对基因表达调控的关系。(C)仅针对 Gene Ontology 的基因富集分析,限于 DOP 下调的基因。(D)显示脂滴通路中基因表达的热图。(E)将(D)中基因首先根据其平均表达值进行标准化,然后相加以反映与脂滴相关的基因整体表达水平。(F-G)EAT 中 Plin2(F)和 Plin3(G)基因的相对表达水平。
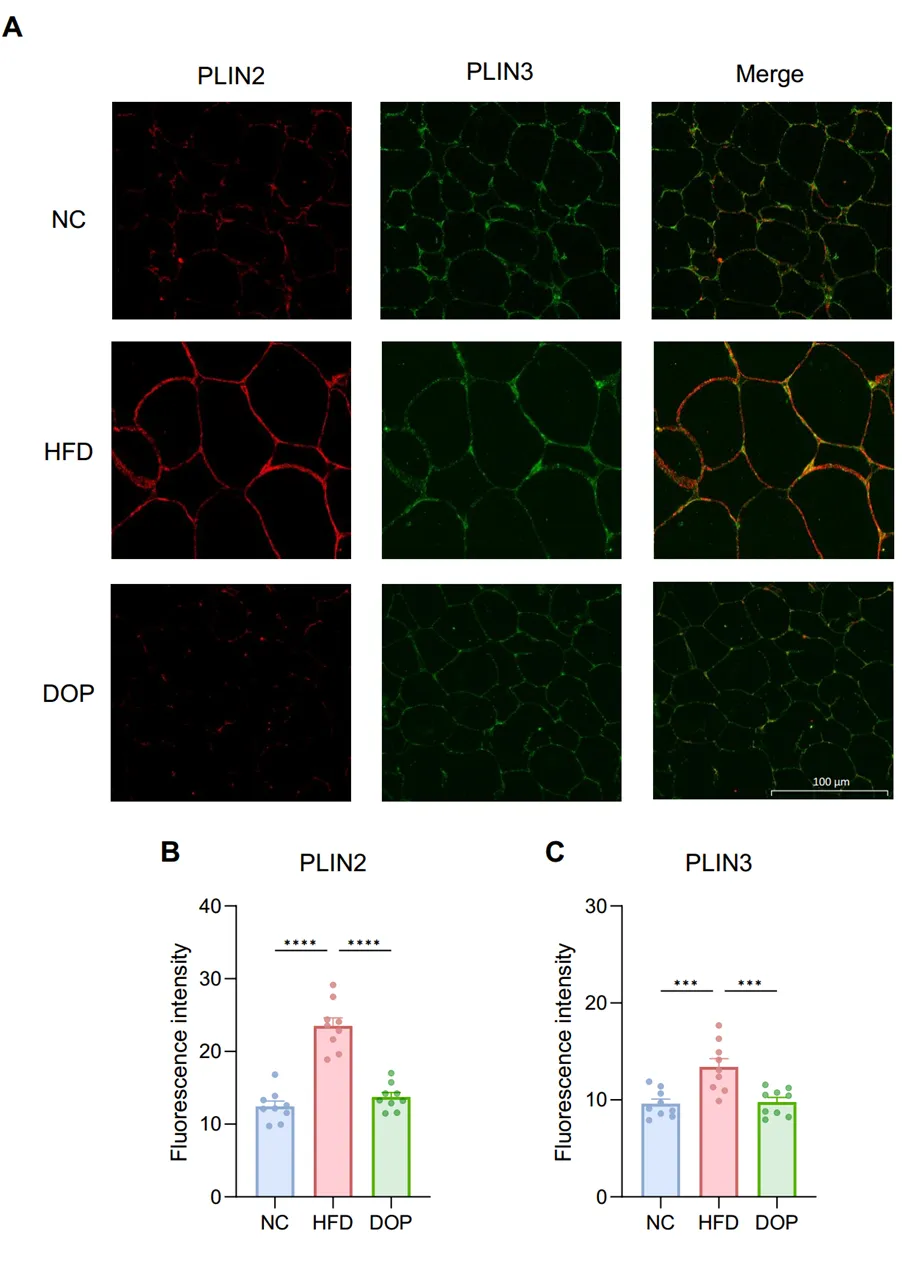
图 免疫荧光分析显示DOP处理对EAT中PLIN2和PLIN3蛋白水平的影响。(A) EAT中PLIN2(红色)和PLIN3(绿色)的代表性免疫荧光图像。(B-C) EAT中PLIN2(B)和PLIN3(C)的荧光强度定量分析。
03
脂滴包被蛋白在肥胖小鼠与人类中的表达均上调
在DIO小鼠与肥胖人群的脂肪组织中,PLIN3均呈现出强有力且一致的上调特征,而PLIN2的上调则具有边缘统计学意义。因此,PLIN3在跨物种肥胖中具有稳定且显著的上调特性,而PLIN2的表达变化则更具变异性和背景依赖性。
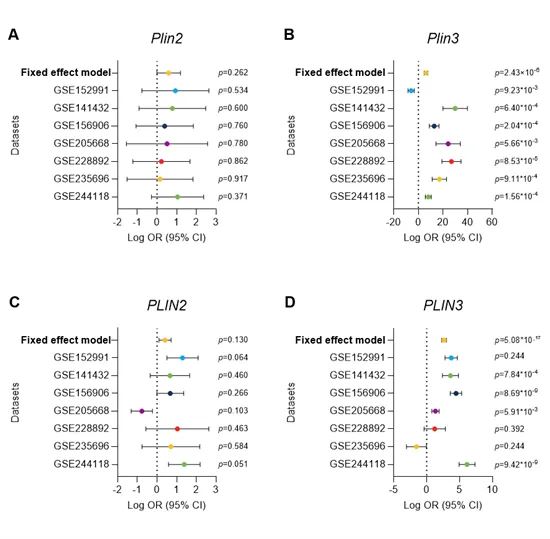
图附睾脂肪组织(EAT)中脂滴相关基因与肥胖的荟萃分析。(A-B) 小鼠数据集中脂滴包被蛋白2(Plin2, A)和脂滴包被蛋白3(Plin3, B)表达水平的森林图。(C-D) 人类数据集中脂滴包被蛋白2(PLIN2, C)和脂滴包被蛋白3(PLIN3, D)表达水平的森林图。
04
脂滴相关基因与代谢稳态呈显著正相关
脂滴相关基因的表达水平与多项关键代谢指标存在紧密的正相关关系,包括脂肪细胞大小、体重增长、EAT重量以及葡萄糖和胰岛素耐量状况。整合后的脂滴基因表达得分与体重、空腹血糖、GTT-AUC(糖耐量曲线下面积)及ITT-AUC(胰岛素耐量曲线下面积)均呈现极显著的正相关,表明脂肪组织内脂滴的异常扩张不仅是肥胖的表现,更是导致脂肪肥大、损害全身葡萄糖稳态和胰岛素敏感性的核心驱动因素。
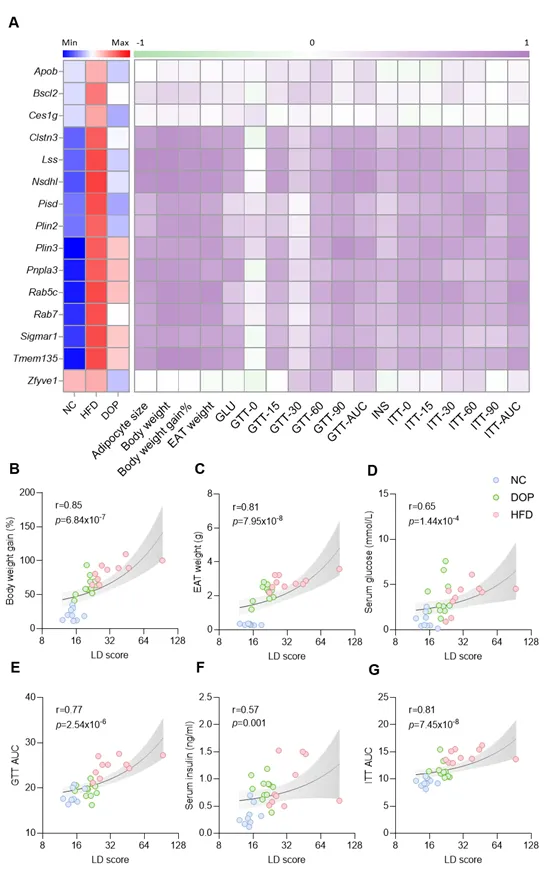
图 EAT中脂滴相关基因的表达水平与各项代谢指标的相关性分析。(A)脂滴信号通路中基因的表达模式及其与多种代谢参数之间的相关性。(B-G)脂滴基因表达得分与不同代谢表型之间的具体相关性关系。
05
DOP下调脂肪组织的脂质生物合成与储存通路
脂滴是脂肪储存的核心,DOP 显著抑制了附睾脂肪(EAT)中的脂质合成与储存通路。针对高脂饮食诱导的基因异常,DOP 显著下调了负责脂肪酸从头合成的 FASN、脂肪酸转运的 FABP1、胆固醇摄取的 LDL-R 以及反映瘦素抵抗的 Leptin。此外,DOP 还能抑制促进脂肪细胞分化的 Cebpb 并逆转 Dio2 等基因表达。这些发现表明,DOP 通过多靶点干预脂质生物合成与分化过程,有效遏制了脂滴的过度扩张。
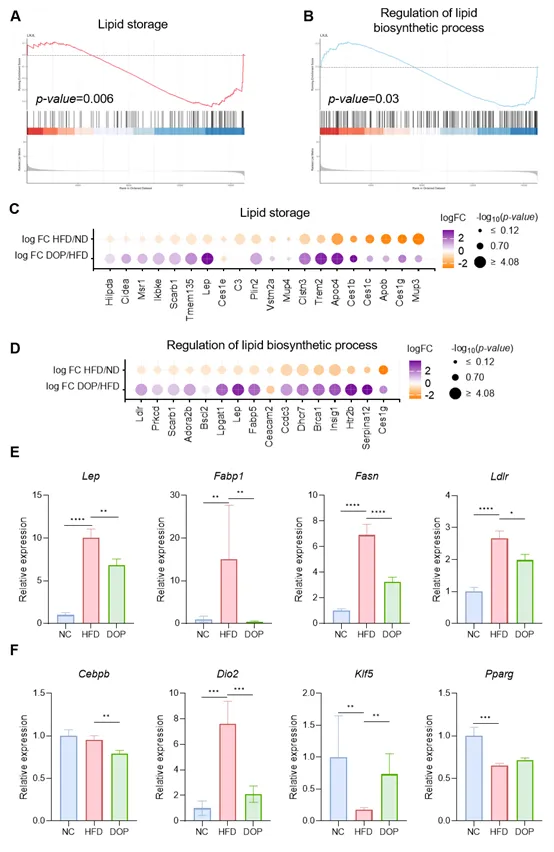
图 DOP 抑制HFD小鼠EAT中的脂质生物合成与储存。(A-B) GSEA 富集分析结果显示,DOP 显著抑制了脂质储存通路(A)及脂质生物合成调节通路(B)。(C-D) DOP 分别对 A、B 两通路中关键基因的调节作用。(E-F) 脂质储存与生物合成相关基因(E)及脂肪细胞分化相关基因(F)的相对表达水平。
06
DOP上调脂肪组织的Wnt信号通路
DOP对脂质合成与储存的抑制作用可能源于其对Wnt信号通路的激活,该通路在生理状态下具有抑制脂肪细胞分化的功能。GSEA分析确认,补充DOP显著激活了EAT中的Wnt信号传导。在肥胖小鼠中,Wnt家族的关键配体基因(如Wnt5b、Wnt6和Wnt7b)表达显著受损,而DOP干预则有效恢复或上调了这些基因的表达。这一发现表明,激活Wnt信号通路可能是DOP改善脂肪组织脂质代谢、对抗肥胖的重要分子机制之一。
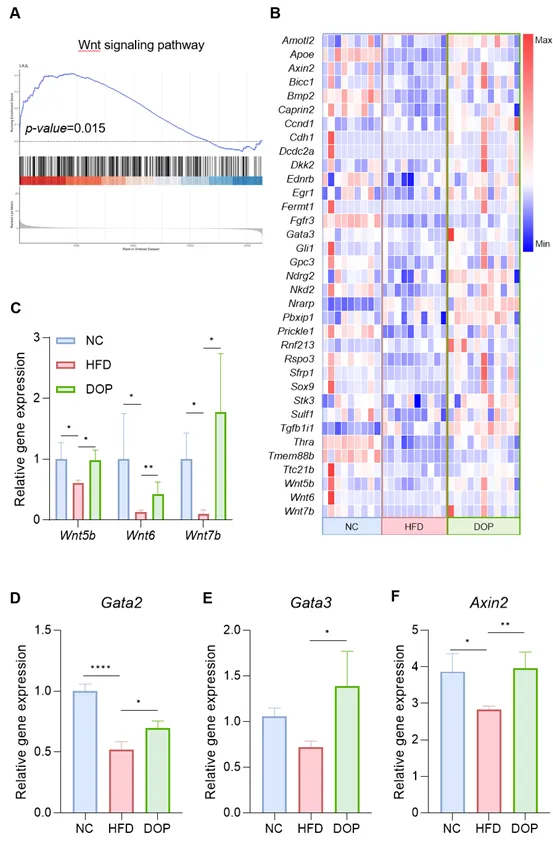
图 DOP 上调HFD小鼠EAT中的 Wnt 信号通路。(A) GSEA 富集分析结果显示DOP 显著增强了 Wnt 信号通路。(B) 热图展示了 Wnt 信号通路中相关基因的表达模式。(C) Wnt5b、Wnt6 和 Wnt7 的相对表达水平。(D-F) Gata2、Gata3 和 Axin2 的相对表达水平。
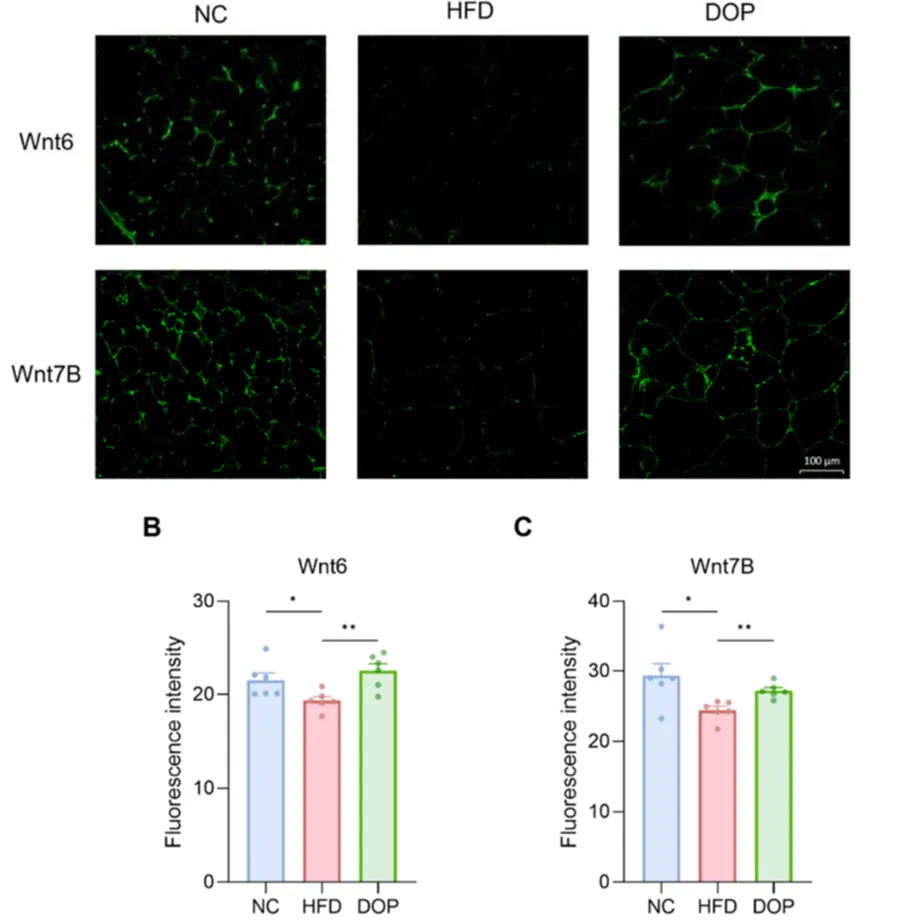
图EAT中Wnt6和Wnt7B蛋白表达的免疫荧光分析。(A) Wnt6和Wnt7B表达的代表性免疫荧光图像。(B-C) 不同组小鼠中Wnt6和Wnt7B蛋白水平的定量比较。*P < 0.05,**P < 0.01。
07
DOP 缓解高脂饮食诱导的肠道菌群失调
作为膳食纤维,DOP 通过调节肠道菌群展现出强大的代谢调节能力。DOP 显著逆转了高脂饮食(HFD)引起的菌群丰度波动:原本在 HFD 组消失的 331 种菌(如 Bifidobacterium castoris)在 DOP 干预后重新出现,而 HFD 诱导产生的 51 种菌(如 Campylobacter coli)则在DOP干预后后消失。而被 DOP 回调的菌群丰度与脂滴基因表达得分及体重增长、GTT-AUC 等代谢指标呈显著负相关;反之,被抑制的菌群则与肥胖表型正相关。
研究发现B. pseudolongum和B. choerinum是潜在的关键介导者,其丰度受 DOP 驱动而显著回升,并与脂滴基因表达得分和代谢表型呈强负相关。即DOP主要通过重塑肠道微生态、提升特定核心菌群丰度,进而遏制脂滴扩张并改善代谢表型。
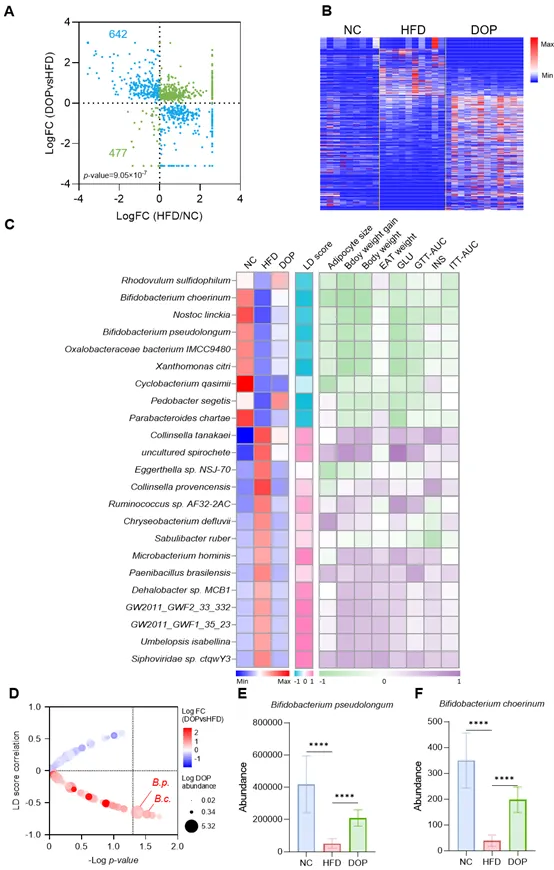
图 DOP 对HFD诱导的肠道菌群失调的调节作用及其与脂滴形成和代谢表型之间的关系。(A) DOP 和 HFD 对肠道微生物调节作用之间的关系。(B)DOP 显著调节的肠道微生物丰度(FDR < 15%)。(C) DOP 调节的肠道微生物丰度,且其水平与脂滴(LD)扩张及代谢参数呈现一致的相关性。(D) 肠道微生物散点图(x 轴和 y 轴分别代表微生物丰度与脂滴基因表达之间相关性的 p 值和相关系数;散点颜色表示 DOP 调节下微生物的差异倍数,散点大小代表其在粪便中的平均丰度)。(E-F) Bifidobacterium pseudolongum(E)和Bifidobacterium choerinum(F)的丰度。****p < 0.0001。
08
DOP改变了高脂饮食小鼠体内循环的代谢物谱
非靶向代谢组学分析显示,NC、HFD 与 DOP 组的小鼠血清代谢物谱在低维空间内呈现显著分离,揭示了 DOP 对血清代谢物谱的强力调节作用。DOP 能够逆转高脂饮食诱导的多种代谢物异常波动,且这些代谢物的表达变化与脂滴相关基因及表型(如脂肪细胞大小、体重增长、GTT-AUC 及 ITT-AUC 等)密切相关。
DOP 显著上调了在肥胖小鼠中下调的长链酰基肉碱类物质(如 L-棕榈酰肉碱等),此类代谢物的回升与代谢紊乱表型呈负相关,反映出 DOP 可能通过优化脂肪酸β氧化水平,重塑血清代谢特征,进而调控脂质代谢基因表达并改善整体代谢表型。
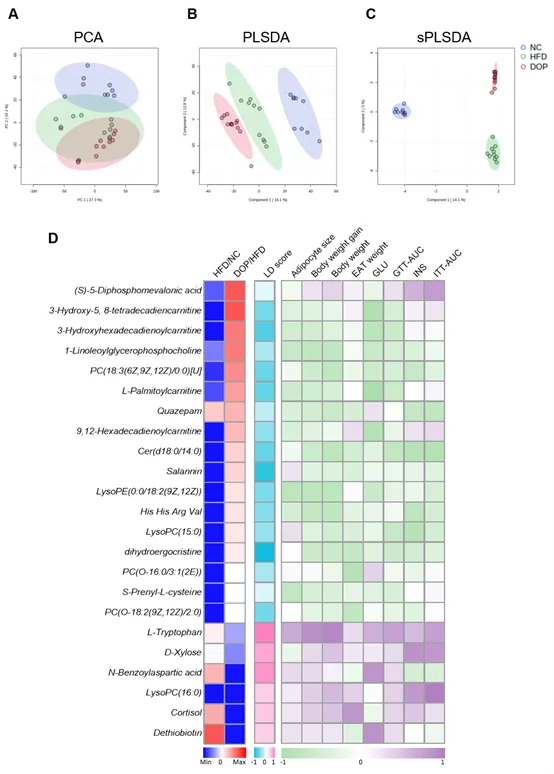
图DOP 调节的代谢物可能介导其对脂滴(LD)相关基因及代谢表型的调控作用。(A-C) 血清代谢物的主成分分析(PCA)、偏最小二乘判别分析(PLSDA)及稀疏偏最小二乘判别分析(sPLSDA)。(D)DOP 调节的代谢物及其与 脂滴基因表达得分、代谢表型之间的相关性。
09
DOP通过调节肠道菌群及其代谢物来调控代谢
微生物群主要通过代谢物中介作用影响脂肪组织基因表达,而非直接作用于表型。DOP 能够调节“肠道—脂肪组织轴”,进而激活白脂肪组织中的 Wnt 信号通路,通过抑制脂质合成、储存及脂滴扩张,有效逆转饮食诱导的肥胖。这种跨组织的信息流揭示了 DOP 改善代谢紊乱的核心机制。
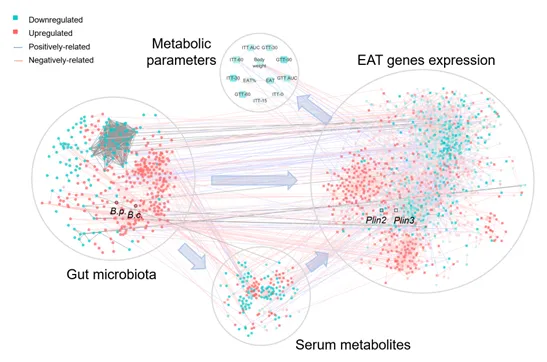
图 多组学协方差网络揭示 DOP 对高脂饮食诱导肥胖小鼠的信息流调控模式。图中节点代表受 DOP 显著调节的肠道微生物、血清代谢物、基因表达或代谢表型。节点颜色对应 DOP 的调节方向。连线代表两个节点间的 Spearman 相关性,连线颜色反映相关性的正负。
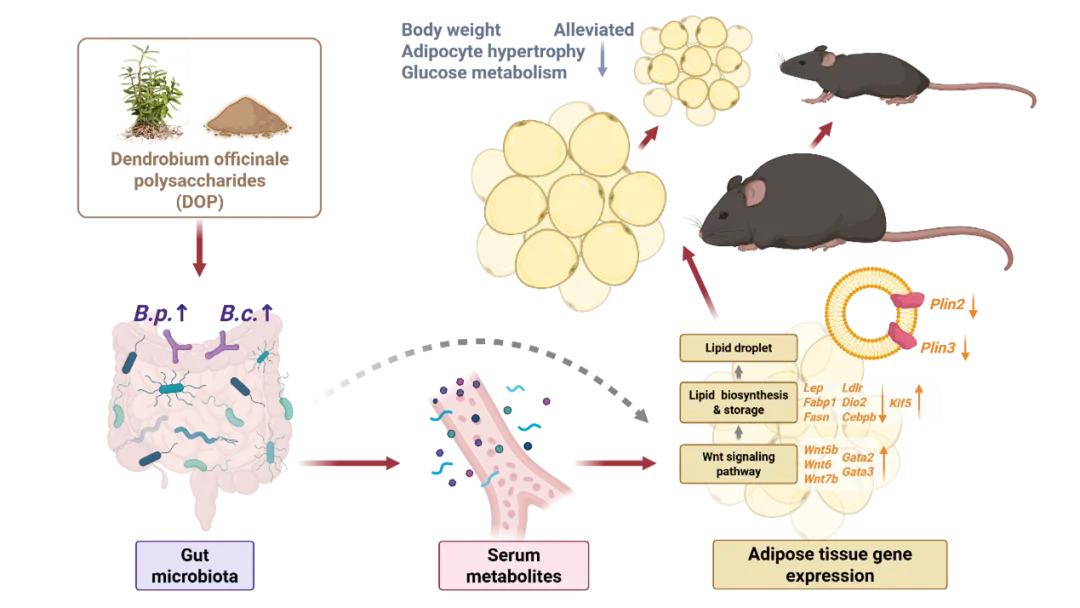
图 铁皮石斛多糖通过“肠道—脂肪组织轴”激活 Wnt 信号通路,进而抑制脂质合成与脂滴扩张,最终缓解饮食诱导的肥胖。
结论与展望

DOP 可显著缓解小鼠肥胖,其核心机制在于通过调控“肠道微生物—代谢产物”轴,进而激活白脂肪组织中的 Wnt 信号通路。这一调控过程有效抑制了脂质合成、减少了脂滴形成并改善了整体代谢紊乱。研究不仅为 DOP 的抗肥胖机制提供了多维度见解,更凸显了其作为功能性食品成分在预防和管理肥胖及相关代谢疾病中的潜力。
(请点击标题查看)
分子对接与分子动力学黄酮类化合物
食品感官科学与分析农产品贮藏与加工
肉与肉制品蛋与蛋制品水产品
奶及奶制品豆及豆制品果蔬及果蔬制品
大米及米制品
炎症性肠病糖尿病肝病神经疾病
(请点击标题查看)
(请点击学者姓名查看)


在线投稿平台链接:https://www.wjx.top/jq/85151447.aspx
标注‘原创’仅代表原创编译,本平台不主张对原文的版权。本平台转载仅仅是出于学术交流和传播信息的需要,并不意味着代表本平台观点或证实其内容的真实性;转载文章版权归原作者所有,作者如果不希望被转载或有侵权行为,请联系本平台删除。由于编译水平有限,推文或简历有不妥之处,深感抱歉,请联系本平台修改或者删除。
