结肠癌是全球范围内高发的消化道恶性肿瘤,其术后复发与远处转移始终是临床治疗的核心难题。数据显示,2023 年结肠癌患者术后肿瘤复发与远处转移发生率约 20%,超 50% 的患者在初诊后 5 年内会发生远处转移,而化疗耐药正是导致肿瘤复发、转移的首要元凶。
目前,奥沙利铂联合方案是结肠癌一线化疗的核心选择,但临床中仍有大量患者对治疗不敏感,最终面临治疗失败。既往研究证实,肿瘤干细胞特性、上皮 - 间质转化(EMT)是调控肿瘤化疗耐药与转移的核心生物学过程。因此,找到驱动这两大过程的关键分子,破解结肠癌化疗耐药与转移的机制困局,成为消化道肿瘤领域的研究重点。
南昌大学第二附属医院黄俊教授团队在国际期刊发表重磅研究,首次完整阐明了OTUB2/SP1/GINS1 调控轴在结肠癌干细胞特性维持、化疗耐药和 EMT 进程中的核心作用,为结肠癌的精准靶向治疗、逆转化疗耐药提供了全新的靶点与理论依据。
吉凯助力: 本文中过表达OTUB2、SP1质粒以及泛素质粒均由吉凯基因提供。

一、锁定关键分子:OTUB2 高表达,与结肠癌不良预后密切相关
OTUB2 是卵巢肿瘤(OTU)去泛素化酶家族的重要成员,既往研究已发现其在多种恶性肿瘤中参与调控肿瘤进展,但它在结肠癌中如何影响肿瘤干细胞特性、化疗敏感性与转移能力,此前始终未有明确答案。
研究团队首先通过多维度的临床样本与数据库分析,锁定了 OTUB2 在结肠癌中的异常表达特征:
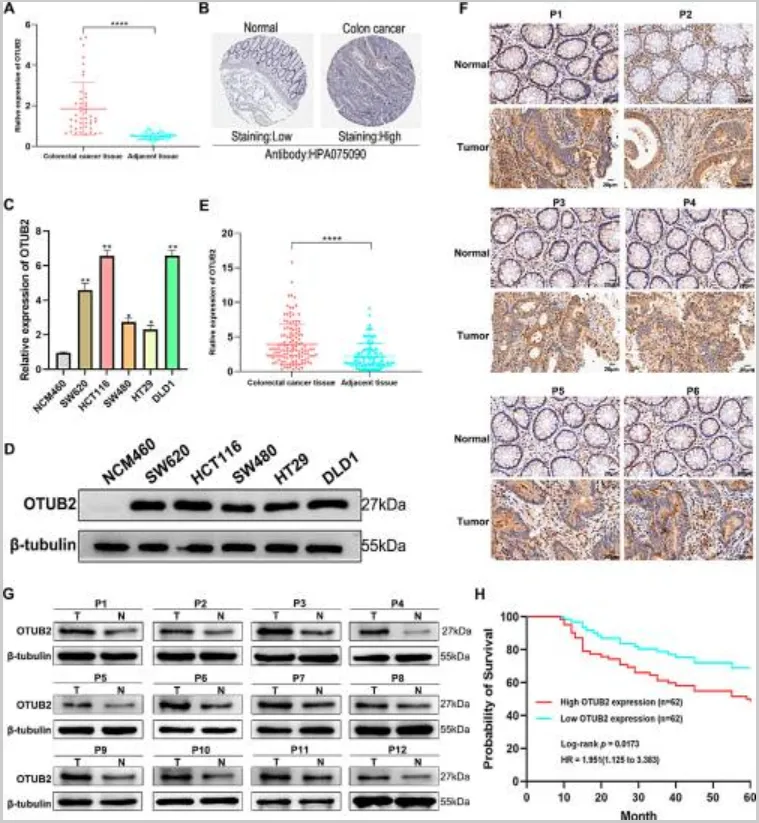
- 基于 TCGA-COAD 数据库、HPA 数据库的分析显示,结肠癌组织中 OTUB2 的 mRNA 与蛋白表达水平,显著高于癌旁正常组织;
- 团队收集 124 例结肠癌患者的配对临床样本,通过 qRT-PCR、免疫组化、Western blot 等实验进一步验证,癌组织中 OTUB2 的表达显著上调;生存分析结果显示,OTUB2 高表达的结肠癌患者,总生存期(OS)显著更低,其表达水平与患者不良预后呈负相关;临床病理特征分析证实,OTUB2 高表达与肿瘤直径增大、淋巴结转移、远处转移显著相关。
这一系列结果明确提示:OTUB2 的异常高表达,可能是驱动结肠癌恶性进展的关键分子,也是评估患者预后的潜在生物学标志物。
二、功能验证:OTUB2 是结肠癌恶性表型的核心 “助推器”
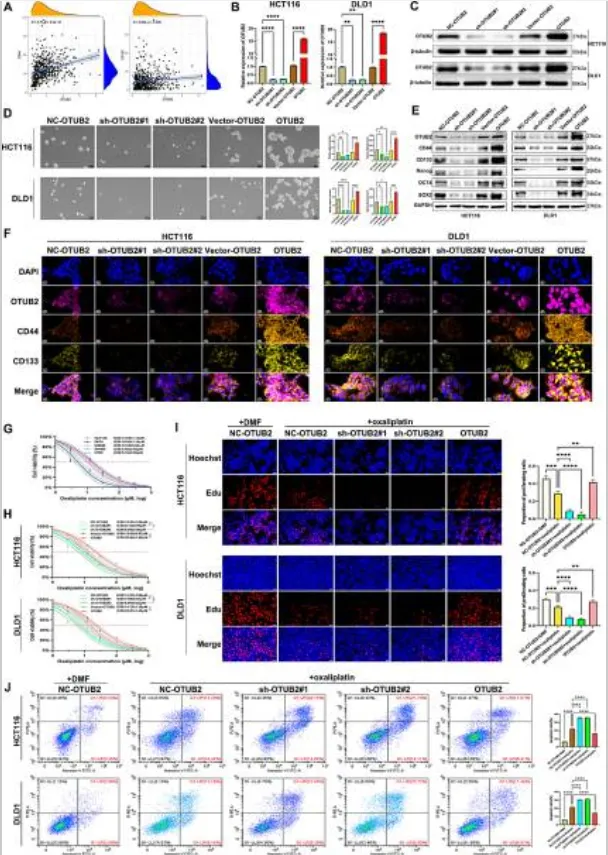
为了明确 OTUB2 在结肠癌中的具体生物学功能,研究团队开展了系统的体外功能实验,通过敲低 / 过表达 OTUB2,全面验证了其对结肠癌恶性表型的调控作用:
- 调控肿瘤干细胞特性:敲低 OTUB2 显著削弱了结肠癌细胞的干细胞特性,而过表达 OTUB2 则明显增强了肿瘤细胞的成球能力与干细胞相关表型;
- 调控化疗敏感性:敲低 OTUB2 显著降低了结肠癌细胞对奥沙利铂的 IC50 值,增强了奥沙利铂诱导的细胞凋亡,提升了化疗敏感性;反之,过表达 OTUB2 则诱导结肠癌细胞对奥沙利铂产生耐药;
- 调控 EMT 与转移能力:敲低 OTUB2 显著抑制了结肠癌细胞的 EMT 进程(上皮标志物 E - 钙粘蛋白上调,间质标志物 N - 钙粘蛋白、波形蛋白下调),同时大幅削弱了肿瘤细胞的迁移与侵袭能力;过表达 OTUB2 则呈现完全相反的效应,显著促进 EMT 进程与肿瘤转移。
综上,研究团队证实:OTUB2 通过正向调控结肠癌干细胞特性、化疗耐药与 EMT 进程,最终驱动肿瘤的恶性进展与远处转移。
三、抽丝剥茧:完整揭示 OTUB2/SP1/GINS1 调控轴的分子机制
明确了 OTUB2 的生物学功能后,研究团队进一步深挖其背后的分子调控机制,逐步解锁了完整的信号调控链路。
第一步:锁定下游核心效应分子 GINS1
研究团队对敲低 OTUB2 的结肠癌细胞进行转录组测序,发现 OTUB2 敲低后,GINS1 的表达出现显著下调。而 GINS1 作为 DNA 复制调控的核心分子,既往研究已证实其在多种肿瘤中参与调控干细胞特性、化疗耐药与 EMT,是潜在的促癌基因。
通过系列回复实验,团队进一步验证:
- 过表达 GINS1 可完全逆转敲低 OTUB2 对结肠癌细胞干细胞特性、化疗敏感性、EMT 与迁移能力的抑制作用;
- 敲低 GINS1 可显著抵消过表达 OTUB2 诱导的肿瘤恶性表型。
这一结果明确:GINS1 是 OTUB2 发挥促癌作用的核心下游效应分子。
第二步:找到中间关键桥梁 —— 转录因子 SP1
有趣的是,团队通过泛素化实验发现,OTUB2 并不直接调控 GINS1 的泛素化与蛋白稳定性。这意味着,OTUB2 对 GINS1 的调控,必然存在一个关键的中间分子。
通过数据库预测与系列实验验证,团队最终锁定了答案:转录因子 SP1。
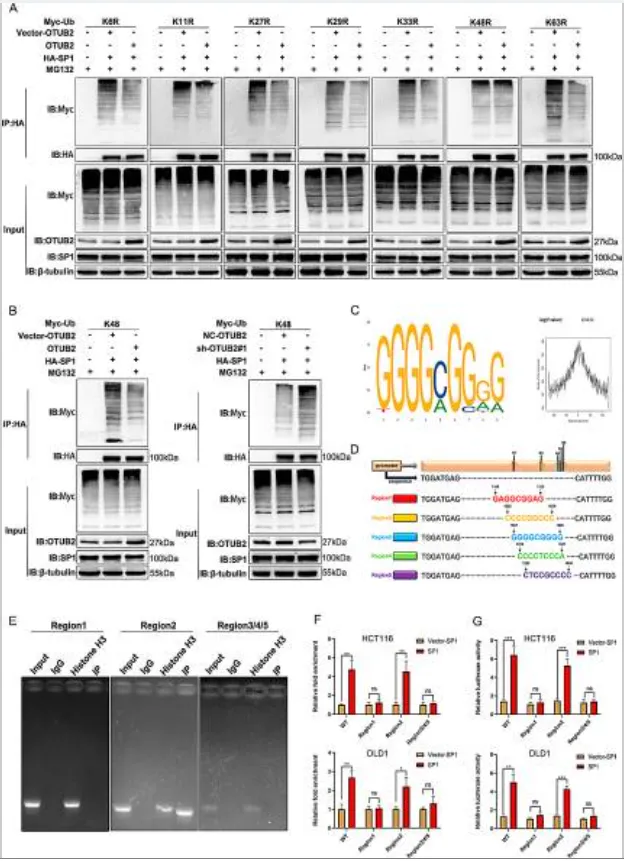
- OTUB2 直接稳定 SP1 蛋白表达:OTUB2 作为去泛素化酶,可直接与 SP1 蛋白结合,特异性抑制 SP1 蛋白的 K48 位泛素化降解,从而显著上调 SP1 的蛋白表达水平;
- SP1 直接转录激活 GINS1:SP1 作为转录因子,可特异性结合 GINS1 启动子的 1822–1830 区域,直接增强 GINS1 的转录活性,上调其表达水平;
- SP1 通过 GINS1 驱动结肠癌恶性进展:回复实验证实,SP1 对结肠癌干细胞特性、化疗耐药、EMT 与转移的调控作用,完全依赖于下游的 GINS1。
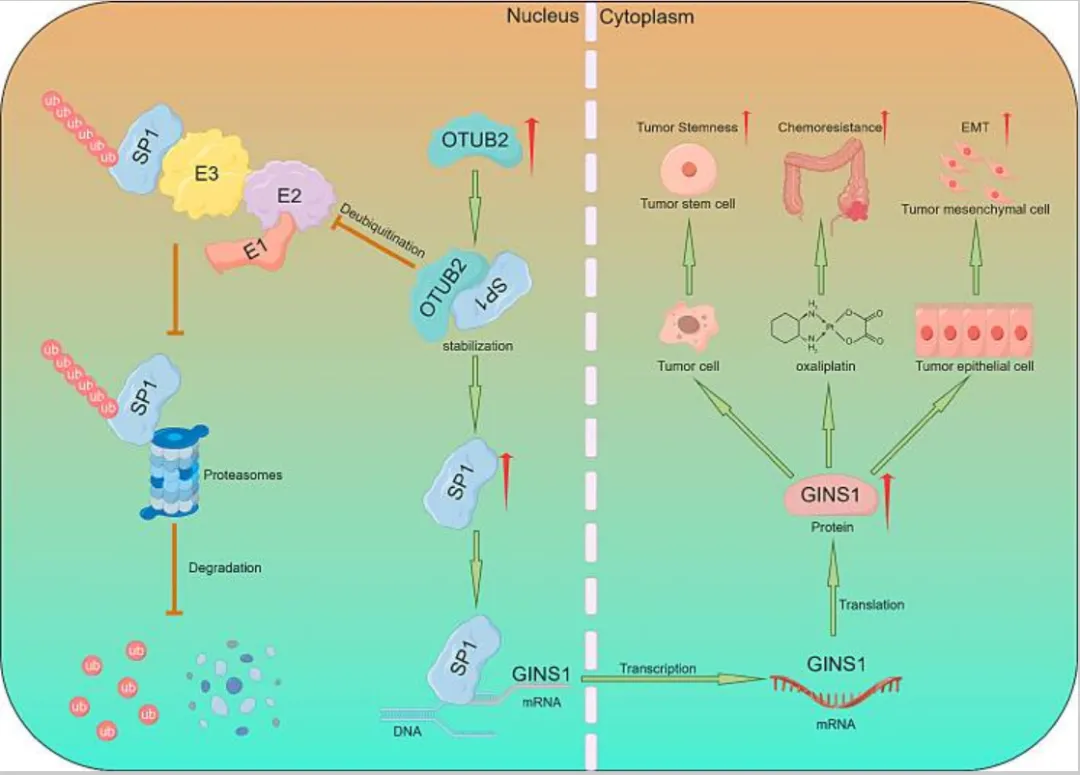
至此,研究团队完整揭示了整个调控链路:OTUB2 通过去泛素化修饰稳定 SP1 蛋白,上调的 SP1 转录激活 GINS1 表达,最终通过 OTUB2/SP1/GINS1 轴,驱动结肠癌干细胞特性维持、化疗耐药、EMT 进程与远处转移。
四、研究意义:为结肠癌精准治疗开辟新方向
这项研究首次系统阐明了 OTUB2 在结肠癌中的促癌作用与完整分子机制,填补了领域内的研究空白,具有重要的理论价值与临床转化意义:
- 明确了 OTUB2 可作为结肠癌预后评估的潜在标志物,以及精准治疗的全新靶点;
- 揭示了靶向抑制 OTUB2,可通过促进 SP1 泛素化降解、下调 GINS1 表达,最终增强结肠癌细胞对奥沙利铂的敏感性,逆转化疗耐药,同时抑制肿瘤干细胞特性与远处转移;
- 为结肠癌的联合治疗提供了全新策略 ——OTUB2 靶向药物联合奥沙利铂,有望突破临床化疗耐药的困局,为晚期 / 耐药结肠癌患者带来新的治疗希望。
当然,研究团队也指出,目前研究仍存在待完善之处,包括 OTUB2 与 SP1 结合的具体结构域、OTUB2 在肿瘤干细胞与耐药细胞株中的具体作用等,团队后续将开展进一步研究,推动该靶点的临床转化进程。
🔬 吉凯基因,助力您的研究~
🎯本文中过表达OTUB2、SP1质粒以及泛素质粒均由吉凯基因提供!
吉凯基因长期提供各类载体的泛素产品,覆盖:
✅ 泛素化质粒(Ubiquitination plasmids)✅ E3泛素连接酶相关载体✅ 蛋白互作与降解研究工具
📦 现货供应,即买即用,更有专业技术团队提供全程实验指导,助您快速推进泛素化机制研究!
吉凯基因4月活动进行中:
乳酸化修饰——国自然"代谢+表观"交叉领域的明星分子,研究范式正在快速迭代。如果你正关注这个领域:🕢 4月9日(周四)19:30🎯 深度解析:乳酸化修饰研究套路
📌 预约方式:长按下方海报识别二维码预约,锁定直播👇