南昌大学/江西农大/新加坡国立ACS Catal. |氧空位不是越多越好——Ni/CeZrO₂催化CO₂甲烷化中氧空位“活性”与“惰性”的区分
- 2026-05-09 06:23:17

这篇文章讨论的是Ni/CeZrO₂催化剂上CO₂加氢制甲烷过程中氧空位的真实作用。一个长期没搞清楚的问题是:我们都知道氧空位很重要,但它到底是怎么起作用的?是不是越多越好?哪些空位真正干活,哪些只是凑数的?之前的研究虽然注意到空位的影响,但大多停留在调控密度上——比如改变CeO₂的形貌、掺点别的金属、或者用等离子体处理一下,默认“空位多了活性就高”。
可这篇工作发现事情没那么简单。作者通过调Ce/Zr的比例,做了一系列Ni/CeₓZr₁₋ₓO₂催化剂(x=0, 0.25, 0.5, 0.75, 1)。结果很有意思:Ni/Ce₀.₅Zr₀.₅O₂活性最好,325℃时CO₂转化率能到81.4%,而且在450℃跑120个小时都很稳定。但Ni/Ce₀.₇₅Zr₀.₂₅O₂呢?它的氧空位浓度并不低,性能却最差。这就说明:空位不是越多越好,关键看是什么类型的空位。
表征结果也支持这个判断。
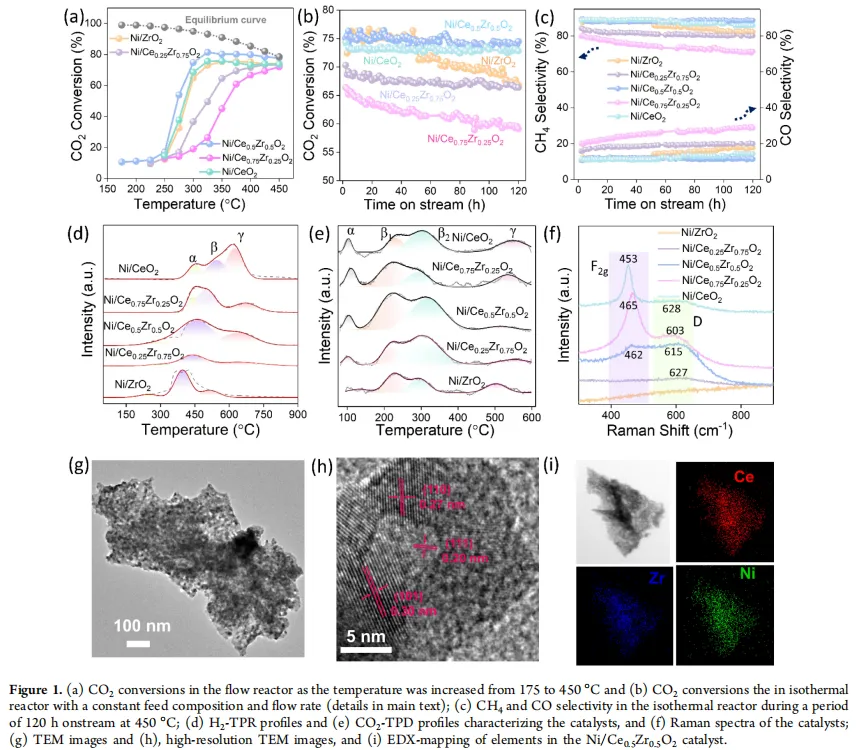
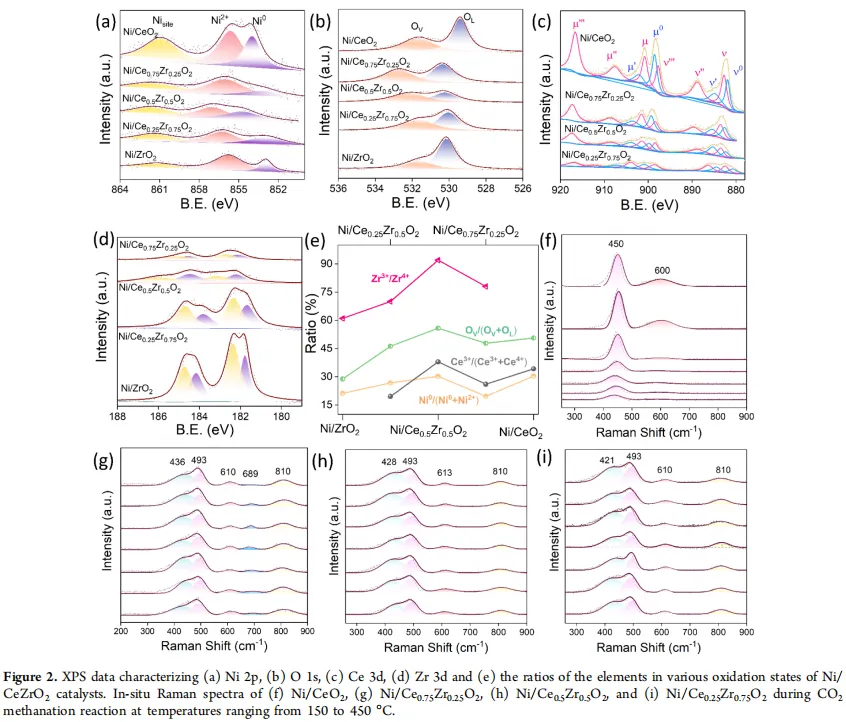
H₂-TPR显示,Ni/Ce₀.₅Zr₀.₅O₂的中等强度金属-载体相互作用最强,最有利于把NiO还原成金属Ni。CO₂-TPD和XPS都表明,这个催化剂的表面氧空位浓度确实最高(Ov占表面氧的55.8%,Ce³⁺比例0.38),金属Ni的比例也最高。Raman里缺陷峰与F₂g峰的比值(1.02)也证实它缺陷最多。但如果只看缺陷密度,Ni/Ce₀.₇₅Zr₀.₂₅O₂的比值也有0.49,不算低,可它就是不行。所以空位之间确实有本质差别。
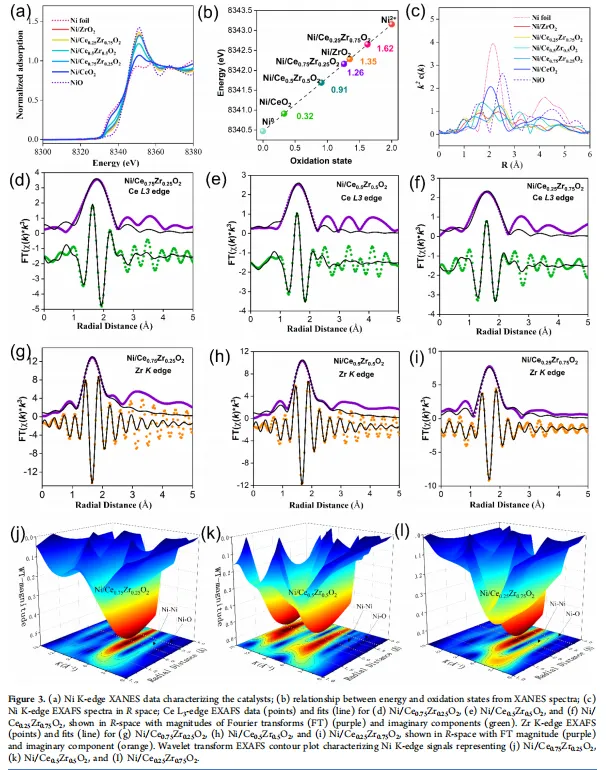
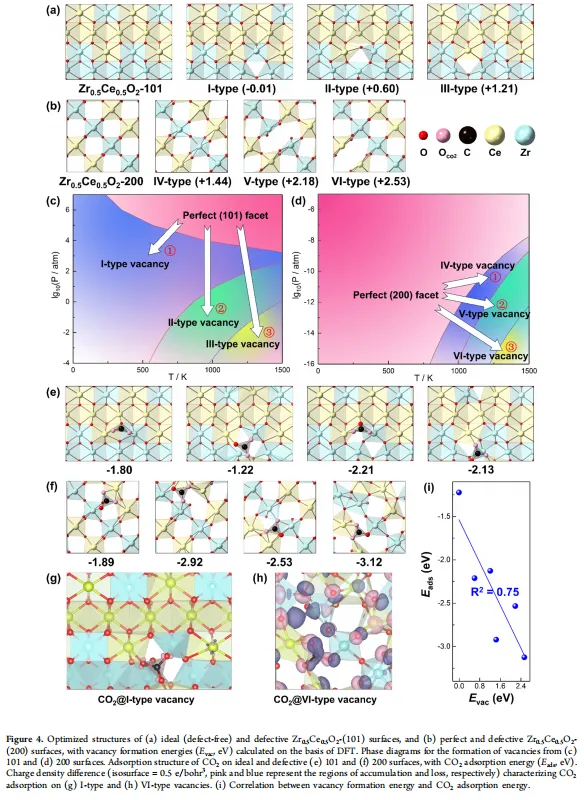
XAS结果进一步确认了这一点。Ni/Ce₀.₅Zr₀.₅O₂中Ni的氧化态已经很接近金属Ni,而且Ce-O和Zr-O的配位数最低,说明它周围的氧确实缺得多。DFT计算则把空位的“好坏”讲清楚了。在(101)晶面上,最稳定的I型空位(形成能-0.01 eV)对CO₂的吸附能力反而很弱,吸附能只有-1.22 eV,还不如没有缺陷的表面(-1.80 eV)。这就是那种“光站着不干活”的惰性空位。而不太稳定的III型空位(形成能+1.21 eV)反而能牢牢抓住CO₂,吸附能达到-2.13 eV。在(200)晶面上,最不稳定的VI型空位(形成能+2.53 eV)吸附CO₂后甚至会发生表面重构,电荷重新分布。总的趋势是:空位越容易形成,越稳定,就越“懒”;空位越难形成,越不稳定,反而越能干活。形成能和吸附能之间是负相关。
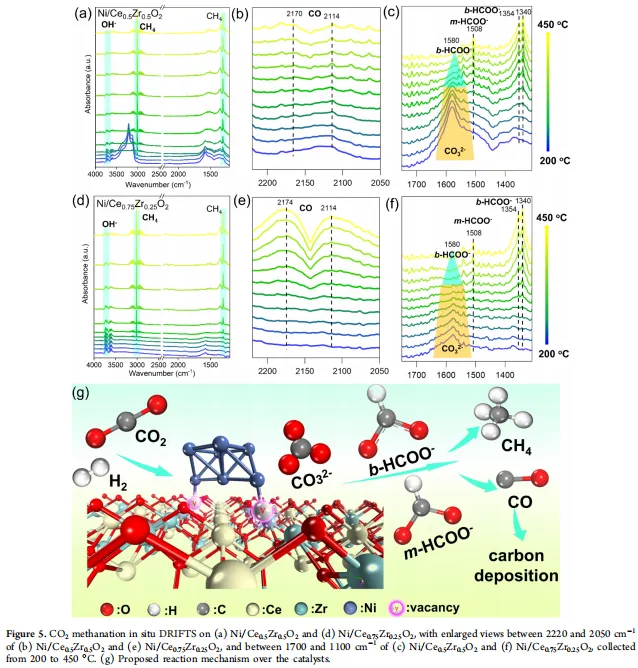
原位红外(DRIFTS)也给出了很直接的证据。在Ni/Ce₀.₅Zr₀.₅O₂表面,甲酸盐(HCOO⁻)的特征峰很强(1508、1354、1340 cm⁻¹),而CO的峰很弱,说明反应走的是甲酸盐路径,高效生成CH₄。反过来,性能差的Ni/Ce₀.₇₅Zr₀.₂₅O₂表面CO信号很强,甲酸盐信号弱,说明它走了CO中间体路径,不仅选择性差,还容易积碳失活。TGA和反应后的TEM也确实看到,只有Ni/Ce₀.₅Zr₀.₅O₂没有积碳,Ni颗粒也没有烧结。
CO₂甲烷化的活性不取决于氧空位的总浓度,而取决于活性空位(比如III型、VI型)和惰性空位(比如I型)的比例。活性空位能强吸附CO₂,让它走甲酸盐加氢的路;惰性空位吸附CO₂太弱,CO₂会跑到Ni位点上变成CO,然后就堵了、失活了。
论文信息: Vacancy-Driven Pathways in CO2 Hydrogenation over Ni/CeZrO2, ACS Catalysis , 2026, 16 5: 4583-4596. DOI:10.1021/acscatal.5c07746.
江南大学/中科院深圳先进院/华东理工Nat. Commun.:1T′-MoS₂靠面内+边缘位点协同实现CO₂高选择性制甲醇
