近日,南昌师范大学/肖强团队在《ACS催化》(ACS Catalysis)发表题为“A Nickel-Catalyzed Method for Csp3−P(III) Bond Formation: Efficient Transformation of Chlorophosphines with Alkyl Bromides”的研究,报道了一种镍催化还原交叉偶联构建 Csp³-P (III) 键的新方法,首次实现未活化烷基溴与易得氯膦的直接一步偶联,无需预制备有机金属试剂或多步合成磷源,显著提升了合成的原子和步骤经济性,该方法为高价值烷基膦化合物的合成提供了简洁、通用的新路线,有望推动有机磷化学在催化、生物医药和材料领域的进一步发展。镍催化还原交叉偶联反应实现了未活化烷基溴与氯膦的高效 Csp³-P (III) 键构建。该策略具有广泛的底物适用范围,可实现伯、仲、叔烷基溴的直接磷化。与传统方法相比,该方法无需使用预制备的对空气敏感的有机金属试剂或多步合成的磷源,同时克服了烷基底物反应活性低、竞争性 β- 氢消除以及氯膦亲电性强、易水解等关键难题。本文提出了合理的反应机理,为构建多样化的烷基膦化合物库提供了一条简洁、通用的路线,有望推动有机磷化合物在催化、材料科学和生物学领域的应用。三价膦是有机磷化学的核心,其可调控的电子性质和配位能力使其成为均相催化中的优势配体,能提升工业过程的选择性和效率。富电子烷基取代的三价膦衍生物因强给电子性和大空间位阻,在惰性键活化和选择性转化中表现优异,但这类膦的合成存在重大挑战。
传统合成策略主要基于亲核取代反应,存在严格的无水 / 无氧要求、需化学计量金属试剂、底物对空气 / 水分敏感等局限性,限制了官能团耐受性和底物范围。过渡金属催化为 C (sp³)-P (III) 键构建提供了温和、官能团耐受性好的方法,但现有方法的磷源仍需从氯膦前体制备,直接将易得的氯膦与未活化烷基溴偶联的方法尚未被探索,开发一步偶联策略具有重要的原子和步骤经济性。
镍催化还原交叉偶联为碳 - 杂原子键构建提供了新策略,但氯膦与未活化烷基溴的高效偶联面临三大难题:烷基亲电试剂反应活性低、烷基 - 镍 (II) 物种易发生 β- 氢消除、氯膦亲电性强且易水解导致催化剂失活。本研究利用镍催化剂的单电子氧化还原能力,通过自由基接力策略实现了二者的高效选择性还原偶联。
3.1 反应条件优化
以 1 - 溴 - 3 - 苯基丙烷与二苯基氯化膦为模型反应,筛选得到最优条件:10 mol% Ni (二甘醇) Br₂为催化剂、10 mol% 2,2':6',2''- 三联吡啶为配体、3.0 当量 Mn 为还原剂、DMF 为溶剂(0.1 M),0℃反应 24 h 后加入 BH₃・THF 处理,目标产物分离收率达 84%。烷基溴:伯烷基溴均能高效反应,含氟、氯、醚、酯、氨基、酰胺、氰基、磷酸酯、羟基等官能团的底物均能耐受,酸性性质子(酰胺、羟基)也与体系兼容;呋喃、噻吩等杂环取代烷基溴可顺利反应,吡啶杂环则不适用;烯丙基溴、苄基溴收率分别为 84% 和 72%;仲、叔烷基溴(含大位阻底物)也能高效转化,四至六元环烷基溴、含氧 / 氮杂环烷基溴均能以 76%-80% 的收率得到产物。氯膦:芳环上连有吸电子、给电子或中性取代基的氯膦均能高效反应,间位取代、呋喃杂环取代的氯膦反应性良好;烷基取代氯膦在标准条件下反应失败,仅检测到氯膦的自偶联产物。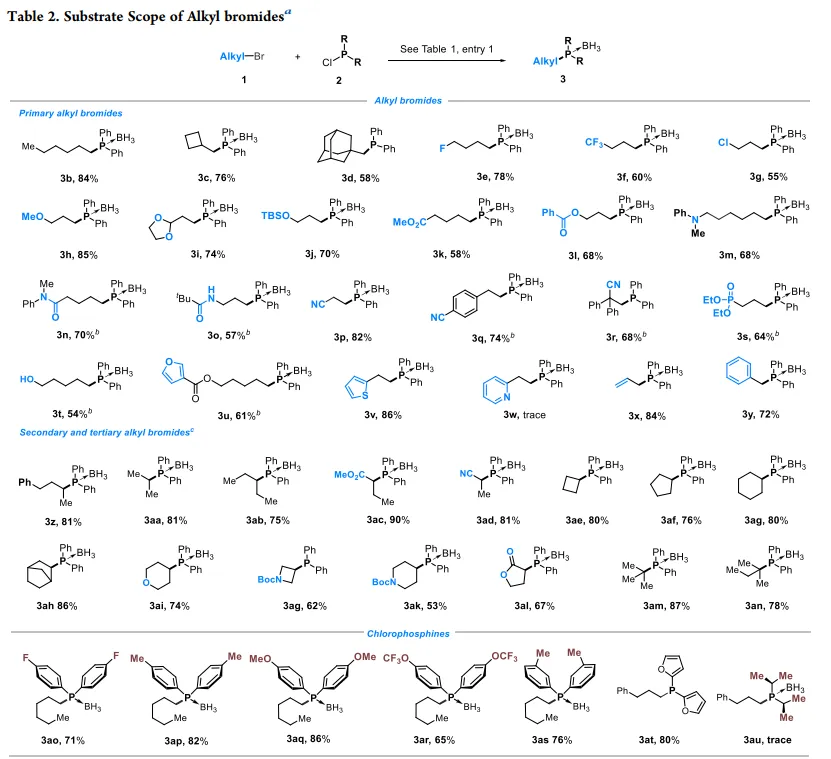
- 可高效合成 1,1-、1,4-、1,12 - 二取代二苯基膦等双膦化合物,为双齿膦配体的合成提供新路线;
- 可实现膦基向生物活性分子的高效引入,从 D - 薄荷醇、二丙酮果糖、D - 生物素、脱氢松香酸、雌酮、扎托洛芬衍生的烷基溴均能与二苯基氯化膦顺利偶联,产物分离收率达 56%-82%,体现了该方法在复杂分子后期官能团化中的价值。
4. 机理研究- 自由基捕获实验:加入 BHT、TEMPO 等自由基清除剂会显著抑制产物生成,TEMPO 可捕获烷基自由基和二苯基膦基自由基,证实反应为自由基机理;Ni (0) 可介导烷基溴产生烷基自由基,Ni (0) 和 Ni (I) 均可活化氯膦生成膦基自由基。
- 自由基钟实验:(溴甲基) 环丙烷仅生成开环产物,6 - 溴 - 1 - 己烯生成烯烃保留产物和环化产物,进一步证实烷基溴的活化通过自由基途径。
Ni (0) 与烷基溴发生单电子转移,生成烷基自由基和 Ni (I)-Br 中间体;Ni (I) 捕获烷基自由基形成烷基 - Ni (II) 配合物;该配合物与 Ni (0)/Ni (I) 活化氯膦生成的膦基自由基结合,得到烷基 (二苯基膦基)-Ni (III) 物种;该物种经还原消除生成目标产物并释放 Ni (I)-Br;Mn 粉将 Ni (I) 还原为 Ni (0),完成催化循环。
开发了一种镍催化自由基接力策略,实现了氯膦与烷基溴的还原交叉偶联,直接构建 C (sp³)-P 键。该策略的核心是利用镍的单电子氧化还原能力协同活化两种前体:低价镍向烷基溴的单电子转移原位生成烷基自由基,有效避免了传统 Ni (II) 途径中常见的 β- 氢消除副反应;氯膦在还原条件下被活化为磷自由基。镍催化剂作为电子库,选择性捕获并偶联这些活性中间体,高效得到目标有机磷产物。该方法为从易得的卤代物前体合成高价值烷基膦提供了新颖、通用的路线。
核心内容总结:
本文报道了一种镍催化还原交叉偶联构建 Csp³-P (III) 键的新方法,解决了传统有机磷合成的诸多痛点,核心亮点和结论如下:
- 方法创新首次实现未活化烷基溴与易得氯膦的直接一步偶联,无需预制备有机金属试剂或多步合成磷源,显著提升了合成的原子和步骤经济性。
- 反应优势克服了烷基底物活性低、β- 氢消除、氯膦易水解 / 失活等关键难题,反应条件温和(0℃),官能团耐受性极广,酸性性质子、多种杂环、卤代、含氧 / 氮 / 磷官能团均能兼容。
- 底物广泛适用于伯、仲、叔烷基溴与多种芳基 / 杂环取代氯膦的偶联,仅烷基取代氯膦不适用;可高效合成大位阻、富电子的三烷基膦化合物。
- 应用价值不仅能合成双齿膦配体,还可实现膦基向 D - 生物素、雌酮、扎托洛芬等生物活性分子的后期官能团化,收率 56%-82%,在催化配体设计、药物合成、材料科学中具有重要应用前景。
- 反应机理为自由基接力机理,Ni (0) 活化烷基溴生成烷基自由基,Ni (0)/Ni (I) 活化氯膦生成磷自由基,二者通过镍中间体偶联,最终经还原消除得到产物,Mn 粉作为还原剂实现镍催化剂的循环。
- 最优条件以 Ni (二甘醇) Br₂为催化剂、2,2':6',2''- 三联吡啶为配体、Mn 为还原剂、DMF 为溶剂,是该反应的最优组合,仲 / 叔烷基溴反应可更换叔丁基取代三联吡啶配体并升温至 40℃。
该方法为高价值烷基膦化合物的合成提供了简洁、通用的新路线,有望推动有机磷化学在催化、生物医药和材料领域的进一步发展。
A Nickel-Catalyzed Method for Csp3−P(III) Bond Formation: Efficient
Transformation of Chlorophosphines with Alkyl Bromides
期刊及doi:ACS Catal. 2026, XXX, XXX−XXX
https://doi.org/10.1021/acscatal.5c08800