南昌大学第二附属医院 邹芳(IF 12.6):硒缓释裂褶菌多糖通过调节肠道菌群 T 细胞平衡,减轻 1 型糖尿病患者的胰腺和肺部炎症损伤
- 2026-04-19 13:12:38

各位热爱科研的小伙伴们,今天为大家推介2026年3月14日发表在 《Journal of Nanobiotechnology》杂志的研究性文章。该文章由南昌大学第二附属医院 邹芳副主任医师等团队共同完成,主要研究方向为糖尿病、糖尿病慢性并发症、甲状腺疾病、肾上腺疾病、性腺疾病、骨质疏松症、痛风、性腺相关内分泌疑难疾病等。文章题目“Selenium-loaded sustained-release schizophyllan alleviates pancreatic and pulmonary inflammatory damage in type 1 diabetes mellitus by modulating gut microbiota and T cell balance”。本研究旨在开发一种硒负载的缓释裂褶菌多糖复合物,并探究其通过调节肠道菌群和Toll样受体4/核因子κB信号通路,从而缓解与1型糖尿病相关的炎症免疫反应的具体机制,并且围绕硒纳米颗粒、裂褶菌多糖、肠道菌群、Toll样受体4/核因子κB信号通路、免疫稳态、1型糖尿病等关键词展开研究。

背景:1型糖尿病是一种由免疫系统介导、导致胰腺β细胞被破坏的慢性自身免疫性疾病。近年来的研究表明,沿着“肠道-肺部”轴的免疫失调在其发病机制中扮演着关键角色。然而,目前针对这一全身性免疫调控网络的干预策略尚不完善。
目的:开发一种负载硒的缓释裂褶菌多糖复合物(Se/s-SPG)。研究该复合物是否能通过调节肠道微生物群和Toll样受体4(TLR4)/核因子κB(NF-κB)信号通路,缓解T1DM相关的胰腺及肺部炎症免疫反应。
方法:
1.材料制备: 制备Se/s-SPG纳米复合物,并进行理化性质表征(TEM, DLS, XRD等)。
2.动物模型: 使用非肥胖糖尿病(NOD/LtJ)小鼠建立T1DM模型,分为PBS对照组、SeNPs组、SPG组、Se/s-SPG组及干预组(过表达p65)。
3.代谢评估: 血糖监测、糖耐量试验(OGTT)、胰岛素分泌检测。
4.组织病理学: H&E染色观察胰腺、肠道和肺组织结构;TUNEL染色检测凋亡。
5.分子生物学: 16S rRNA测序分析肠道菌群;转录组测序(RNA-seq)分析差异基因;WB、ELISA、免疫荧光检测TLR4/NF-κB通路及相关因子。
6.细胞实验: 使用Caco-2细胞模型验证屏障保护作用。
结果:
1.材料特性: Se/s-SPG呈球形,粒径分布均匀(~31 nm),具有良好的稳定性和缓释性能。
2.代谢改善: Se/s-SPG显著降低了空腹血糖,改善了糖耐量,增加了胰岛素分泌,修复了胰岛结构。
3.菌群调节: Se/s-SPG增加了肠道微生物多样性,重塑了菌群结构(如增加有益菌Lactobacillus,减少有害菌),恢复了肠道微生态平衡。
4.屏障修复与抗炎:肠道: 修复了肠道屏障完整性(上调ZO-1, Occludin等),抑制了TLR4/NF-κB通路,减少了炎症因子(IL-6, TNF-α)。肺部: 减轻了肺部炎症和纤维化,改善了肺泡结构,证实了“肠-肺轴”的调节作用。
5.免疫平衡: 调节了CD4+ T细胞亚群平衡(减少Th1/Th17,增加Treg),促进了巨噬细胞向抗炎M2型极化。
结论:Se/s-SPG复合物作为一种新型纳米递送系统,能够通过调节肠道菌群和抑制TLR4/NF-κB信号通路,重塑“肠道-肺部”轴的免疫稳态,从而有效减轻1型糖尿病相关的胰腺和肺部损伤,为1型糖尿病的治疗提供了一种基于免疫-菌群调控的多靶点新策略。
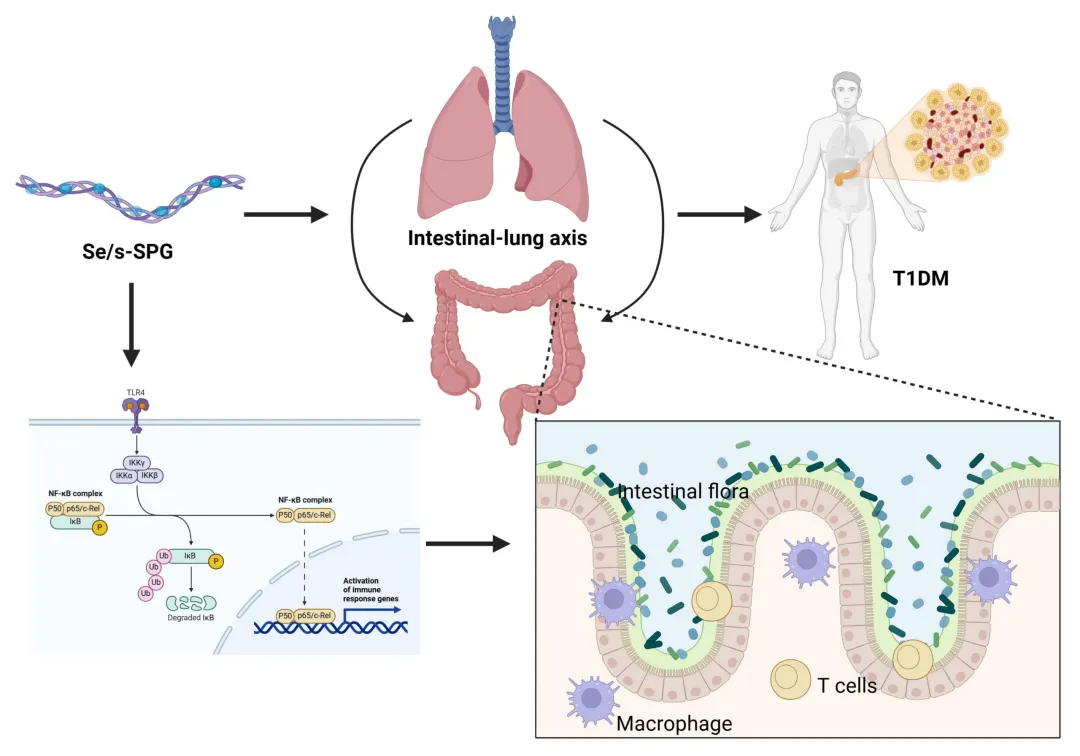
机制图
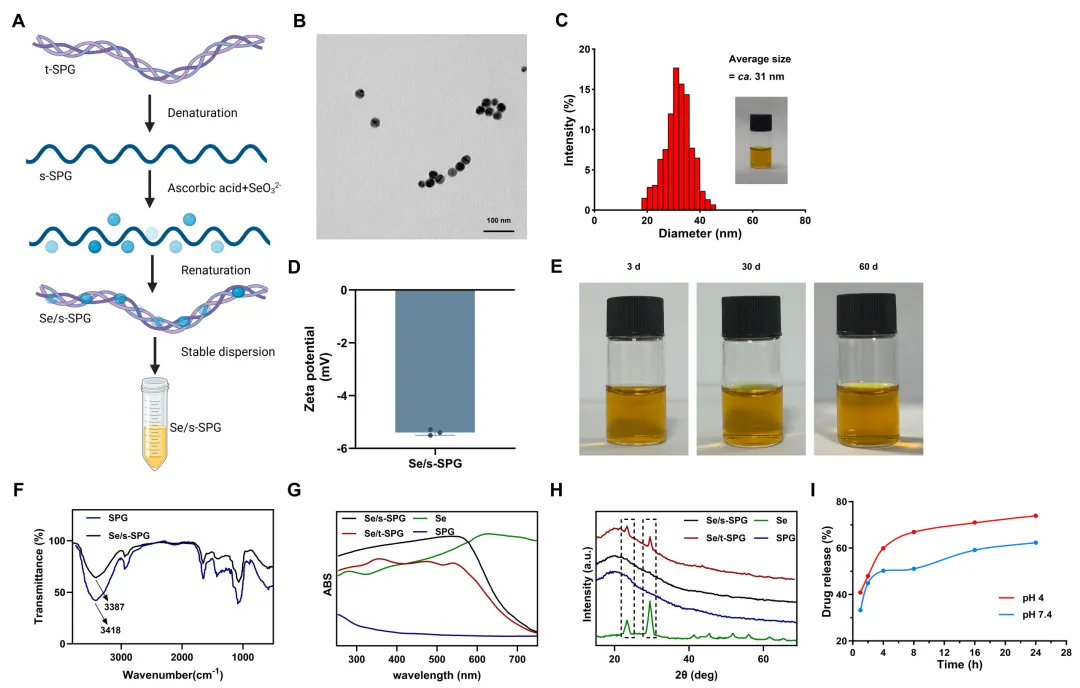
图1 Se/s-SPG纳米复合物的制备与理化表征。
(A) Se/s-SPG合成过程示意图,展示SPG包封SeNPs的过程;(B) TEM图像,显示Se/s-SPG的形态;(C) DLS分析,显示Se/s-SPG在水溶液中的流体动力学尺寸分布;(D) Zeta电位测量,显示Se/s-SPG胶体的表面电荷特征;(E) Se/s-SPG溶液在室温避光储存3天、30天和60天后的稳定性评估;(F) FTIR分析,显示SPG与SeNPs之间的相互作用;(G) UV-Vis光谱,比较SeNPs、SPG和Se/s-SPG的吸收谱;(H) XRD分析,显示SeNPs与Se/s-SPG之间的晶体结构差异;(I) Se/s-SPG的体外释放曲线。
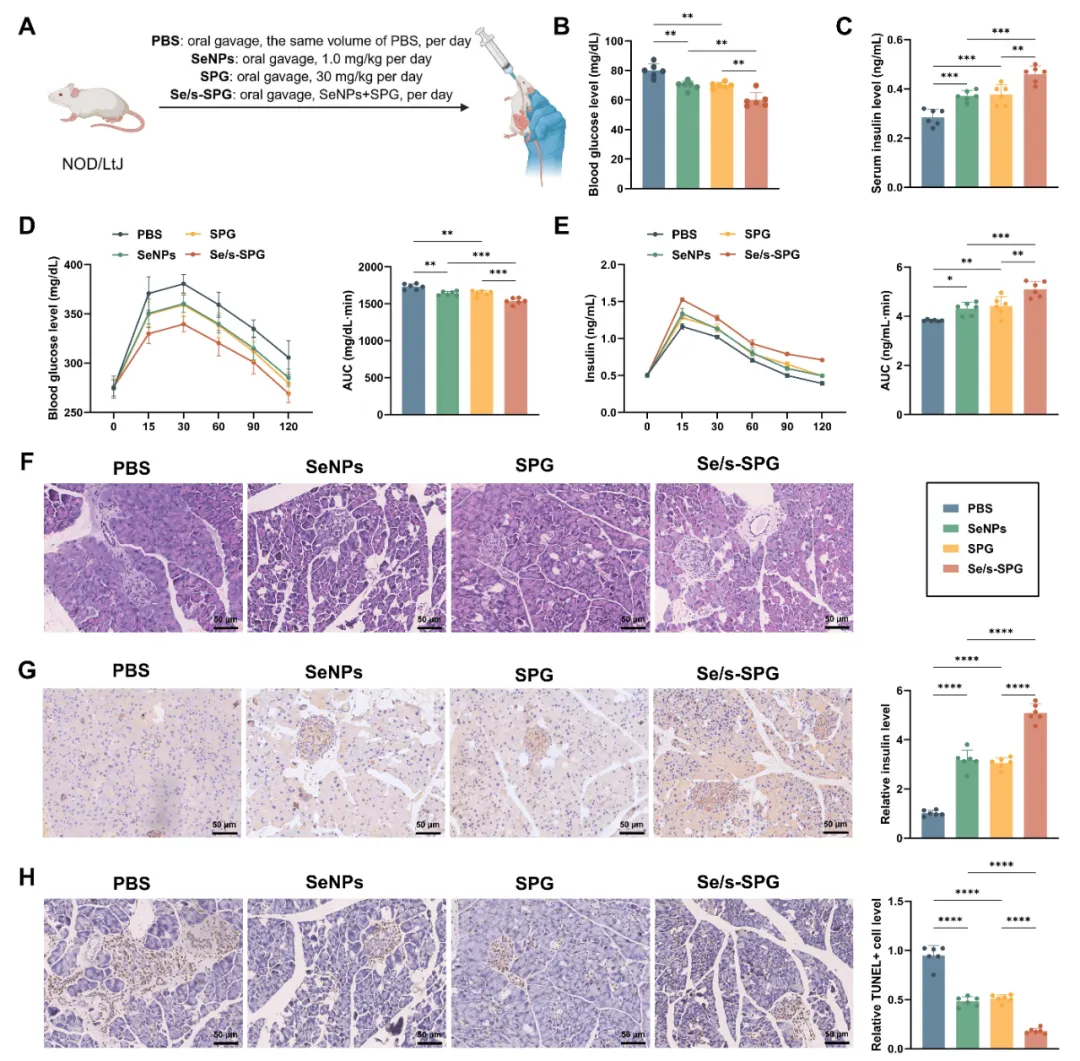
图2 Se/s-SPG改善NOD小鼠血糖水平及胰腺功能。
(A) 小鼠分组及干预时间线示意图;(B) 使用血糖仪测定的空腹血糖水平;(C) ELISA法测定的血清胰岛素浓度;(D) OGTT显示各时间点血糖水平,以及动态血糖曲线和AUC分析;(E) OGTT期间测定的血清胰岛素水平,及相应的胰岛素分泌曲线和AUC;(F) 胰腺组织H&E染色,评估结构完整性和炎性细胞浸润;(G) 胰腺组织胰岛素表达IHC染色;(H) TUNEL染色检测胰腺组织细胞凋亡。
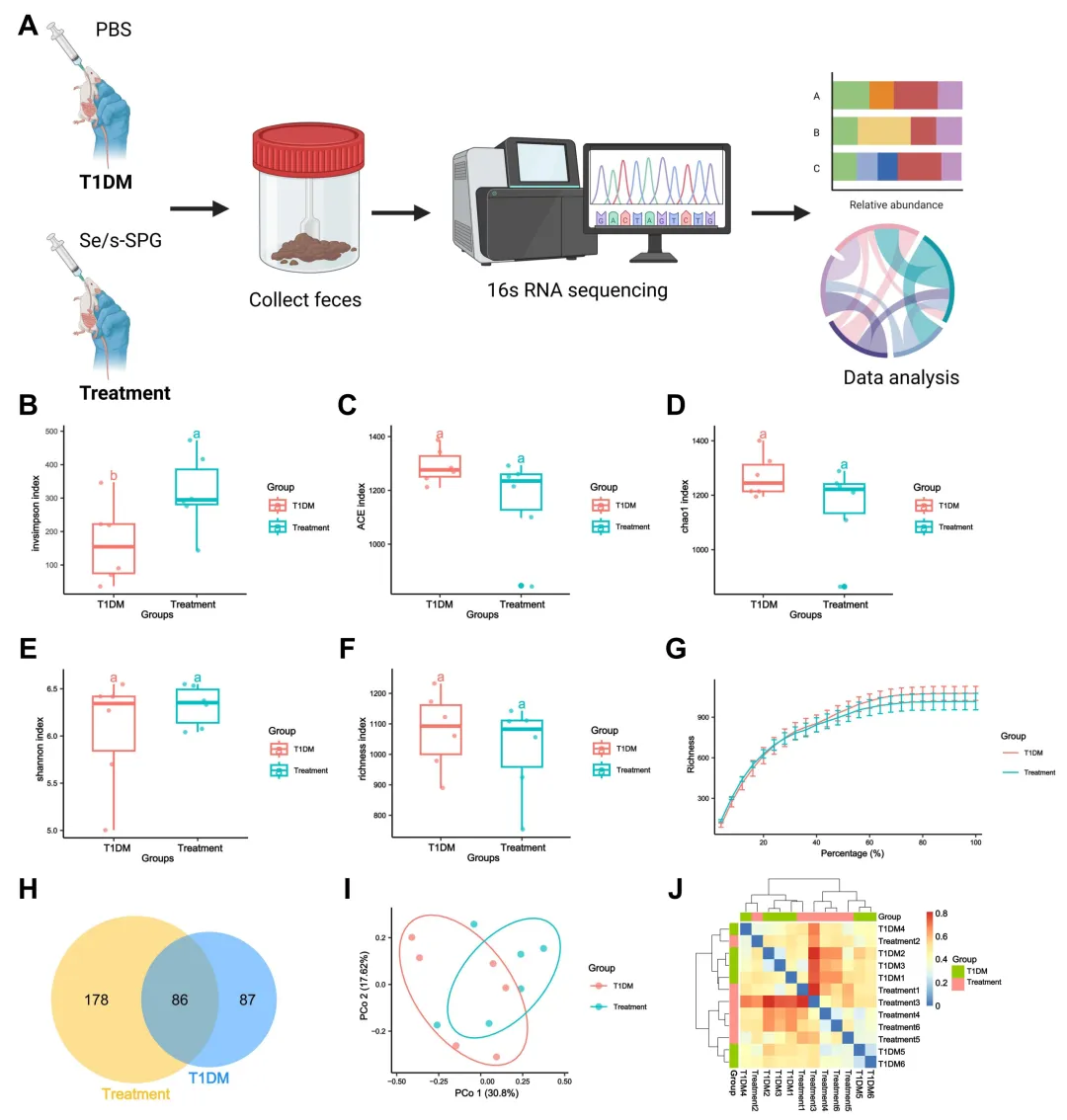
图3 Se/s-SPG干预对T1DM小鼠肠道菌群多样性与群落结构的影响。
(A) T1DM组与治疗组粪便样本16S rRNA高通量测序的工作流程示意图;(B) 使用InvSimpson指数进行α多样性分析,评估微生物多样性;(C-F) 使用Shannon、Chao1、ACE和Richness指数评估微生物丰富度;(G) 稀释曲线,评估测序深度;(H) Venn图,显示组间共有及独有OTU;(I) 基于β多样性的主坐标分析,评估微生物群落结构差异;(J) Bray-Curtis距离热图,显示样本间微生物组成的相似性。
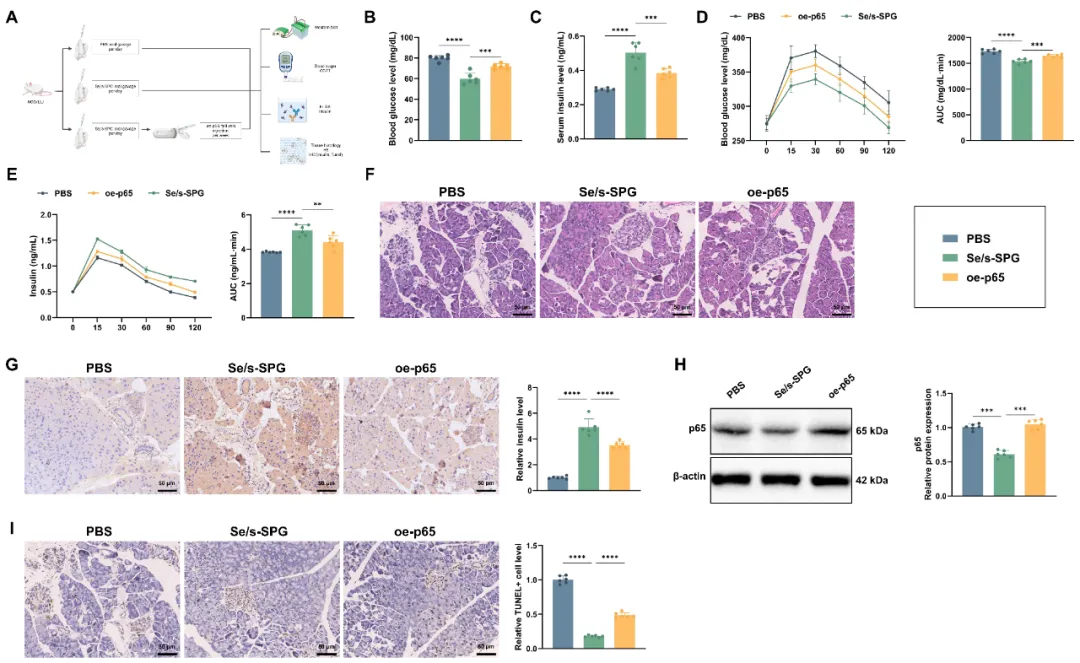
图4 Se/s-SPG通过TLR4/NF-κB通路改善糖尿病小鼠葡萄糖代谢紊乱及胰腺功能障碍。
(A) 实验设计示意图,显示模型组、Se/s-SPG组及Se/s-SPG+oe-p65组的干预方案及样本处理流程;(B) 血糖仪测定的空腹血糖水平;(C) ELISA法测定的血清胰岛素浓度;(D) OGTT显示动态血糖水平随时间变化,及相应AUC分析;(E) OGTT期间ELISA测定的血清胰岛素水平,及胰岛素分泌曲线和AUC;(F) H&E染色评估胰腺组织结构和炎性细胞浸润;(G) IHC染色评估胰腺组织中胰岛素阳性细胞的分布与表达;(H) Western blot检测胰腺组织中p65表达及定量分析;(I) TUNEL染色检测胰腺组织中凋亡细胞数量。
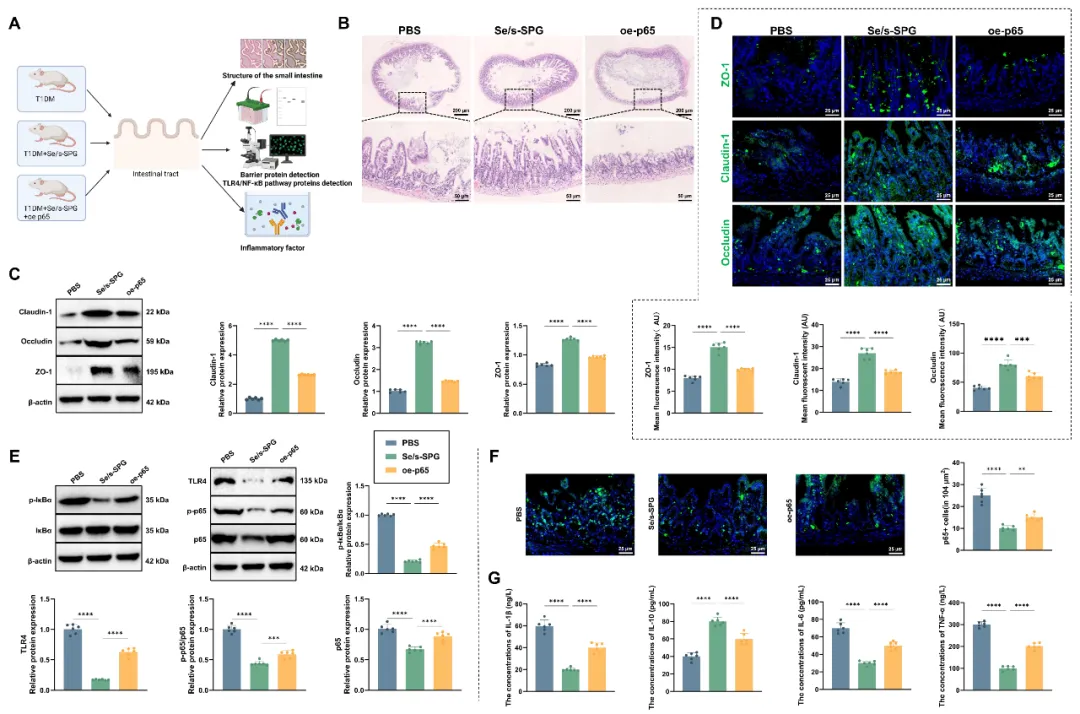
图5 Se/s-SPG通过抑制TLR4/NF-κB通路恢复糖尿病小鼠肠道屏障结构与功能。
(A) T1DM组、Se/s-SPG组及Se/s-SPG+p65过表达组小肠组织处理流程示意图;(B) H&E染色显示小肠绒毛形态及炎性细胞浸润;(C) Western blot检测肠道组织中屏障相关蛋白ZO-1、Occludin和Claudin-1的表达;(D) 免疫荧光检测ZO-1、Occludin和Claudin-1在肠上皮界面的定位与表达;(E) Western blot检测小肠组织中TLR4、磷酸化p65、p65及磷酸化IκBα蛋白水平;(F) 免疫荧光分析p65核转位,评估NF-κB通路激活状态;(G) ELISA检测肠道组织中促炎细胞因子(IL-6、TNF-α、IL-1β)及抗炎细胞因子IL-10水平。
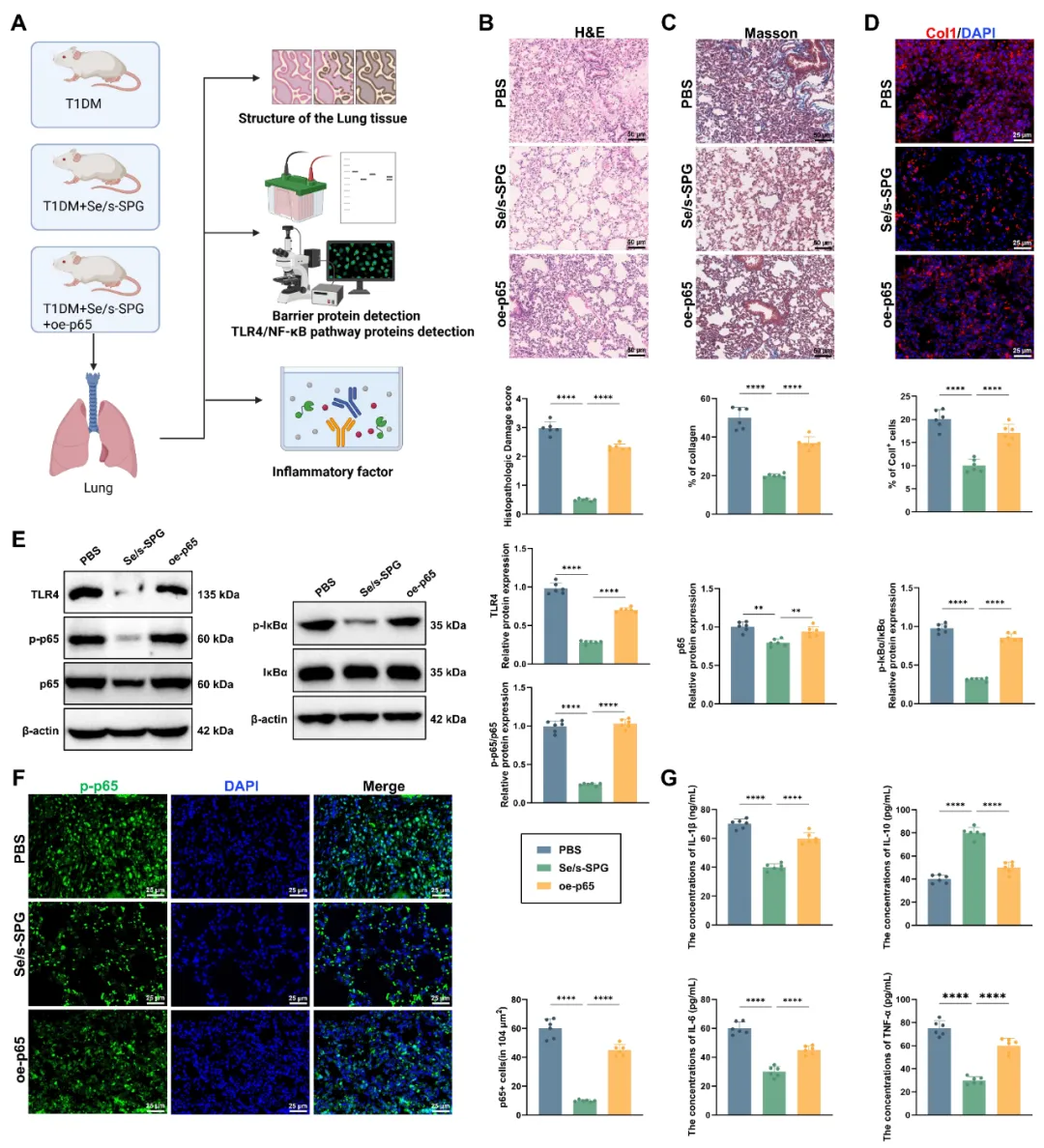
图6 Se/s-SPG通过抑制TLR4/NF-κB信号通路减轻糖尿病小鼠肺组织损伤及纤维化进展。
(A) 实验设计示意图,显示模型组、Se/s-SPG组及Se/s-SPG+p65过表达组肺组织处理流程;(B) H&E染色显示肺泡结构、间质增生及炎性细胞浸润;(C) Masson三色染色评估肺组织胶原沉积,蓝色区域代表胶原纤维;(D) 免疫荧光检测肺组织中胶原蛋白I的表达与空间分布;
(E) Western blot检测肺组织中TLR4、磷酸化p65、p65及磷酸化IκBα表达水平;(F) 免疫荧光分析p65核转位,评估NF-κB通路激活状态;(G) ELISA定量检测肺组织中促炎细胞因子(IL-6、TNF-α、IL-1β)及抗炎细胞因子IL-10水平。
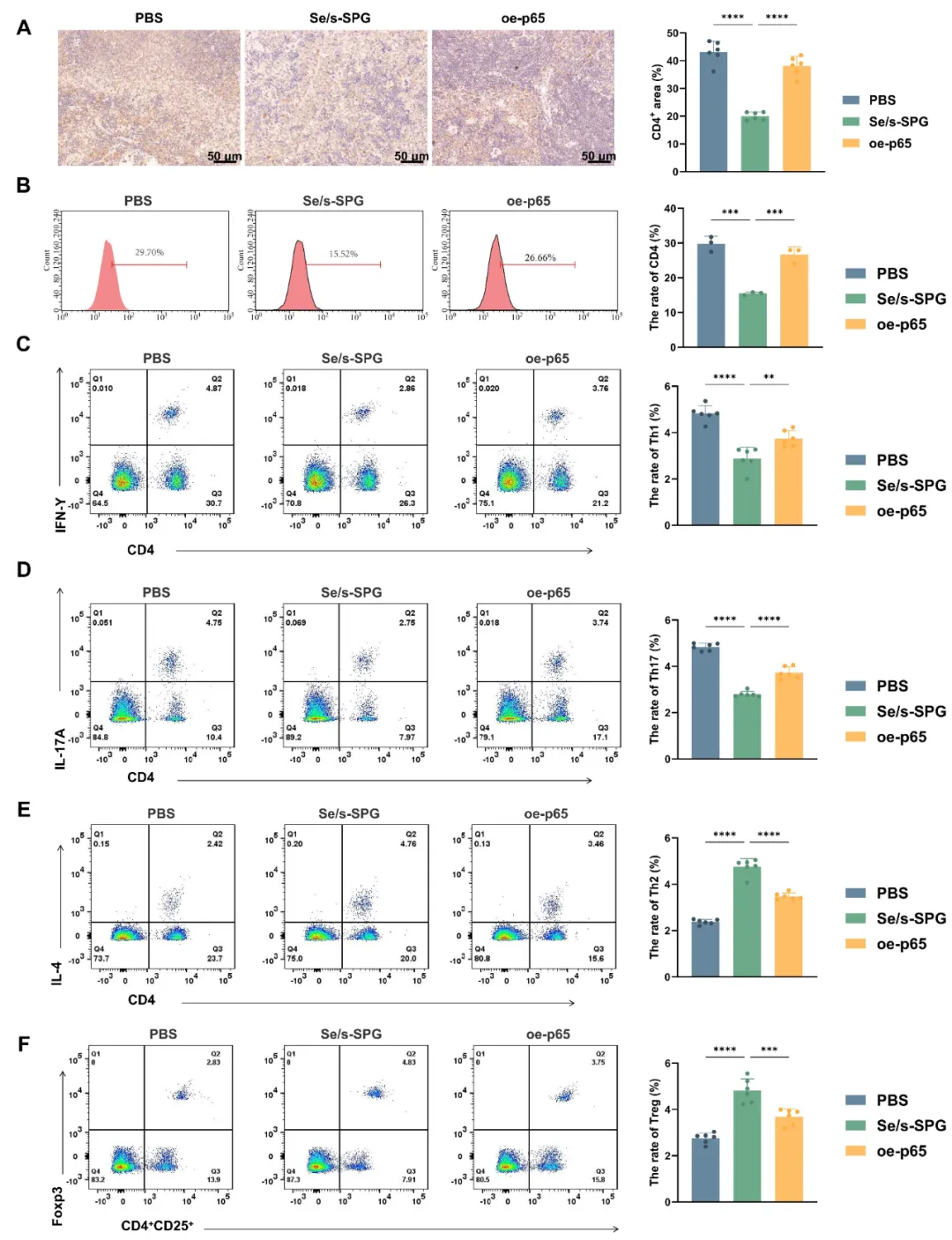
图7 Se/s-SPG恢复CD4+ T细胞亚群的免疫平衡。
(A) 小鼠脾脏组织IHC染色,显示CD4+细胞的分布与表达水平;(B) 流式细胞术分析各组脾脏单个核细胞中CD4+ T细胞的总体比例;(C) 流式细胞术分析Th1细胞;(D) 流式细胞术分析Th2细胞;(E) 流式细胞术分析Th17细胞;(F) 流式细胞术分析Treg细胞。
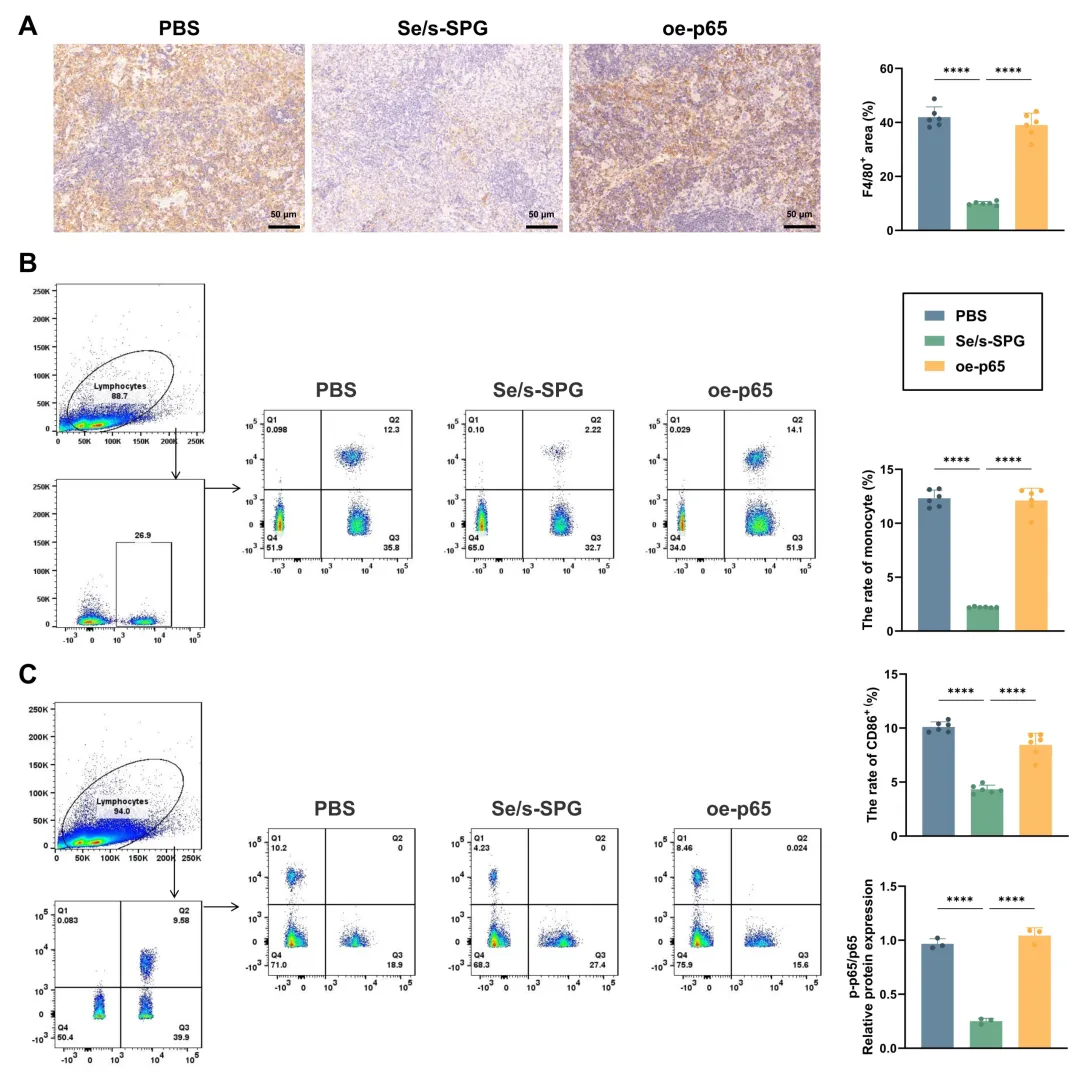
图8 Se/s-SPG调节巨噬细胞活化并促进M2型极化。
(A) 各组小鼠脾脏组织F4/80 IHC染色,评估巨噬细胞浸润情况;(B) 流式细胞术分析脾脏中单核细胞群;(C) 流式细胞术定量分析脾脏中CD86+(M1型)和CD206+(M2型)巨噬细胞的比例。
综上所述,我们的研究系统阐明了一种新型硒负载缓释裂褶菌多糖复合物通过调节“肠道-肺部”轴来改善1型糖尿病免疫失调的作用机制。研究证实,Se/s-SPG能够显著改善糖尿病小鼠的血糖代谢和胰腺功能,同时有效修复肠道屏障、恢复菌群多样性并减轻远端肺部炎症。深入的机制分析表明,这些治疗效果主要依赖于对TLR4/NF-κB信号通路的抑制,以及对CD4+ T细胞亚群(如Th1、Th17、Treg)和巨噬细胞极化的协同调节作用。从科学意义上看,本研究揭示了“肠道-肺部”轴在1型糖尿病相关免疫失衡中的核心地位,并为纳米材料介导的免疫调节提供了清晰的分子框架。从转化前景来看,Se/s-SPG复合物展现出了良好的生物安全性和多靶点治疗潜力,有望作为一种新型的营养-免疫佐剂,为1型糖尿病,尤其是早期干预和儿童患者的辅助治疗,提供一种安全、有效且具有广阔应用前景的临床转化策略。


需要领取文献的同学,后台私信“86”,即可领取!
《医研三人行》公众号推送文章仅为学术交流使用,仅供读者参考。公众号中“原创”标识仅代表原创编译之作,不代表本公众号对文本主张版权。版权归文章作者所有。
1、新思路!嘉兴大学 徐龙副教授&嘉兴市中医医院 唐洁:转录组学和代谢组学揭示了功能性纳米塑料诱导的男性生殖损伤以及白藜芦醇的拮抗作用
3、遵义医科大学 李彩兰教授(IF 12.6):植物源性外泌体样纳米囊泡在溃疡性结肠炎治疗中的生物发生、制备、表征、治疗机制及安全性评价



